Углеродные наноматериалы для очистки воды, загрязненной тяжелыми металлами, и восстановления окружающей среды
Аннотация
Нанотехнологии - это передовая область науки, способная решать множество экологических проблем, контролируя размер и форму материалов в наномасштабе. Углеродные наноматериалы уникальны из-за их нетоксичной природы, большой площади поверхности, более легкого биоразложения и особенно полезного восстановления окружающей среды. Загрязнение воды тяжелыми металлами является серьезной проблемой и представляет большой риск для здоровья человека. Углеродным наноматериалам уделяется все больше и больше внимания из-за их превосходных физико-химических свойств, которые можно использовать для глубокой очистки воды, загрязненной тяжелыми металлами. Углеродные наноматериалы, а именно углеродные нанотрубки, фуллерены, графен, оксид графена и активированный уголь, имеют большой потенциал для удаления тяжелых металлов из воды из-за их большой площади поверхности, наноразмеров и доступности различных функций, а также их легче химически модифицировать и переработанный. В этой статье мы рассмотрели последние достижения в области применения этих углеродных наноматериалов при очистке воды, загрязненной тяжелыми металлами, а также подчеркнули их применение для восстановления окружающей среды. Также обсуждались токсикологические аспекты углеродных наноматериалов.
Введение
Загрязнение определяется как присутствие нежелательного химического объекта / объектов, препятствующих естественному процессу или вызывающих неблагоприятное воздействие на живые организмы и окружающую среду [1,2,3]. Индустриализация и огромный рост населения, ведущие к растущей урбанизации, вызывают рост загрязнения тревожными темпами [2, 4]. Улучшение качества воды, почвы и воздуха - огромная задача современной эпохи. Выявление и обработка загрязнителей окружающей среды и их предотвращение - ключевой шаг в защите окружающей среды. Материаловедение играет жизненно важную роль в достижении цели чистой окружающей среды, а технологии материаловедения за последнее десятилетие достигли экспоненциального прогресса, особенно в области наноматериалов [1, 5]. Чистая и чистая вода становится дефицитной из-за индустриализации, и мир сталкивается с нехваткой чистой воды, особенно в развивающихся странах [6]. Загрязняющими веществами воды могут быть органические вещества, бактерии, вирусы, красители и ионы тяжелых металлов, таких как свинец, кадмий, цинк, никель, мышьяк, хром и ртуть, не поддающиеся биологическому разложению, представляющие большой риск для здоровья человека. Ионы тяжелых металлов могут вызывать множество побочных эффектов, таких как рак, поражение почек, гепатит, выкидыши, анемия, энцефалопатия и нефритический синдром [7,8,9,10]. Ионы свинца выделяются в окружающую среду, как правило, в горнодобывающей промышленности, свинцово-кислотных аккумуляторах, в бумажной, стекольной и полировальной отраслях. Кадмий обычно содержится в воде, сбрасываемой при проектировании гальванических элементов батарей, фотоэлектрических элементов, металлургических процессов и фабрик по производству тканей [11]. Ионы никеля могут вызывать кожные заболевания при контакте с мусором, молниями, часами, монетами и т. Д. язва слизистой носа [12]. На рисунке 1 показана адсорбция ионов тяжелых металлов на углеродном наноматериале (графене), а на рисунке 2 показаны различные источники загрязнения тяжелыми металлами в окружающей среде. Из-за этих серьезных побочных эффектов удаление ионов тяжелых металлов из воды имеет первостепенное значение для спасения человеческих жизней от таких проблемных проблем со здоровьем. Ионы токсичных металлов можно удалить с помощью множества методов, таких как ионный обмен, обратный осмос, фильтрация с осаждением, биосорбция, коагуляция и экстракция [13, 14]. Адсорбция считается лучшим методом, поскольку она рентабельна, очень эффективна и проста в эксплуатации для удаления следовых количеств ионов тяжелых металлов [15]. Для обработки воды применялись различные материалы, такие как адсорбенты растений и материалы органической природы, особенно гуминовая кислота, которая широко применялась для дезинфекции воды и удаления ионов тяжелых металлов [8, 16,17,18,19]. Wang et al. всесторонне рассмотрели гуминовую кислоту и ее нанокомпозит для очистки воды [20].
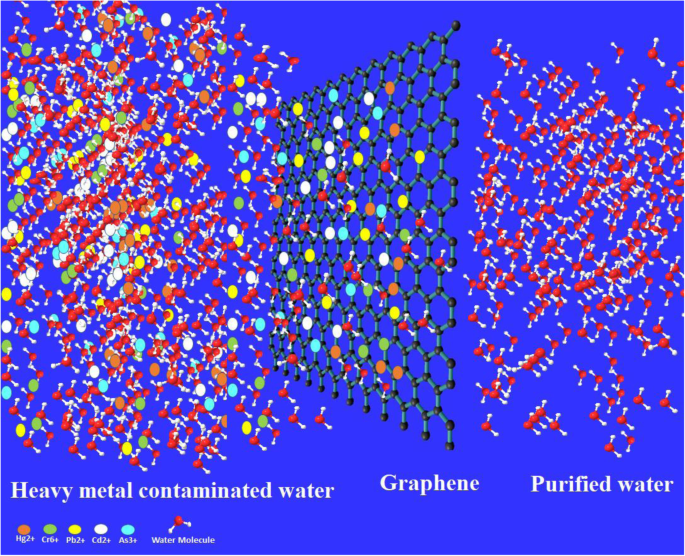
Графическое изображение, показывающее, что процесс очистки воды, загрязненной тяжелыми металлами, с использованием графена и других материалов на основе углерода также может делать то же самое
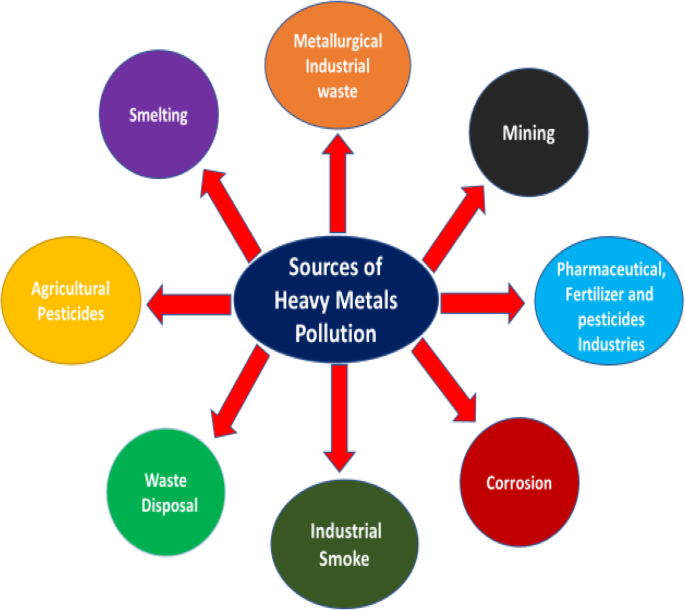
Источники загрязнения окружающей среды тяжелыми металлами
Платформа нанотехнологий находит применение почти во всех областях, таких как наука об окружающей среде, здравоохранение, электроника, промышленное разделение, большие / малые установки для очистки воды, катализаторы, накопители энергии и производство энергии [21,22,23]. Наноматериалы обеспечивают специальную платформу для очистки загрязненной воды из-за большой площади поверхности наносорбентов и их способности к химической модификации и более легкой регенерации. Наноматериалы все больше и больше используются для удаления из воды различных типов загрязнителей, а именно органических веществ, ионов металлов, биологических загрязнителей и мышьяка [24,25,26,27]. Углеродные наноматериалы, а именно графен, оксид графена, углеродные нанотрубки, фуллерены и активированный уголь, широко используются в накопителях энергии, датчиках, электронике, очистке воды, доставке лекарств, диагностике заболеваний и т. Д. Благодаря своим исключительным химическим, механическим, термическим и тепловым свойствам. Электрические характеристики. В этой статье мы попытались рассмотреть последние достижения в применении углеродных наноматериалов, а именно фуллеренов, углеродных нанотрубок (УНТ), графена, оксида графена и активированного угля для очистки воды, загрязненной ионами тяжелых металлов.
Здоровье человека и токсичность тяжелых металлов
Тяжелые металлы обычно определяются на основе их атомного веса; однако тяжелые металлы также относятся к элементам, токсичным для живых существ [28]. Некоторые тяжелые металлы в различных формах и дозах смертельны для здоровья человека и других живых существ (Таблица 1). Часто тяжелые металлы считаются токсичными; однако более легкие металлы также могут быть смертельными, например бериллий и литий. Не все тяжелые металлы ядовиты для здоровья, некоторые из них являются фундаментальными, например, железо и Cr (III). Наиболее известные токсичные металлы - это Pb, Cd, Cr, Mn, Hg, As и радиоактивные металлы. Радиоактивные металлы обладают как радиологической, так и химической токсичностью. Токсичность тяжелых металлов оказалась серьезной угрозой, и с ними связано множество рисков для здоровья. Смертельное воздействие этих металлов заключается в том, что они не играют никакой биологической роли; однако они могут имитировать как элемент тела и вмешиваться в метаболические и другие биологические процессы. Некоторые металлы, такие как алюминий, могут легко удаляться системой выведения, в то время как определенные металлы накапливаются в пищевой цепи и организме. Токсичность, вызванная металлами, зависит от дозы, пути воздействия и времени контакта (например, острая или хроническая). Подробная информация о токсичности, связанной с различными тяжелыми металлами, приводится ниже.
Токсичность ртути (Hg)
Ртуть (Hg) представляет собой элемент d-блока с атомным номером 80 и находится в жидкой форме при стандартных условиях. Ртуть находится в месторождениях сульфида ртути, называемого киноварью. Загрязнение ртутью вызывается фармацевтической промышленностью, консервированием целлюлозы и бумаги, производством каустической соды, сельским хозяйством и т. Д. [47]. Ртуть является наиболее токсичным тяжелым металлом в окружающей среде, и отравление ртутью называют розовой болезнью, также известной как акродиния. Ртуть может сочетаться с органическими и неорганическими соединениями. Повышенные уровни воздействия ртути в любой форме могут повредить почки, мозг, развивающийся плод и т. Д. [48]. Агентство по охране окружающей среды объявило метилртуть и хлорид ртути канцерогенными. Воздействие ртути также может вызвать повреждение легких, кожную сыпь, проблемы с памятью и выпадение волос. Всемирная организация здравоохранения (ВОЗ) установила стандарт для питьевой воды с более низким содержанием ртути - 0,01 мг / л [29].
Токсичность свинца (Pb)
Свинец (Pb) представляет собой элемент с атомным номером 82 и считается тяжелым металлом с серебристо-голубоватым оттенком, который под действием воздуха становится тускло-серым [30]. Существуют различные источники загрязнения свинцом, в основном отходы аккумуляторной промышленности, удобрения и пестициды, металлизация и отделочные операции, выхлопные газы, добавки в бензин, пигменты в автомобилях и выплавка руд. Этот тяжелый токсичный металл становится проблемой для окружающей среды и здоровья во всем мире из-за его широкого использования [31]. Свинец (Pb) является канцерогенным элементом, объявленным Агентством по охране окружающей среды (EPA). Отравление свинцом - это термин, используемый для обозначения его токсичности, и оно может быть острым или хроническим. Отравление свинцом может вызвать умственную отсталость, врожденные дефекты, такие как аутизм, аллергию, дислексию, паралич, повреждение мозга и почек, а также может привести к смерти [32].
Токсичность мышьяка (As)
Мышьяк представляет собой металлоидный элемент с атомным номером 33 и встречается в минеральной форме, обычно в сочетании с серой, некоторыми другими металлами, солями железа, кальция, натрия и меди, а также в чистой элементной форме [33]. Вода загрязнена пестицидами на основе мышьяка, отложениями природных минералов и неправильной утилизацией реагентов или химикатов на основе мышьяка. Мышьяк в форме арсената и арсенита смертельно опасен для окружающей среды и живых существ. Мышьяк нарушает протоплазму клеток, взаимодействуя с сульфгидрильной группой клеток, вызывая нарушение дыхания и влияя на митоз и клеточные ферменты [34].
Токсичность кадмия (Cd)
Кадмий имеет атомный номер 48 и является голубовато-белым мягким металлом, имеющим химические свойства, подобные ртути и цинку группы 12 [30]. Они производятся при плавке руд, гальванике, батареях, пластификаторах, сплавах, пигментах, атомной промышленности и сигаретном дыме. Как правило, кадмий присутствует в окружающей среде в небольших количествах; однако промышленные отходы значительно увеличили эти уровни. Токсичность, вызванная кадмием, может вызвать повреждение почек, дыхательной системы и скелета и является канцерогенным для человека [30, 33]. Кадмий занимает седьмое место среди самых токсичных металлов Агентства по регистрации токсичных веществ и заболеваний (ATSDR) [34].
Токсичность хрома (Cr)
Хром (Cr) - это элемент с атомным номером 24 и стальным серым цветом [35]. Хром находится в разных состояниях, например, в двухвалентном, четырехвалентном, пятивалентном и шестивалентном состояниях; однако трехвалентные и шестивалентные формы являются наиболее стабильными. Хром (III) - важная пищевая добавка для людей и животных [35]. Однако форма хрома (VI) является высокотоксичной и канцерогенной по своей природе [36, 37]. Хром производится в матрице окружающей среды (воздух, вода и почва) из различных источников, например, из сточных вод и воздуха, которые в основном выбрасываются в металлургической и химической промышленности. Шестивалентный хром Cr (VI) - промышленный загрязнитель, признанный канцерогеном для человека [38, 39]. Концентрация Cr (VI) в грунтовых и поверхностных водах превышает норму, и Всемирная организация здравоохранения (ВОЗ) установила предел в 50 мкг на литр [40].
Токсичность цинка (Zn)
Цинк (Zn) - это элемент с атомным номером 30, который находится во 2-й группе периодической таблицы. Хотя цинк является важным следовым металлом для человека, чрезмерное поглощение цинка может подавить поглощение железа. Ионы цинка очень токсичны для растений, позвоночных рыб, беспозвоночных и т. Д. [41,42,43].
Классификация углеродных наноматериалов на основе их размеров
Наноматериалы, имеющие все три размера менее 100 нм, называются нульмерными (0-D) наноматериалами; примерами являются фуллерен и квантовые точки [44]. Наноматериалы, имеющие только один размер больше 100 нм и два размера меньше 100 нм, называются одномерными (1-D) наноматериалами, например, углеродными и титановыми нанотрубками [45, 46]. Наноматериалы, два размера которых превышают 100 нм, называются двумерными наноматериалами, известным примером является графен. Трехмерные материалы, все размеры которых превышают 100 нм, называются трехмерными (3-D) материалами; примерами являются графит и некоторые композиты из наноматериалов [46]. На рисунке 3 показаны некоторые типичные известные структурные углеродные материалы с разными размерами, например фуллерен 0-D, одностенная углеродная нанотрубка 1-D, графен 2-D и графит 3-D.
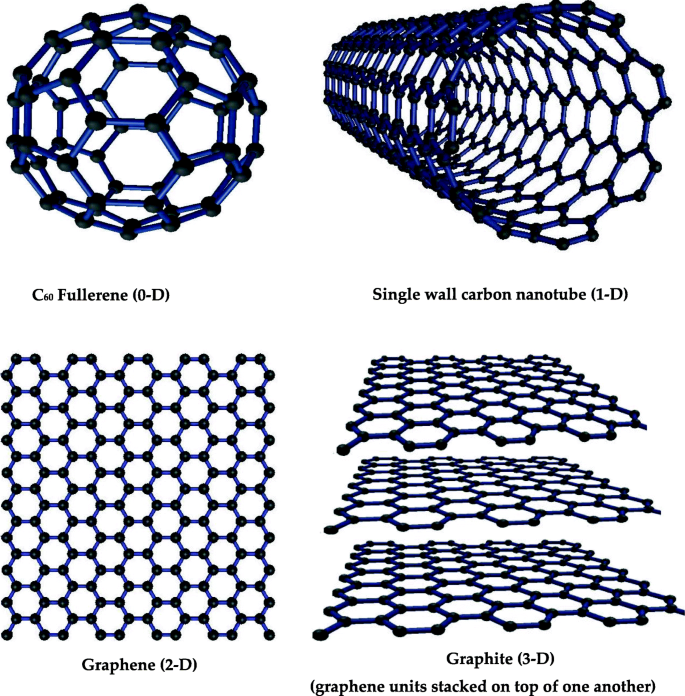
Примеры углеродных наноматериалов разных размеров
Применение фуллеренов для восстановления окружающей среды и очистки воды
Фуллерены были открыты в 1985 году из межзвездной пыли, и они имеют пятиугольную и шестиугольную кольцевую структуру с замкнутой клеткой, представленную формулой C 20 + m где м является целым числом [49]. Они обладают гидрофобным характером, высоким сродством к электрону и высоким отношением поверхности к объему, а также поверхностными дефектами. Эти уникальные физико-химические свойства делают их идеальным материалом для различных приложений, таких как полупроводники, электроника, биомедицины, солнечные элементы, сенсоры, косметика, искусственный фотосинтез и поверхностные покрытия [50,51,52]. Brunet et al. показали, что гидрофильные функционализированные фуллерены (C 60 ) также применялись для уничтожения патогенных микроорганизмов в воде с помощью фотокаталитического процесса. Фуллерены также являются идеальными экологически чистыми материалами для хранения водорода, поскольку молекулы фуллерена могут быть легко преобразованы в связи C – C в C – H из-за более низких энергий связи углерода и водорода [27]. Сообщалось, что фуллерены обладают максимальным запасом водорода 6,1% из-за их химического состава и клеточной молекулярной структуры, а структуру фуллерена можно легко изменить обратно из-за более высоких энергий связи C – C [3, 53, 54]. На поверхность электродов суперконденсаторов нанесены проводящие слои углерода, и их емкость зависит от площади поверхности, распределения пор по размерам и электропроводности [55, 56]. Наноматериалы на основе углерода обеспечивают более высокую электропроводность, чем доступные традиционные материалы, из-за большей площади поверхности [57]. Сообщается, что композитные материалы на основе фуллерена показывают более высокую удельную емкость 135,36 Фг - 1 . чем чистый графеновый материал, не гибридизованный с фуллереном. В дополнение к этому, композит на основе фуллерена показал лучшее время удерживания - 92,35% даже после 1000 циклов заряда / разряда [58]. Фуллерены также используются в литий-ионных батареях в качестве анодов и обеспечивают лучшую эффективность при замене неразлагаемых металлических анодов, что доказывает их эффективность с точки зрения эффективности и экологически чистый материал. Физико-химические свойства фуллеренов также делают их подходящими кандидатами для экстракции различных частиц из водных сред [59, 60]. Пикеринг и др. разработал водорастворимые соединения фуллерена и успешно применил их в качестве сенсибилизатора для образования активных форм кислорода (АФК) в воде при облучении видимым и ультрафиолетовым излучением. АФК могут фотодеструктировать органические загрязнители в воде, и в дополнение к этому водорастворимые фуллерены (фуллеролы) также действуют как антиоксиданты. Что наиболее важно, фуллеролы можно легко удалить из воды после выполнения функции фотодеградации [53].
Считается, что фуллерены адсорбируют частицы за счет проникновения адсорбатов в промежутки / дефекты между углеродными нанокластерами, и, помимо дефектов, более низкая склонность к агрегации и большая площадь поверхности делают их полезными наноматериалами, которые можно применять для адсорбции ионов тяжелых металлов из вода [61, 62]. Алексеева и др. провели сравнительные исследования фуллерена и нанокомпозитно-полистирольной пленки для удаления Cu 2+ ионы; они обнаружили, что фуллерены показали лучшую эффективность [60]. Они также обнаружили, что фуллерены следуют модели адсорбции Ленгмюра для Cu 2+ ионы [60]. Они установили, что Cu 2+ в первом случае эффективность удаления фуллеренов выше, и равновесная изотерма Cu 2+ адсорбция на фуллерене соответствует модели Ленгмюра. Хотя фуллерены имеют большой потенциал для адсорбции воды, их стоимость слишком высока, что ограничивает их использование. Однако небольшое количество фуллеренов может быть использовано для изготовления других материалов, таких как активированный уголь, лигнин и цеолиты, для повышения их эффективности адсорбции [63]. Производство фуллерена увеличивает гидрофобный характер, что делает материалы более пригодными для адсорбции, а также помогает облегчить переработку [64]. Сообщается, что антибактериальный материал образуется путем прививки фуллерена C 60 с поливинилпирролидоном (ПВП), который может применяться при дезинфекции воды. Все больше внимания уделяется мембранным технологиям в очистке воды от солей, органических веществ, частиц и газов. Характеристики мембраны зависят от состава материала, так как он отвечает за реакционную способность, селективность и механическую прочность. Фуллерены имеют большой потенциал для применения в мембранной технологии из-за их простоты функционализации, высокого сродства к электронам, большой прочности, способности изменять размер и т. Д. Фуллерены могут быть полезны при прививке наноадсорбентов для повышения их адсорбционной эффективности.>
Биосовместимость фуллеренов
Наноматериалы на основе фуллерена используются в биомедицинских целях, и различные исследования показали их биосовместимость с живыми организмами. Он использовался как биорецептор, а также как биосенсор, а также в биомедицинской инженерии, и сообщалось, что он биосовместим с живыми системами [65,66,67,68,69]. Фуллерен - нетоксичный материал, который можно использовать для фильтрации, адсорбентов и мембранных материалов для окружающей среды и очистки воды.
Углеродные нанотрубки (УНТ)
Углеродные нанотрубки были открыты Лидзимой в 1999 году, и они могут быть одностенными (ОСУНТ), например, слоистым свернутым графеном, или многослойными углеродными нанотрубками (МУНТ), например, многослойным свернутым графеном [70]. УНТ были в центре внимания нанотехнологических исследований с момента их открытия из-за их уникальных физико-химических свойств. Эти цилиндрические наноструктуры аллотропов углерода применяются в электронике, полупроводниках, автоэлектронной эмиссии, накоплении энергии, катализе, биомедицине, воздушных и водных фильтрах и т. Д. Их диаметр может составлять от 1 нм до нескольких нанометров с большой удельной площадью поверхности (150–150 нм). 1500 м 2 / г), и они обладают мезопорами, что делает их идеальным кандидатом для удаления ионов тяжелых металлов путем адсорбции [71, 72]. В дополнение к этому, УНТ могут быть легко функционализированы различными органическими молекулами, что может сделать их специфичными для выбора адсорбатов, а их адсорбционная способность может быть улучшена [73]. Механизм сорбции тяжелых металлов УНТ зависит от свойств поверхности, электрохимического потенциала и процесса ионного обмена [11, 73].
Экологическое применение УНТ / экологичных технологий на основе УНТ
Мировой спрос на энергию стремительно растет, и прилагаются большие усилия для разработки простого, экономичного и экологически чистого материала для надежных технологий получения энергоресурсных материалов. Солнечная энергия производится путем преобразования солнечной энергии и солнечного теплового преобразования [74]. Однако основным препятствием является низкая эффективность преобразования тепла в солнечных коллекторах.
Наножидкости углерода широко применяются в солнечной тепловой конверсии из-за их хороших характеристик в качестве поглотителей солнечной энергии [75]. Фотоэлектрические элементы на основе углеродных нанотрубок привлекли большое внимание ученых, поскольку они могут быть полупроводниками p-типа с превосходной подвижностью, а их сочетание с донорами электронов является новой и уникальной идеей [76, 77]. Органические фотоэлектрические устройства могут быть легко сконструированы путем изготовления УНТ из полимеров [78]. Солнечные элементы на основе гетероперехода CNT-Si (p-n) были разработаны, что привело к получению превосходных проводящих и прозрачных пленок. В дополнение к этому, УНТ с арсенидом галлия n-типа (n-GaAs) также описаны с лучшей эффективностью 3,8% для зеленого лазера и настольной лампы [79]. УНТ также широко используются в качестве накопителей энергии, работающих на принципах электрохимических двухслойных конденсаторов (EDLC), таких как ультраконденсаторы [80]. Включение УНТ в электроды ультраконденсаторов привело к значительному увеличению срока службы, превышающего 300 000 циклов [81]. В дополнение к этому, суперконденсаторные УНТ также используются в диодах вместо обычных транзисторов, поскольку они могут создавать идеальные p-n-переходы благодаря своим превосходным механическим и электрическим свойствам [58]. УНТ также широко используются в передовых сенсорных технологиях, поскольку они могут улучшить чувствительность, селективность, время отклика, рентабельность и срок службы химических и биосенсоров [90]. Эти результаты позволяют предположить, что лучшие УНТ являются идеальными материалами с превосходной подвижностью и большей эффективностью без негативного воздействия на окружающую среду, что является основным недостатком наиболее часто применяемых материалов p-типа на металлической основе.
Применение УНТ в фотокатализе
Фотокатализ - одна из передовых технологий, применяемых для очистки сточных вод с использованием полупроводников [82]. Применяются самые разные полупроводниковые материалы, а именно Fe 3 . О 4 , ZnO и TiO 2 ; однако квантовая эффективность этих материалов невысока, и в дополнение к этому их ультрафиолетовый фотоотклик также медленный [83]. УНТ являются перспективными передовыми материалами для катализа из-за их улучшенной квантовой эффективности, наноразмеров, высокой химической стабильности, полой трубчатой структуры и расширенной области адсорбции света из-за их большой удельной поверхности [84]. Gao et al. разработаны сверхтонкие сетевые фотокатализаторы на основе ОСНЦ-TiO 2 и успешно применяется для очистки воды от нефти [85]. Park et al. декорировал оксид титана на аэрогеле ОСУНТ и успешно применялся для удаления метиленового синего из воды [86]. Zhao et al. изготовленные MWCNTs-TiO 2 и применен для фотодеградации метиленового синего [87]. Xu et al. разработанные фотокатализаторы на основе комбинации гидрокси-MWCNTs и PbO 2 нанокристаллический анод и успешно применил его для удаления пиридина из воды [88].
ОСУНТ в очистке воды, загрязненной тяжелыми металлами
ОУНТ представляют собой одномерные (1-D) углеродные наноматериалы, состоящие из полой трубки со стенками толщиной в один атом. Этот одномерный материал демонстрирует исключительные физико-химические свойства благодаря своей уникальной структуре. ОСУНТ широко применяются в различных областях, таких как полупроводники, электроника, биомедицины, химия и биосенсоры [44, 89, 90, 91, 92, 93]. ОСУНТ также широко используются для борьбы с загрязнением окружающей среды из-за их пористой структуры, большой площади поверхности, более легкой функционализации поверхности и наноразмеров. Эти свойства ОУНТ очень перспективны для применения в водоподготовке. Алиджани и др. разработали нанокомпозит на основе ОСУНТ, изготовив его из сульфида кобальта магнетита, и полученные нанокомпозиты были применены для удаления ртути; результаты показали высокую адсорбцию более 99,56% за более короткий период - 7 мин [94]. Для сравнения:одни только ОУНТ адсорбируют 45,39% ртути [94]. Anitha et al. провели молекулярно-динамическое моделирование голых ОСНТ и их функционализированных аналогов, например, ОСУНТ-OH, ОСУНТ-NH 2 , и ОСУНТ-СООН для адсорбционной способности ионов тяжелых металлов, например, Cd 2+ , Cu 2+ , Pb 2+ , и Hg 2+ из водных сред. Результаты показали, что ОСУНТ-COOH имеют намного большую адсорбционную способность, примерно на 150–230% выше, чем у ОСУНТ без покрытия. Было обнаружено, что ОУНТ-ОН и ОУНТ-NH обладают слабой адсорбцией, поскольку они просто показали на 10–47% более высокую адсорбцию по сравнению с ОУНТ [95]. ОУНТ-COOH также сообщалось об адсорбции Pb 2+ , Cu 2+ , и Cd 2+ ионы с адсорбционной емкостью 96,02, 77,00 и 55,89 мг / г соответственно. По сравнению с этим было обнаружено, что нефункционализированные ОУНТ адсорбируют 33,55, 24,29 и 24,07 мг / г для Pb 2+, Cu 2+ , и Cd 2+ ионы соответственно [96]. Зазули и др. разработали нанокомпозиты SWCNT, функционализировав их l-цистеином. Они применили разработанные нанокомпозиты для удаления ртути из воды. Эффективность адсорбции разработанного ОУНТ-цистеина составила 95% [97]. Гупта и др. разработана мембрана на основе нанокомпозита ОСУНТ-полисульфон и применяется для удаления тяжелых металлов. Включение SWCNT привело к уменьшению размера пор мембраны и более гладкой поверхности. Было обнаружено, что разработанная мембрана демонстрирует высокую способность задерживать ионы металлов и удаляет 96,8% Cr + 6 . , 87,6% как + 3 , и 94,2% Pb + 2 ионы. Мембрана без ОСУНТ показала только 30,3%, 28,5% и 28,3% отторжения Cr + 6 . , Как + 3 , и Pb + 2 ионы соответственно. Эти результаты показывают повышение эффективности мембраны за счет включения ОСУНТ [98]. Дехгани и др. применил SWCNT для удаления Cr + 6 ионов из воды и оценили влияние различных параметров, например, времени контакта, начального pH и начального Cr + 6 концентрация ионов от адсорбционной емкости. Было замечено, что эффективность адсорбции зависит от pH, максимальная эффективность была обнаружена при pH 2,5, а адсорбция следует модели изотермы Ленгмюра [99]. Эти исследования показали, что одностенные углеродные нанотрубки подходят для очистки воды, загрязненной тяжелыми металлами.
МУНТ в очистке воды, загрязненной тяжелыми металлами
Углеродные нанотрубки, имеющие несколько свернутых слоев графена, называются многослойными углеродными нанотрубками (MWCNT), как показано на рис. 4. MWCNT демонстрируют уникальные свойства, такие как большая площадь поверхности, высокая электрическая проводимость, теплопроводность и высокая прочность на разрыв [100]. Благодаря этим физико-химическим свойствам они широко применяются в электронике, солнечных элементах, сенсорах и биомедицинских науках [101,102,103]. МУНТ также широко применялись при очистке воды, и особенно ионы тяжелых металлов адсорбируются за счет химического взаимодействия с функциональными группами МУНТ. Сообщалось, что окисленные MWCNT обладают высокой адсорбционной способностью и эффективностью для Cr 6+ , Pb 2+ , и Cd 2+ ионы из воды [104, 105]. Адсорбция ионов металлов также зависит от значения pH, и это свойство можно применять для десорбции ионов путем изменения pH, а MWCNT можно использовать повторно. Некоторые исследования показали, что MWCNT, окисленные плазмой, обладают лучшими адсорбционными свойствами, чем химически окисленные; это можно приписать большему количеству кислородсодержащих функциональных групп, присутствующих на поверхности углеродных нанотрубок. Кроме того, сообщалось, что окисленные плазмой MWCNT могут быть легко переработаны и использованы повторно [72, 106].
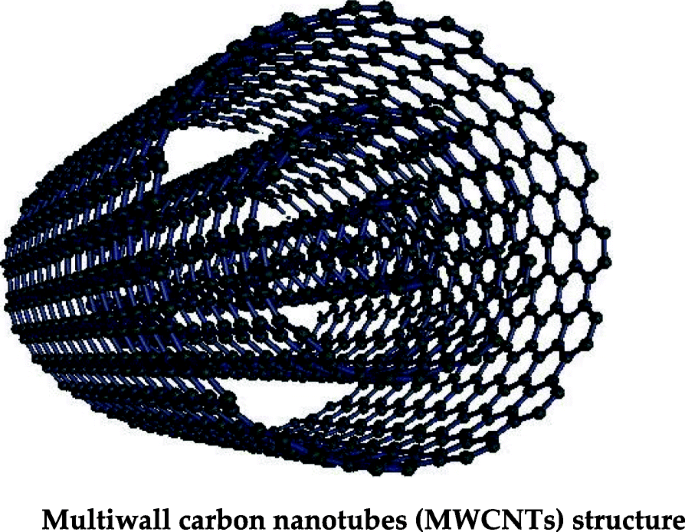
Структура многослойных углеродных нанотрубок (MWCNT)
Композиционный материал MWCNT также использовался для адсорбции ионов тяжелых металлов из воды. МУНЦ-Fe 2 О 3 , МУНЦ-ZrO 2 , МУНЦ-Fe 3 О 4 , МУНЦ-Al 2 О 3 , и МУНЦ-MnO 2 -Fe 2 О 3 нанокомпозиты успешно применяются для удаления тяжелых ионов Cr 6+ , Как 3+ , Ni 2+ , Pb 2+ , и Cu 2+ ионы из воды [107,108,109,110]. Условия экспериментов в растворах, включая pH и концентрацию ионов металлов, могут влиять на адсорбционные характеристики МУНТ, и модель адсорбции Фрейндлиха удовлетворяет их экспериментальные данные [81, 111]. Эффективность адсорбции функционализированных МУНТ увеличилась по сравнению с другими материалами из органических оксидов, а также предсказано, что функционализированные МУНТ в 20 раз более эффективны в адсорбции ионов металлов, чем неокисленные МУНТ [112]. Принято считать, что основным механизмом сорбции являются связи ионов и наличие полярной поверхности углеродных нанотрубок [113, 114]. Окисленные MWCNT также показали исключительно высокую сорбционную способность и эффективность для Pb 2+ . , CD 2+ , и Cr 6+ из воды. Сорбционная эффективность МУНТ при кислотной обработке увеличивает возможность удаления ионов свинца, хрома и кадмия с кислородной функциональной группой, образуя комплексы ионов или осаждения солей на поверхности [115]. Адсорбция MWCNT, обработанных концентрированной HNO 3 increases significantly mainly due to oxygen functional groups created on the surface of acidified nanotubes that can react with metal ions to form complex or salt precipitates on the surface. The MWCNT composites with certain compounds like iron (III) oxide, zinc oxide, and aluminum oxide are formed by a coprecipitation method, and resulting composites are successfully applied for the removal of chromium, nickel, lead, copper, and arsenic ions. The adsorption efficiency of these nanocomposites was found to be dependent on the pH value and temperature, and the sorption process can be accomplished by changing these parameters [116, 117]. Depending on the pH and temperature, the sorption capacity of these composites varied from 10 to 31 mg/g. The adsorption process for these nanocomposites was well described by the Langmuir model [118]. The nanocomposites of oxidized multiwalled MWCNTs with manganese oxide/iron (III) oxide are reported to remove Cr 6+ ions with maximum adsorption capacity of 186.9 mg/g with the maximum removal capacity of 85% at the optimum pH 2.1 studies. Their promising adsorption was due to the surface polarity of the adsorbents. It has also been reported that plasma-oxidized MWCNTs are better in adsorption compared to chemically oxidized ones as the prior ones have more oxygenated functional groups [119]. Plasma-oxidized technique has also been reported for the formation of nanotubes with titanium oxide and manganese dioxide and utilized for the removal of lead ions from water. The results showed that these hybrid systems can act as an effective adsorbent for the lead ions in the first case; the adsorption capacity was 137 mg/g, and in the second case, it was 78.74 mg/g [120]. In a heterogeneity adsorbent surface, sites combined twice are fitted in the isotherms models of the Langmuir-Freundlich equation that was used to differentiate between two types of adsorption sites with greater and lesser energy affinities for the Ni 2+ ions [121]. It is believed that nickel ion sorption mainly occurs at the sites of energy with modified nanocomposites of MWCNTs and the nano-modification leads to a 20% increase in the adsorption capacity at small (up to 0.1 mol/l) equilibrium adsorbate concentrations. Another modification reported for MWCNTs is their functionalization with hydroxyquinoline and their application for the removal of copper, lead, cadmium, and other toxic ions [122]. The carbon nanotubes alone as well as in their oxidized and in their composite forms have tremendous ability to adsorb the heavy metal ions, and a lot of research is in progress for their applications in purification of water. Elsehly et al. applied commercial MWCNTs for the removal of the manganese and iron which could reach 71.5% and 52% respectively with a concentration in aqueous solution of 50 ppm of these metal ions [123]. In another study, CNT-based nanocomposites have been applied for the removal iron and manganese from the water [124].
Biocompatibility of CNTs
Carbon nanotubes have great potential to be applied for multidisciplinary fields like drug delivery, diagnosis, biosensors, electronics, semiconductors, and environmental remediations [125]. Different studies revealed the biocompatibility of CNTs as it has been widely exploited for biomedical applications [126, 127]. Carbon-based materials like CNTs are safe to be applied for the environmental remediation and in particularly for water treatment.
Graphene Based Material for Environmental Remediation
Graphene-based material for the adsorption of gaseous contaminants
Carbon dioxide (CO2 ) has been the environmental concern because of its immense effect in global warming [128]. Nanomaterials have been found to be promising materials as compared to conventional materials both with respect to cost and efficiency [129]. Graphene-based materials have been utilized for the adsorption of gaseous contaminants [130]. Gosh et al. showed the successful application of graphene-based nanomaterials for the capture of CO2 и H 2 . A single layer of graphene has been reported to capture 37.93% of CO2 [130]. Graphene has been reported to selectively adsorb CO2 as compared to methane (CH4 ) and nitrogen (N2 ) gases. Selectivity of graphene oxide (GO) for CO2 can be attributed to higher dipole moment of carbon dioxide which can easily interact with polar oxygenated functional groups of CO2 [74, 131]. Other studies have also been reported for tuning the graphene chemistry for the improved selectivity of the desired gaseous contaminant [75, 131].
Graphene Oxide in Removal of Organic Dyes from Water
Graphene-based nano-adsorbents are excellent advanced materials for the removal of the organic contaminants from the water because of their nano-scaled size, high surface area, ability to interact via pi-pi stacking, hydrogen bonding, and electrostatic interactions [26]. In comparative adsorption studies of GO and graphite using methylene blue and malachite green as standard organic dyes, it was found that GO showed much better adsorption than graphite [26]. GO has also been utilized for the removal of cationic dyes namely methylene blue (MB), crystal violet (CV), and rhodamine B (RhB) from water. It was found that the higher the initial dye concentration, the higher will be the adsorption with adsorption capacities of 199.2, 195.4, and 154.8 mg g −1 for MB, CV, and RhB, respectively [76]. GO has also successfully applied for the removal of anionic dyes like Acid Orange 8 (AO8) and Direct Red 23 (DR23) from aqueous solutions [77].
Graphene-Based Photocatalytic Materials for Water Decontamination
Although adsorption can remove the contaminant from water, the adsorption technique is unable to destroy/degrade the contaminants and disposal step is required [77]. Photocatalysis is a useful approach for water remediation/wastewater treatment for the complete degradation and mineralization of organic/biological contaminants [78]. Graphene-based photocatalysts have been reported for their improved activity because of their high surface area, nanosize, and more electronic movements as compared to the traditionally used materials [78, 132]. Rommozzi et al. designed reduced graphene oxide (rGO) with a greener reduction method using glucose and ammonium hydroxide and successfully designed a photocatalyst which is visible by the fabrication with TiO2 . The designed rGO-TiO2 photocatalyst was successfully applied for the refractory dye named Alizarin Red S (ARS) [133]. In other studies, graphene oxide fabricated with TiO2 and ZnO exhibited much photodegradation of methylene blue as compared to TiO2 /ZnO alone [79, 80].
Graphene and Graphene Oxide-Based Adsorbents for the Purification of Heavy Metal-Contaminated Water
Graphene is one-atom-thick-layered hexagonal lattice of carbon atoms and is known as the thinnest material with the strength of 200 times than steel. Graphene was discovered in 2004 by Sir Andre Geim and Sir Konstantin Novoselov, who were awarded a Nobel prize for their discovery in 2010. Graphene (2-D) is being used widely in almost every field such as in touch screens, mobiles, LCDs, semiconductors, computer chips, batteries, energy generation, water filters, supercapacitors, solar cells, and biomedical and environmental sciences [134,135,136,137]. These 2-D graphene-based materials are getting more and more attention in water treatment due to their unique physicochemical characteristics namely electronic properties, high surface area, thermal mobility, high mechanical strength, and tunable surface chemistry [118, 134, 138, 139]. Tabish et al. designed porous graphene and applied it as an adsorbent for the removal of heavy metal ions as well as other pollutants from water. They applied this porous graphene material for As 3+ removal from water and found 80% efficiency. The material was found to retain its water treatment properties after regeneration and recycling [138]. Guo et al. designed a nanocomposite of partially reduced graphene oxide by its fabrication with Fe3 О 4 via in situ co-precipitation method and applied it for the removal of Pb 2+ ions from water. The designed nanocomposite was found to be excellent in removing the Pb 2+ ions from aqueous solution with an adsorption capacity of 373.14 mg/g [140]. Zhang et al. functionalized the reduced graphene oxide with 4-sulfophenylazo (rGOs) and applied it for the removal of a variety of heavy metal ions from aqueous solution. The designed material showed the maximum adsorption capacity of 689, 59, 66, 267, and 191 mg/g for the Pb 2+ , Cu 2+ , Ni 2+ , CD 2+ , and Cr 3+ respectively [141]. Diana et al. designed a graphene-based self-propelled microbot system whose structure was made up of nanosized multilayered consisting of graphene oxide, nickel, and platinum. Each layer performed a different function, e.g., graphene oxide captures the heavy metal Pb 2+ ions, the middle layer of Ni enables the control of microbots with the help of external magnetic field, and the inner layer of platinum helps the engine in self-propelling [142]. The designed system was found to remove the 80% of the Pb 2+ water solution. Figure 5 shows the schematic illustration of the working principle of microbots. Ян и др. designed hydrogen beads using graphene oxide and sodium alginate (GO-SA) and successfully applied them for the removal of Mn 2+ ions from the aqueous solution with excellent adsorption capacity of 56.49 mg/g [9]. Zheng et al. designed nanocomposites by fabrication of zinc oxide with tea polyphenol with reduced graphene oxide (TPG-ZnO). Designed material was applied for the removal of heavy metal ions with an added advantage of antibacterial properties [143]. They applied this material for the removal of Pb 2+ ions from aqueous solution with adsorption efficiency of 98.9%, and the adsorbent was found to possess antibacterial properties against Streptococcus mutans with 99% eradication [143]. Mousavi et al. designed nanocomposites of graphene oxide with iron oxide magnetite nanoparticles Fe3 О 4 and applied them for the removal of Pb 2+ ions from water and the material showed 98% removal efficiency with a capacity of 126.6 mg/g [144]. Considering functionalized graphene as an adsorbent to remove Pb 2+ ions from an aqueous medium, the highest record of Pb 2+ ion removal over graphene is 406.6 mg/g at pH of 5.0 in 40 min [145]. Graphene-hydrogel lingo sulfonate functionalized nanocomposites having oxygenated functional groups making the surface highly polar reported to increase the rate of adsorption of Pb 2+ ions with maximum efficacy of 1308 mg/g with the equilibrium reached in 40 min. Awad et al. modified graphene oxide with chloroacetic acid (GO-COOH) and ethylenediamine (GO-amino). The designed systems were applied for the removal of mercury (Hg 2+ ) from water and found that the nanocomposites (GO-COOH) and (GO-amino) have an adsorption capacity of 122 mg/g and 230 mg/g. In addition to this, designed systems retained their adsorption efficiency after the recycling process [146]. Ян и др. designed magnet graphene oxide for the rapid removal and separation of Fe (II) and Mn (II) from micropolluted water [147]. Ali et al. designed graphene-based adsorbent successfully for the removal of noxious pollutants namely Cu (II), Pb (II), Fe (II), and Mn (II) [148].
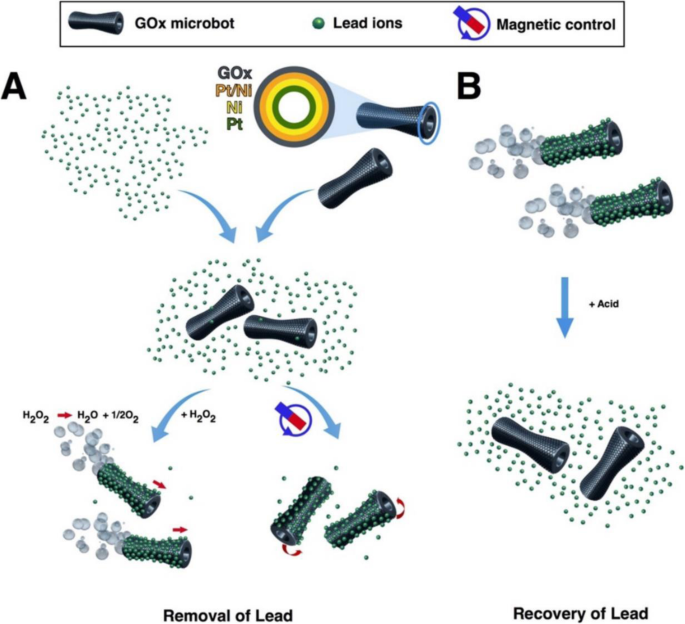
Scheme of GOx-microbot-based approach for lead decontamination and recovery. а Decontamination of polluted water using GOx-microbots fabricated by electrodeposition of nanolayers of graphene oxide (GOx), Pt/Ni layer, Ni magnetic layer, and Pt catalytic inner layer. The decontamination strategy for lead ions can be carried out by two different techniques:self-propulsion of the GOx-microbots in the presence of H2 О 2 or by using an external rotating magnetic field. б Recovery of lead ions from the GOx-microbots in the presence of acidic media [117]
Biocompatibility of Graphene-Based Nanomaterial
Graphene-based nanomaterials have been applied in different fields like electronics, chemical sensors, biosensors, drug delivery, theragnostic, and other related biomedical fields. These studies also report the cytocompatibility of graphene-based materials both by in vitro as well as in vivo animal studies [122, 133, 149,150,151,152]. These findings suggest that the graphene-based materials are safe for the environmental remediation application as they are just used for the removal and degradation of pollutants and are not consumed by humans directly.
Activated Carbon in Environmental Remediation
Activated carbon is a fabulous material because of its high surface area, highly porous structure, and ease of preparation with variety of starting materials. Because of its ideal physicochemical properties, it has wide application in environmental remediations in different industries like pharmaceutics, fertilizer plants, petroleum, cosmetics, automobiles, and textiles [153] It is also widely applied for the adsorption of gases, solvent recovery, and wastewater treatment especially for the removal of organic dyes/other pollutants; not only this, but it is also used as a catalyst in biodiesel production. It is also applied as a low-cost material for the treatment and removal of water containing COD, BOD, and TSS and stabilizing and maintaining the optimum pH for biological uses [154,155,156]. Maguana et al. prepared activated carbon from the pear seed cake and successfully applied it for the removal of methylene having an adsorption capacity of 260 mg/g [157]. Antonio et al. prepared activated carbon from the kenaf plant and applied it successfully for the treatment of the wastewater of hospitals containing paracetamol as the main pollutant [158]. The above literature suggests that the activated carbon is the pretty useful economical material which can easily be prepared and it has immense application in environmental remediations.
Activated Carbon as Adsorbents in the Purification of Heavy Metal-Contaminated Water
Activated carbon (AC) is also known as activated charcoal, and this of type carbon material is formed under some treatment protocols resulting in micro/nanopores and having the large surface area of more than 3000 m 2 [159]. The AC is produced on a large scale from coal, wood, and agricultural wastes [160]. In addition to its porous nature (as shown in Fig. 6), AC also has a high mechanical strength which enables its applications in catalyst support, capacitors, electrodes, and gas storage and most importantly used as the adsorbent for removal of metal ions, organic wastes, and gases from water [160,161,162]. The high mechanical strength of activated carbon enables its periodic cleaning, regeneration, and reutilization [160]. Abeer et al. reported the preparation of AC from apricot stone and its application in removal of Zn + 2 and Al + 3 ions with removal efficiency of 92% [163]. Ebrahim et al. designed AC from sewage sludge, applied it for the removal of Cu + 2 ions from water, and found that the designed material showed maximum adsorption capacity of above 50% [164].
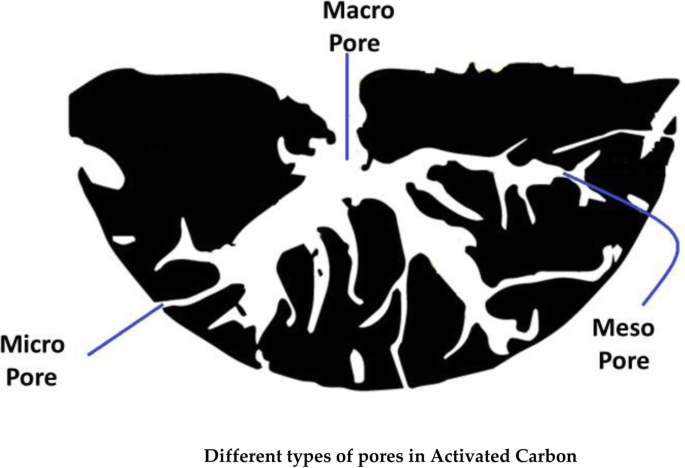
Different types of pores in activated carbon
Ли и др. prepared the AC from sewage sludge produced from the wastewater treatment plant and functionalized it with sulfur [165]. They applied sulfonated AC for the removal of Pb 2+ , CD 2+ , Cu 2+ , и Ni 2+ ions from water. The adsorption capacity of metal ions were found to be 238.1 mg/g, 96.2 mg/g, 87.7 mg/g, and 52.4 mg/g for Pb 2+ , CD 2+ , Cu 2+ , и Ni 2+ respectively [165]. Cao et al. designed multipore activated carbon (MPAC) with a large surface area using the agricultural waste of long-root Eichhornia crassipes and applied it for removing heavy metal ions, e.g., Pb 2+ , CD 2+ , Cu 2+ , Ni 2+ , и Zn 2+ . They found that at 30 °C adsorption capacity being 1.34 mmol/g, 1.07 mmol/g, 1.22 mmol/g, 0.97 mmol/g, and 0.93 mmol/g for Pb 2+ , CD 2+ , Cu 2+ , и Ni 2+ respectively [166]. Dong et al. investigated the application of spent activated carbon (AC) for heavy metal ion removal from water and found high adsorption capacity of 95% and 86% for Pb 2+ and Cd 2+ ions respectively [167]. M. Bali et al. [168] applied commercial AC for the removal of heavy metal ions and found that adsorption equilibrium of Cd 2+ ion took 15 min while for Pb 2+ , Zn 2+ , and Cu 2+ it took 45 min with percentage removal of 64% for all these ions and with Cd 2+ being the highest [10]. Kongsuwan et al. prepared the activated carbon from the agricultural waste of eucalyptus bark. They applied it for the removal of Cu 2+ и Pb 2+ from water with maximum removal capacity of 0.45 and 0.53 mmol per gram of AC respectively, with adsorption being the main mechanism of ion uptake [169]. AC poultry litter has also been reported and applied for the treatment of heavy metal-contaminated water and found that for 1 kg of poultry litter AC adsorbs 404 mmol, 945 mmol, 236 mmol, and 250–300 mmol of Cu 2+ , Pb 2+, Zn 2+ , and Cd 2+ ions respectively [170]. This adsorption is significantly higher than the commercially available AC derived from coconut and bituminous. The AC of wood saw dust of rubber plant has also been reported for the removal of heavy metal ions of Cr + 6 from water with adsorption capacity of 44 mg/g [171]. AC formed from Moso and Ma bamboo was found to be highly efficient in removing the heavy metal ions, i.e., Pb 2+, Cu 2+ , Cr 3+ , and Cd 2+ with the maximum adsorption capacity of more than 90% removal [172]. Naser et al. prepared AC from rice husk and applied them for the removal of Cu 2+ from aqueous solution, and maximum capacity was found to be 33.92%. Similar results have also been reported for the removal of Cu 2+ from the AC formed from Palm shell [173]. AC of love stones has been reported for the adsorption of Cd + 2 and Ni + 2 with adsorption capacity of 1.85 mg/g and 0.67 mg/g respectively in two different studies [174, 175]. AC prepared from olive stone using the microwave method has been applied for the removal of Fe 2+, Pb 2+, Cu 2+, Zn 2+, Ni 2+ , and Cd 2+. from wastewater. Another study reported on the olive stone AC prepared via microwave to remove a group of metal ions from synthetic wastewater:Fe 2+ , Pb 2+ , Cu 2+, Zn 2+ , Ni 2+ , and Cd 2+ with removal efficiency of more than 98% [176]. Tamarind wood AC has been reported for the highest adsorption capacity of above 97% for Pb 2+ from water [177]. Activated carbon has been applied as an adsorbent for the removal of Fe (II) and Mn (II) with great efficiency [178, 179]. The activated carbon is easy to synthesize, is cheaper, and is the most promising material for the adsorption of heavy metal ions and can be prepared at a large scale from a variety of carbon sources especially form agricultural waste. In addition to easier preparation, AC can easily be functionalized. Table 2 summarizes the effect of different parameters on the process of metal ion adsorption.
Biocompatibility of the Activated Carbon
Different studies have been conducted for the biocompatibility evaluation of the activated carbon materials prepared form different carbon sources. Activated carbon has been applied for the treatment of cystitis and was found to be effective and nontoxic compared to the antibiotics being applied [180]. Biocompatibility of activated carbon can be attributed to its inertness, and it has also been functionalized and fabricated with other materials to confer on the disinfection properties [181]. The activated carbon is also given orally to human beings as a sorbent for the removal of toxins from the human body and has also been utilized in biomedical applications [182, 183]. These studies strongly suggest the biocompatibility of the activated carbon.
Заключение
In this review, environmental and special purification of heavy metal from heavy metal contaminants by the applications of carbon nanomaterials, namely fullerene carbon nanotubes, graphene, graphene oxide, and activated carbon discussed. These carbon nanomaterials have been utilized in the purification of heavy metal-contaminated water with great success. The reason behind the successful application is due to their fascinating properties like high surface area, ease of recycling, and easiness to desorb the adsorbed metal ions; only using mineral acid solution and regenerated material can be reused with retention of adsorption capability. In addition to these properties, the carbon nanomaterials can easily be fabricated with other nanomaterials and are easy to be functionalized resulting in multifunctional nano-adsorbent. Carbon-based materials are highly biocompatible with living organisms and environment. There is also an immense effect of different parameters such as pH, contact time, and type of adsorbents on the process of metal ion adsorption. Based on this literature review, it can be concluded that carbon nanomaterials have fascinating physicochemical properties and have great potential to be exploited in the environmental remediation and water purification.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- AC:
-
Activated carbon
- GO:
-
Оксид графена
- MWCNT:
-
Multiwall carbon nanotubes
- r-GO:
-
Восстановленный оксид графена
- SWCNTs:
-
Single-wall carbon nanotubes
Наноматериалы
- Идеальная формула для согласования операций и обслуживания
- Плюсы и минусы колец из углеродного волокна
- Разница между углеродным волокном и стекловолокном
- Материалы:полипропилен, армированный стеклом и углеродным волокном, для автомобилей
- Пять основных проблем и проблем для 5G
- Достижения и проблемы флуоресцентных наноматериалов для синтеза и биомедицинских приложений
- Понимание концепции IoT в очистке и управлении сточными водами
- Лунный фонарик для поиска воды на Луне
- Подходящая установка для правильной конфигурации
- Важность эффективной термообработки пуансонов, штампов, лезвий и инструментальных сталей



