Активность ультратонких Pd-нанозимов, имитирующая пероксидазу, активируемую горячими электронами
Аннотация
Активируемые светом нанозимы могут открыть множество новых возможностей для химической промышленности и биотехнологии. Однако существующие каталитические системы с дистанционным управлением все еще далеки от удовлетворительных результатов. Здесь мы представляем интересный пример применения ультратонких нанолистов Pd (Pd NSs) в качестве имитатора пероксидазы, управляемого светом. Поскольку большая часть атомов Pd экспонирована на их поверхности, НС Pd толщиной 1.1 нм обладают высокой пероксидазоподобной активностью. Что еще более важно, при световом возбуждении такая внутренняя активность может быть дополнительно активирована почти в 2,4–3,2 раза. Такое явление можно приписать уникальному оптическому свойству ультратонких НЗ Pd, которые могут эффективно захватывать фотоны для генерации горячих электронов за счет эффекта поверхностного плазмонного резонанса и, таким образом, способствовать разложению H 2 in situ. О 2 в радикалы активных форм кислорода (O *). Этот усиленный катализ также можно использовать для высокочувствительного колориметрического обнаружения H2O2 в режиме реального времени. Мы надеемся, что наша работа может дать ценную информацию о рациональном дизайне искусственных нанозимов с контролируемой и эффективной деятельностью в биомедицинской диагностике, доставке лекарств и химии окружающей среды.
Введение
Природные ферменты - это прекрасные биокатализаторы, способные катализировать практически любое химическое преобразование жизни [1, 2]. Однако все же существуют врожденные дефекты, такие как низкая стабильность и высокая стоимость. Поскольку о наночастицах магнетита с присущей им активности пероксидазы впервые сообщалось [3], дизайн и разработка наноматериалов с ферментоподобной активностью (нанозимы) привлекают все большее внимание исследователей [4]. До сих пор ряд наноматериалов на основе оксидов [5,6,7], металлов [8,9,10] и углерода [11,12,13] использовался для имитации пероксидазы хрена (HRP). Среди них наноматериалы благородных металлов [8, 14,15,16,17,18,19], такие как серебро (Ag) [15], золото (Au) [16, 17], платина (Pt) [8], и палладий (Pd) [18, 19] и др., как сообщается, обладают высокой пероксидазной миметической активностью. С другой стороны, также сообщалось о введении света для активации активности нанозимов, что открывает множество возможностей для биотехнологии и химической промышленности [4, 20]. Однако существующие каталитические системы с дистанционным управлением все еще далеки от удовлетворительных результатов.
Плазмонные металлические наноматериалы могут улавливать солнечный свет или реагировать на него благодаря уникальному оптическому свойству поверхностного плазмонного резонанса (ППР). Эти металлические наноматериалы, которые могут захватывать фотоны для генерации горячих электронов за счет эффекта ППР, стали ключевыми материалами для улучшения каталитической скорости [21], продвижения нового оптического зондирования биомолекул [22], инженерной фототермической терапии и использования солнечного света в качестве возобновляемой энергии [ 23, 24]. Однако ни один из них не сосредоточился на эффекте SPR плазмонных нанозимов на основе металлов на их ферментативную активность. Таким образом, было бы привлекательно комбинировать нанозимы на основе плазмонных металлов с эффектом ППР для достижения высокоактивного и регулируемого светом ферментного катализа.
Здесь мы впервые сообщаем, что ультратонкие нанолисты Pd (Pd NS) толщиной около 1,1 нм могут служить отличным и управляемым светом имитатором пероксидазы. Сообщалось, что системы нанозимов на основе Pd и светорегулируемых нанозимов проявляют множественную ферментативную миметическую активность, включая оксидазу, пероксидазу, каталазу и супероксиддисмутазу [4, 18, 19]. Однако их структуры обычно представляют собой частицы, объемы и стержни. Как мы все знаем, ультратонкие НС Pd обладают высокой поверхностной энергией, малым латеральным размером и высокой подвижностью электронов, что приводит к высокой плотности активных поверхностных центров [25]. Кроме того, большинство атомов, экспонируемых на ультратонких нанолистах, могут служить идеальной платформой для разработки их характеристик [26]. Вдохновленные уникальной структурой ультратонких нанолистов, мы представляем стратегию, которая не только полностью использует активные центры атомов Pd, но также вводит горячие электроны в процесс ферментативного катализа. Как показано на схеме 1, взаимодействие фотонов со сверхтонкими НЗ Pd может вызвать резонанс поверхностного плазмона, который безызлучательно распадается на горячие электроны и дырки, тем самым способствуя образованию H 2 О 2 восстановительное разложение in situ с образованием радикалов кислородных форм (O *) с окислением ТМБ в видимой области спектра. Вводя видимый свет в ферментативную реакцию, НС Pd проявляют значительно более высокую каталитическую активность, чем НС Pd в темноте.
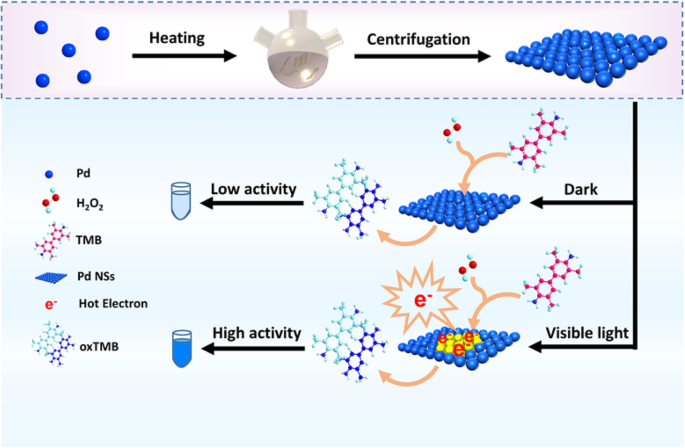
Схематическое изображение структуры НП Pd и изменения активности НП Pd в темноте и в видимом свете
Материалы и экспериментальные
Материалы и характеристики
Лимонная кислота (CA); N, N-диметилформамид (ДМФ); 3,3,5,5-тетраметилбензидин (TMB); и бромид цетилтриметиламмония (CTAB) были приобретены у Sigma Aldrich. Ацетилацетонат Pd (II), W (CO) 6 , и поливинилпирролидон (ПВП) были получены от Macklin. Перекись водорода (H 2 О 2 , 30 мас.%) Закуплен у Beijing Chemicals (Пекин, Китай). Все химические вещества использовались без дополнительной очистки. На протяжении всей работы использовалась экспериментальная вода, очищенная системой Millipore (18,2 МОм; Millipore Co., США).
Фазовые структуры продуктов были охарактеризованы на рентгеновском дифрактометре PANalytical с использованием излучения Cu Kα ( λ =1,5406 Å). И УФ-видимые спектры диффузного отражения (DRS) образцов были охарактеризованы при комнатной температуре с использованием Lambda 750, PerkinElmer. Концентрацию катализаторов в растворах определяли методом ICP-AES (720, Agilent). Изображения, полученные с помощью просвечивающей электронной микроскопии (ТЕМ), получали на просвечивающем электронном микроскопе JEM1400 plus, работающем при 100 кВ. Анализ ПЭМ высокого разрешения (ПЭМВР) был выполнен на полевом просвечивающем электронном микроскопе JEM-2100F (FE-TEM) при 200 кВ.
Синтез Pd-нанолистов
По заявленной методике [27] были синтезированы НС Pd. Вкратце, ацетилацетонат Pd (II) (16 мг), PVP (MW =24000, 30 мг), CA (150 мг) и CTAB (60 мг) смешивали в DMF (10 мл) и перемешивали в атмосфере азота в течение 1 час Когда цвет раствора в колбе (25 мл) изменится на однородный оранжево-красный раствор, 100 мг W (CO) 6 был добавлен в раствор под N 2 Атмосфера. Затем колбу нагревают при 80 ° С в течение 1 ч. После реакции темно-синий продукт отделяли центрифугированием (9000 об / мин, 3 мин) с достаточным количеством ацетона, а затем диспергировали в этаноле. Этот процесс повторялся трижды. Наконец, нанолисты Pd были диспергированы в 10 мл этанола для дальнейших экспериментов.
Фотокаталитическое измерение, имитирующее пероксидазу
Имитирующую пероксидазу активность нанозимов Pd NS оценивали путем измерения окисления TMB. Источником света служила лампа Xe мощностью 300 Вт (CEL-HXF300 / CEL-HXUV300, China education Au-light Co., Ltd., Пекин), а добавление стеклянного фильтра позволяет использовать видимый свет ( λ ≥ 400 нм), чтобы пройти. В типичном эксперименте 12,6 мкг мл -1 Нанозимы Pd NS (измеренные с помощью ICP-AES) добавляли к 1 мл буферного раствора фосфорной кислоты (0,1 М, pH 4), содержащего 50 мМ H 2 О 2 и 0,7 мМ TMB при комнатной температуре. В течение различного времени под облучением активность, имитирующую пероксидазу, определяли путем отслеживания характеристического пика поглощения при 652 нм после центрифугирования, который указывает концентрацию продуктов окисления TMB. В контрольном эксперименте были те же условия, за исключением освещения.
Результаты и обсуждение
Дизайн и характеристика нанозимов Pd NS
Типичный синтез палладиевых нанолистов был подготовлен с помощью классического метода (рис. 1a) для создания серии ультратонких нанозимов с высокоактивными атомными центрами, которые обладают присущими субстратам и фотонами захватывающими и эффективными характеристиками, имитирующими пероксидные ферменты. На рис. 1b – d показано типичное изображение, полученное с помощью просвечивающей электронной микроскопии (ПЭМ) с малым увеличением, синтезированных НС Pd, состоящих из однородных нанолистов с поперечными размерами около 10,0 нм (рис. 1b, вставка) и средней толщиной около 1.1 нм (рис. 1в, вставка). По размеру процентная доля верхней и нижней плоской поверхности составляет более 90%. Просвечивающая электронная микроскопия высокого разрешения (ПЭМВР) используется для дальнейшего подтверждения морфологии и фазы НП Pd. На рис. 1ж показаны соответствующие расстояния ~ 0,22 и 0,256 нм для плоскостей решетки (111) и (200) палладия [27]. Чтобы удовлетворить потребности эксперимента, дифрактограмма НС Pd характеризовалась нагрузкой на технический углерод. Как показано на рис. 1e, дифракционные пики около 40,11, 46,65 и 68,12 соответствуют плоскостям (111), (200) и (220) кубических НЗ Pd, что согласуется с наблюдениями с помощью ПЭМВР. Кроме того, отсутствуют пики, указывающие на наличие кристаллических фаз, кроме пиков, связанных с техническим углеродом. В спектре Pd 3d присутствуют два пика (рис. 1е). Pd 3d 5/2 и Pd 3d 3/2 (в результате спин-орбитального расщепления), расположенные соответственно при 335,5 и 339,2 эВ [25], что показало, что существует два химических окружения для атома палладия.
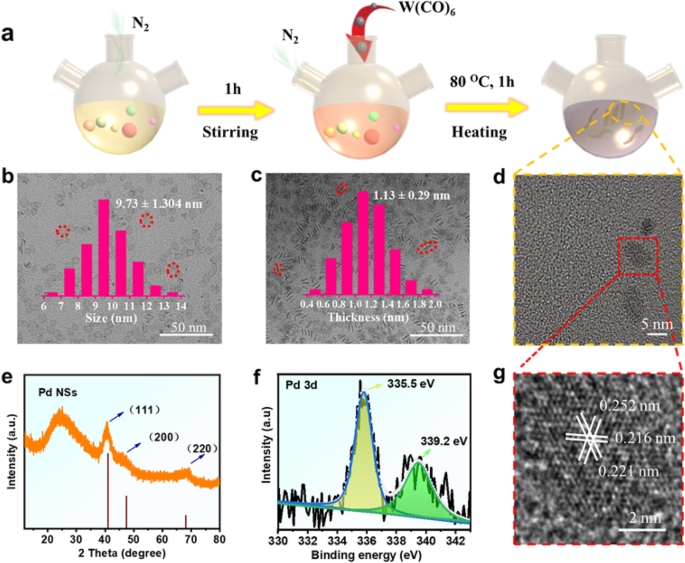
Характеристика нанозимов. а Механизм роста нанозимов Pd. б , c , и d ТЕМ. е Картины XRD. е Pd 3d РФЭС-спектр НЗ Pd. г ВРЭМ изображение НС Pd
Фотокаталитическое действие, имитирующее пероксидазу
Пероксидазоподобную активность НП Pd исследовали с использованием TMB в качестве типичного субстрата пероксидазы. Поскольку большинство атомов Pd экспонировалось на поверхности ультратонких нанолистов, мы полагаем, что ультратонкие НС Pd обладают высокой плотностью активных поверхностных центров и, таким образом, обеспечивают превосходную каталитическую активность. Как и ожидалось, при сосуществовании H 2 О 2 НС Pd могут эффективно катализировать окисление бесцветного субстрата TMB до синего продукта oxTMB с характеристическим поглощением при 652 нм (рис. 2a, b). Однако без добавления H 2 О 2 , активностью НП Pd можно пренебречь в тех же экспериментальных условиях, которые показали, что пероксидазоподобная активность играет важную роль во время реакции. Подобно природным ферментам и другим нанозимам, нанозимы Pd обладают пероксидазной активностью, зависящей от pH, температуры и концентрации (рис. 2c и рис. S1). В условиях эксперимента НС Pd проявляли оптимизированную каталитическую активность в слабом кислотном растворе, а характеристический пик поглощения реакционного раствора был максимальным при 35 ° C, когда температура изменялась от 25 до 75 ° C (рис. 2c). Неожиданно при световом облучении или без него наблюдалась значительная разница в активности, имитирующей пероксидазу (фиг. 2d и фиг. S2). Согласно значению поглощения реакционного раствора в течение 60 мин, активность НП Pd в видимом свете была примерно в 2,4 ~ 3,2 раза выше, чем активность НП Pd в темноте (рис. 2d и рис. S2). Точно так же введение света в процесс катализа других плазмонных металлических наночастиц может также увеличить их пероксидазоподобную активность (рис. S3 – S5). При сравнении этих нанозимов мы обнаружили, что НП Pd демонстрируют наибольший диапазон регуляции активности. Такое явление в основном связано с уникальной структурой ультратонкого нанолиста. Из этих полученных результатов мы можем сделать вывод, что видимый свет имеет прямое влияние на пероксидазоподобную активность всех плазмонных металлических наноматериалов (рис. 2e), а эффект SPR может играть важную роль в каталитическом процессе.
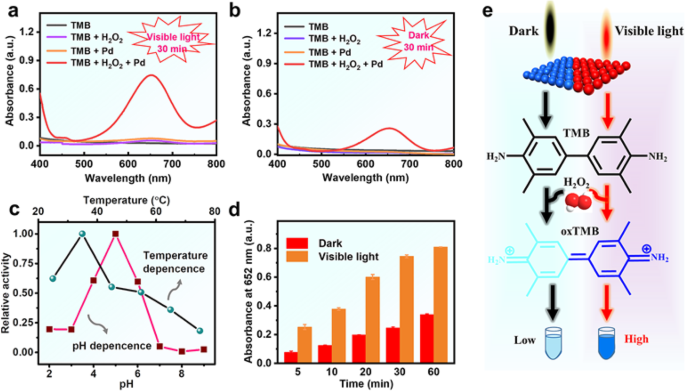
Имитирующая пероксидазу активность НП Pd. а-б Типичные спектры поглощения различных образцов в УФ и видимой областях в условиях видимого света и темноты. c Влияние температуры и pH на активность, имитирующую пероксидазу. г Временные курсы активности, имитирующей пероксидазу. е Пероксидазоподобный механизм НП Pd в темноте и в видимом свете. Условия эксперимента:видимый свет =λ ≥ 400 нм, TMB =0,7 мМ, H 2 О 2 =50 мМ, температура =25 ° C, НС Pd =12,6 мкг / мл и раствор фосфатного буфера (0,1 М, pH 4)
Исследование кинетики и механизмов нанозимов Pd
Чтобы охарактеризовать ферментативное поведение НП Pd, мы определили теорию кинетики фермента для реакции. Однако в подходящем диапазоне концентраций TMB НС Pd представляют собой типичную кривую Михаэлиса-Ментен (рис. 3а). Константа Михаэлиса (км) и максимальная скорость реакции (Vmax) были получены с использованием уравнения Лайнуивера-Берка, как показано в таблице S1. По сравнению с пероксидазой хрена (HRP) кажущееся значение Km для НП Pd с TMB было ослаблено на 0,28 (рис. 3a, b и таблица S1). Этот результат показывает, что ультратонкая пластинчатая структура свежеприготовленных НП Pd демонстрирует высокое сродство к TMB, даже более высокое, чем сродство природного фермента HRP.
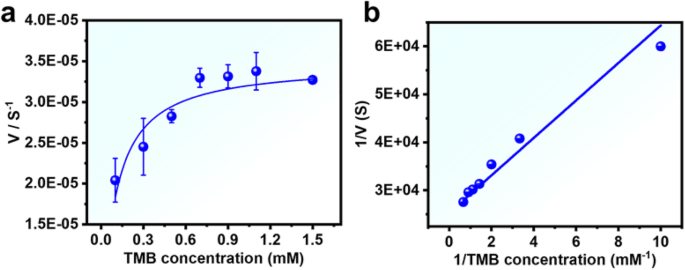
Кинетический анализ устойчивого состояния и каталитический механизм НП Pd (12,6 мкг / мл). а Концентрация H 2 О 2 составляла 50 мМ, концентрация ТМБ варьировалась (0,1–1,5 мМ). б Двойные взаимные графики для TMB
Поскольку ясно, что H 2 О 2 могут быть разложены с образованием активных форм кислорода с НС Pd, важно понимать, какие виды образуются для обеспечения окислительной функции. В принципе, благородные металлы могут катализировать разложение H 2 О 2 с образованием • OH и промежуточных продуктов реакции O * в условиях более низких pH [28], любой из которых может быть разновидностью, которая обеспечивает окислительную функцию в ферментативно-миметических реакциях. Чтобы понять возможный каталитический механизм НС Pd, мы сначала использовали терефталевую кислоту (ТА) / H 2 О 2 Система для проверки того, связаны ли пероксидазоподобные характеристики НП Pd с образованием радикалов • OH (рис. 4а). Используя ТА в качестве флуоресцентного зонда, был получен высоко флуоресцентный продукт реакцией 2-гидрокситерефталевой кислоты с • OH [29]. Как показано на рис. 4б, интенсивность флуоресценции раствора значительно снижается после добавления НС Pd. Результаты хорошо согласуются с интенсивностью флуоресценции, уменьшающейся с увеличением концентрации НП Pd (рис. S6). Эти результаты показывают, что НП Pd могут поглощать радикалы • OH, а не генерировать их. Следовательно, как и сообщалось о каталитическом поведении наночастиц ферритин-платина [30], каталитические характеристики наших НП Pd не зависели от образования радикала • OH.
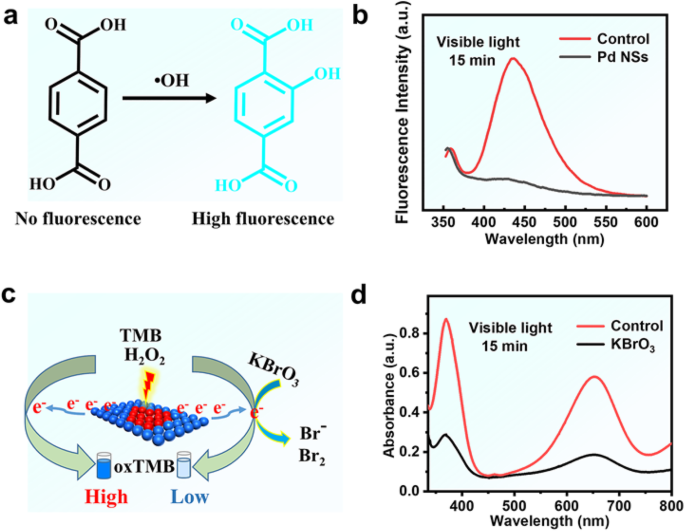
а Схема механизма захвата гидроксильных радикалов терефталевой кислотой (ТА) (• ОН). Спектры образцов, содержащих фосфатный буфер (0,1 М, pH 4), H 2 О 2 (50 мМ) и освещение в видимом свете ( λ ≥ 400 нм, 15 мин). б Спектры излучения флуоресценции в присутствии НС Pd (12,6 мкг / мл) и ТА (66,7 мкМ). c Схема механизма KBrO 3 захват горячей электроники. г Спектр поглощения в присутствии НС Pd (12,6 мкг / мл), KBrO 3 (0,3 мг / мл) и TMB (0,7 мМ)
Чтобы исследовать, связан ли каталитический механизм НП Pd с образованием горячих электронов светом, мы также исследуем эксперимент по захвату горячих электронов активных частиц во время фотокаталитической реакции (рис. 4c) [31]. Как видно из рис. 4d, каталитическая способность НП Pd по отношению к окислению ТМБ значительно снижается в течение 15 мин при добавлении 0,3 мг / мл KBrO 3 (тушитель е - ). Такая огромная разница между KBrO 3 / Реакционная система и чистая система показывают, что присутствие горячих электронов может иметь решающее значение для окисления ТМБ. Это согласуется с результатами рис. S7, что НС Pd имеют широкий пик поглощения за счет эффекта ППР в спектральном диапазоне 500–1000 нм [25]. Кроме того, когда горячие электроны удаляются от поверхности НЗ Pd, на их поверхности остаются соответствующие дырки. Поскольку эти дырки могут окислять этанол с образованием ацетальдегида, они также могут обладать мощной окислительной способностью по отношению к TMB. Как и ожидалось, без добавления H 2 О 2 , больше oxTMB было создано при освещении видимым светом.
Затем мы проверяем, образовались ли активные формы кислорода при активации O 2 в видимом свете, включая супероксид (O 2 - ). В связи с этим контролируемые эксперименты проводились в различных атмосферах. На рис. S8 каталитические характеристики миметических ферментов существенно не меняются, когда мы вводим азот и кислород при насыщении реакционной системы, соответственно, на что не оказывает значительного влияния O 2 для фотокаталитической активности НС Pd. Важно отметить, что предельная производительность Pd NSs, даже до 0,051 у.е. / мин в течение 5 минут в видимом свете, была в 3,2 раза выше, чем у катализаторов Pd NSs в темноте (рис. 2d). Чрезвычайно высокая активность нанозима Pd в видимом свете приводит к гипотезе о том, что существование горячих электронов за счет эффекта ППР НП Pd, способствующих образованию промежуточных продуктов реакции O * вместо свободных радикалов, объясняет пероксидазоподобную активность (рис. 5a). ) [28]. Короче говоря, эксперимент по отлову активных видов и эксперимент с вентиляцией обеспечивают надежную поддержку фотокаталитического ферментативного механизма, имитирующего Pd NS.
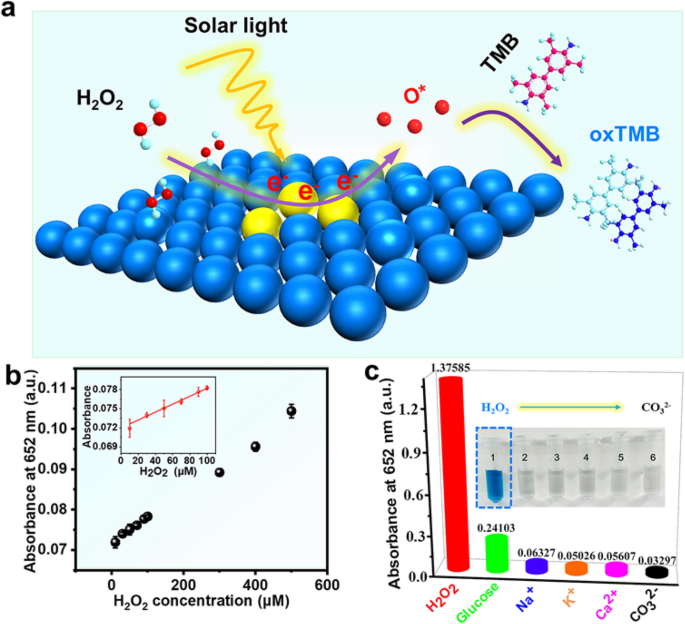
а Принципиальная схема датчика для H 2 О 2 обнаружение. б Кривая "доза-ответ" для различных концентраций перекиси водорода. Условия эксперимента:нанозим Pd (25,2 мкг / мл), фосфатный буфер (0,1 M, pH 4) и TMB (0,7 мМ), освещение в видимом свете ( λ ≥ 400 нм, 3 мин). На вставке:графики линейной калибровки. c Влияние других примесей на оптическую плотность H 2 О 2 колориметрический датчик на 652 нм. Условия эксперимента:нанозим Pd (25,2 мкг / мл), фосфатный буфер (0,1 M, pH 4), TMB (0,7 мМ), освещение в видимом свете ( λ ≥ 400 нм, 15 мин), включая 50 мМ H 2 О 2 , 200 мМ глюкоза, Na + , K + , Ca 2 + , и CO 3 2– , а на вставке показаны изменения цвета реакционных растворов
Новый высокочувствительный датчик реального времени
В нескольких исследованиях было продемонстрировано, что введение света в датчик в качестве входа внешней энергии может улучшить характеристики датчика [22, 32, 33]. Например, Ling et al. [32] обнаружили, что O 2 чувствительные свойства 10 ат. % LaOCl-SnO 2 Датчик был значительно улучшен за счет ультрафиолетовой подсветки. Учитывая значительное влияние света на датчик и превосходную имитирующую пероксидазу активность НП Pd в видимом свете в наших экспериментах, эффективный и чувствительный колориметрический датчик H 2 О 2 был построен. Механизм датчика (рис. 5а) показывает, что НЗ Pd могут полностью использовать свою большую удельную поверхность для захвата фотонов и генерации большого количества горячих электронов. После этого горячий электрон способствует разложению H 2 О 2 с образованием промежуточных продуктов реакции O *, которые могут окислять ТМБ до синего оксТМБ. Наконец, эффективное обнаружение H 2 О 2 было реализовано.
Как видно из вставки к рис. 5b, линейный диапазон построенного H 2 О 2 датчик был от 10 до 100 мкМ, а расчет предела обнаружения составил 13,40 мкМ (LOD =3 s / к , где s и k представляют собой блоки линейной калибровки относительного стандартного отклонения и наклона восьми параллельных контрольных измерений соответственно. В этой работе s =2,97988 × 10 −4 , k =6,67 × 10 −5 ). Таким образом, датчик перекиси водорода на основе НС Pd превосходил другие известные наноматериалы при условии введения света. Из Таблицы S2 видно, что при использовании того же колориметрического метода для определения перекиси водорода и нашего сенсора наблюдается широкий диапазон линейности [34]. И предел обнаружения был ниже, чем у многих сенсоров, основанных на имитаторах пероксидазы на основе Fe или Co (Таблица S3) [35, 36]. Наконец, мы выполнили H 2 О 2 и серию контрольных экспериментов (рис. 5c) с потенциальными помехами, такими как K + , глюкоза, Na + , CO 3 2– , и Ca 2+ . Как показано на вставке к рис. 5c, очевидно, что поглощение этих помех является слабым при 652 нм, и цвет не меняется. На основе наших результатов был успешно реализован эффективный и высокоспецифичный датчик перекиси водорода на основе видимого света. Этот датчик не только полностью использует видимый свет для улучшения характеристик обнаружения, но также является хорошим примером для других плазмонных металлов в датчике.
Выводы
Таким образом, мы продемонстрировали захватывающий пример применения ультратонких нанолистов Pd (Pd NS) в качестве высокоэффективного и контролируемого светом миметика пероксидазы благодаря высокой плотности активных центров на поверхности нанолистов и уникальному оптическому свойству SPR. При облучении видимым светом горячие электроны, генерируемые нанолистами Pd с помощью эффекта ППР, могут впоследствии разлагать H 2 О 2 для производства промежуточных продуктов O *. При облучении видимым светом такие нанозимы проявляли гораздо более высокую пероксидазоподобную активность, чем в темноте. Такая система, активируемая светом, в дальнейшем была использована для улучшенного биочувствительности H 2 О 2 . Представленная здесь базовая концепция, основанная на генерации горячего электричества за счет эффекта SPR на фотоактивированных нанозимах Pd, может внести вклад в разработку интеллектуальных или более эффективных систем искусственных ферментов и открыть множество новых возможностей для химической промышленности и биотехнологии.>
Доступность данных и материалов
Все данные, полученные или проанализированные в ходе этого исследования, включены в эту опубликованную статью.
Сокращения
- ПД NS:
-
Нанолисты Pd
- Ag:
-
Серебро
- Au:
-
Золото
- Pt:
-
Платина
- PDF-файл:
-
Палладий
- SPR:
-
Поверхностный плазмонный резонанс
- ТЕМ:
-
Просвечивающая электронная микроскопия
- HRTEM:
-
ТЕМ высокого разрешения
- XRD:
-
Рентгеновская дифракция
- HRP:
-
Пероксидаза хрена
- км:
-
Константа Михаэлиса
- O 2 - :
-
Супероксид
Наноматериалы
- Активность электронов в химических реакциях
- Нанозимы
- Прогнозирование разобщающей токсичности органических кислот
- Биосовместимые наночастицы FePO4:доставка лекарств, стабилизация РНК и функциональная активность
- Получение и повышенная активность каталитического гидрирования наночастиц Sb / палигорскита (PAL)
- Синергетические эффекты наночастиц Ag / BiV1-xMoxO4 с повышенной фотокаталитической активностью
- Синтез и активность окисления CO 1D смешанного бинарного оксида CeO2-LaO x, нанесенного золотыми катализаторами
- Синтез нанопластин Cu2ZnSnSe4 в одном резервуаре и их фотокаталитическая активность, управляемая видимым светом
- Изготовление, характеристика и биологическая активность систем нано-доставки авермектина с различными разм…
- Фотокаталитическая активность тройного нанокомпозита аттапульгит – TiO2 – Ag3PO4 для разложения родамина B при мод…



