Мини-обзор структуры и свойств (фотокатализ) и методов получения наночастиц на основе графитового нитрида углерода и их применения
Аннотация
Графитовый нитрид углерода (g-C 3 N 4 ) хорошо известен как один из самых многообещающих материалов для фотокаталитической активности, например CO 2 сокращение и разделение воды, а также восстановление окружающей среды за счет удаления органических загрязнителей. С другой стороны, нитрид углерода также демонстрирует выдающиеся свойства и широкие перспективы применения с точки зрения автоэмиссионных свойств. В этом мини-обзоре новая структура, методы синтеза и приготовления полнотелого g-C 3 N 4 на основе композита и пленок. В этом мини-обзоре обсуждались современные достижения в области структуры, синтеза и различных методов, используемых для получения g-C 3 N 4 наноструктурированные материалы. Настоящее исследование дает отчет о полных знаниях об использовании исключительной структуры и свойств, а также о методах получения нитрида углерода графита (g-C 3 N 4 ) и его приложения.
Введение
Центральный источник энергии, извлеченный из внеземного космоса, возможности солнечной энергии значительно превосходят мировой энергетический запрос альманаха [1]. Учитывая длительный прогноз эпохи Солнца, солнечная энергия также считается основным возобновляемым источником, который может быть добыт на планете Земля [2, 3]. Бесконечная и прерывистая природа этого источника энергии, однако, представляет ключевые проблемы во взаимоотношениях сбора, хранения и использования [4]. На данный момент существует ряд технологий, которые могут быть использованы для противодействия им. Солнечная энергия может гибко собираться, преобразовываться и храниться в форме тепла, которое может либо распределять тепло по жилью, либо в дальнейшем преобразовываться в электричество, а также в другие формы энергии [5]. Наиболее инновационными исследованными технологиями, касающимися получения солнечных фотонов, могут быть технологии фотокатализа, как описано Эдмондом Беккерелем, 1839 г. [5].
В основном, сточные воды являются основным источником загрязнения, в частности, сточные воды, образующиеся в результате химической индустриализации, потому что эти сточные воды содержат значительную концентрацию крупных органических фрагментов, которые являются чрезвычайно ядовитыми и канцерогенными по своей природе [3]. Ранее технология восстановления окружающей среды (которая включает адсорбцию, биологическое окисление, химическое окисление и сжигание) использовалась для очистки всех типов органических и токсичных сточных вод, а также эффективно применялась при использовании солнечной энергии, очистке окружающей среды и биомедицинские и сенсорные приложения. Фудзисима и Хонда раскрыли исключительные знания о фотохимическом расщеплении воды на водород и кислород в присутствии TiO 2 в 1972 г .; Исследовательский интерес был сосредоточен на гетерогенном фотокатализе [3,4,5]. Ускорение фотореакции в присутствии катализатора описывается как фотокатализ. Наиболее известно, что реакция фотокатализа проводится в таких средах, как газовая фаза, чистые органические жидкие фазы или водные растворы. Кроме того, в большинстве методов химической деградации фотокаталитическая деградация по отношению к фотонам и катализатору часто определяется как лучший способ контроля органических сточных вод, использования солнечной энергии, обработки окружающей среды, а также биомедицинских и сенсорных приложений [3, 5]. Следовательно, самые современные технологии, используемые для очистки органических сточных вод и связанных с ними применений, приписываются развивающимся фотокатализаторам, работающим от солнечного света [3].
Полупроводниковые фотокатализаторы можно использовать для удаления атмосферных концентраций органических и неорганических веществ из водной или газовой фазы систем при очистке питьевой воды, охране окружающей среды, а также в промышленности и здравоохранении. Это связано с огромной способностью этих полупроводников (g-C 3 N 4, TiO 2 - и ZnO) для окисления органических и неорганических субстратов в воздухе и воде посредством окислительно-восстановительных процессов для эффективного использования солнечной энергии, сточных вод, очистки окружающей среды, биомедицины и датчиков без какого-либо вторичного загрязнения.
Полимерный графитовый нитрид углерода (g-C 3 N 4 ) стал основным центром исследований в области фотокатализа [6]. g-C 3 N 4 представляет собой реагирующий на видимый свет элемент с шириной запрещенной зоны 2,7 эВ, а энергетическое положение CB и VB составляет - 1,1 и 1,6 эВ через нормальный водородный электрод соответственно [Wang et al. 2009]. Кроме того, g-C 3 N 4 обладает способностью противостоять воздействию тепла, сильной кислоты и сильного щелочного раствора [7]. g-C 3 N 4 обладает уникальной способностью быть просто термической поликонденсацией дешевых предшественников, богатых азотом, таких как дицианамид, цианамид, меламин, цианурат меламина и мочевина, и это отличается от других металлосодержащих фотокатализаторов, для получения которых требуются дорогостоящие соли металлов [ 6, 8]. Термическая конденсация, сольвотермический процесс, химическое осаждение из паровой фазы, микроволновая печь, полимеризация и гидротермальный синтез являются примерами препаративных стратегий (таблица 2), которые с одобрением применялись при получении нитрида углерода для различных целей и анализа в области фотокатализа и др. [9].
Благодаря этим выдающимся свойствам g-C 3 N 4 , использование этого многообещающего g-C 3 N 4 при расщеплении воды, CO 2 фото восстановление, очистка от органических загрязнений, каталитический органический синтез и топливные элементы более эффективны и эффективны [6]. Количество замечательных исследований и обзоров на g-C 3 N 4 структура и подготовка за последние несколько лет значительно увеличились [10]. Авторы в основном сделали упор на самые современные достижения в области структуры, синтеза и методов получения g-C 3 N 4 и нитрид углерода (CN x ))))))))) в этом кратком мини-обзоре. Уникальная структура и новые методы синтеза и получения g-C 3 N 4 , и CN X фильмы красиво представлены, и просвещенные концепции по расширению подготовки g-C 3 N 4 в этом мини-обзоре подчеркнуты. Также авторы обсудили приложения на g-C 3 N 4 , а также высказывались мнения о перспективах будущих исследований.
Обзор
Графитовый нитрид углерода и фотокатализ
Фотокатализ лучше всего относить к ускорению химических превращений (окисления и восстановления), вызванных активацией катализатора. В этой реакции участвует полупроводник либо сам по себе, либо в комбинации с металлическими / органическими / металлоорганическими промоторами через поглощение света, последующий перенос заряда или энергии для адсорбции, что может привести к фотокаталитическому превращению загрязнителя. В механизме фотокатализа одновременно происходит по крайней мере два основных действия, которые способствуют успешному производству реакционноспособных окисляющих веществ (рис. 2). Эти реакции представляют собой окисление диссоциативно адсорбированного H 2 O в основном генерируется фотогенерированными дырками, а восстановление акцептора электронов также создается фотовозбужденными электронами (рис. 2). Следовательно, в этих реакциях образуются гидроксильный и супероксидный анион-радикалы соответственно [11]. Во время реакции фотокатализа очевидно, что происходит генерация каталитически активных частиц с помощью фотонов вместо действия света в качестве катализатора в реакции [12,13,14,15, 16]. В значительной степени получение видимого света, в основном солнечного света, катализатором (фотокатализатором) для инициирования химических превращений (рис. 1) описывается как фотокатализ. Применение C 3 N 4 Фотокатализатор для очистки сточных вод, использования солнечной энергии, очистки окружающей среды, а также биомедицинских и сенсорных приложений обсуждался во многих областях науки.
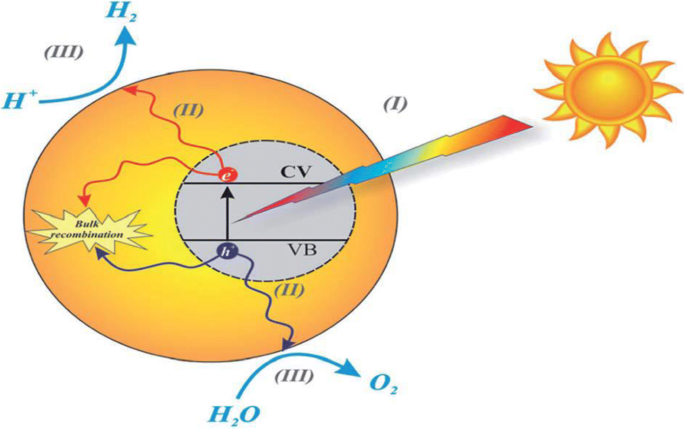
Принципиальная схема основных механизмов фотокаталитической активности расщепления воды. Воспроизведено с разрешения [113, 114]. Авторские права 2015 и 2018. Королевское химическое общество
Просветление полупроводникового катализатора, такого как TiO 2 , ZnO, ZrO 2 , и главный исполнительный директор 2 с фотонами, несущими энергию, равную ширине запрещенной зоны или превышающую ее, создавая пару электронов-дырок, аналогичную фотоиндуцированному переносу электронов и поглощению света, один электрон попадает в зону проводимости. Оксид может передавать свой электрон (рис. 2) любому адсорбированному акцептору электронов (тем самым способствуя его восстановлению), в то время как дырка (или электронная вакансия) может принимать электрон от адсорбированного донора (способствуя его окислению). g-C 3 N 4 способен катализировать выделение водорода / кислорода и CO 2 восстановление при возбуждении запрещенной зоны и в присутствии подходящих сокатализаторов и / или жертвенных агентов.
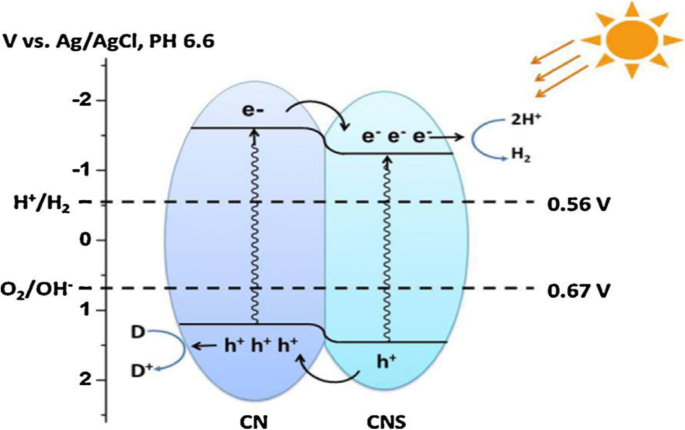
Схематическое изображение органического гетероперехода, образованного между g-C3N4 и g-C3N4, легированным серой. Воспроизведено из исх. [115]. Авторские права 2015. Elsevier
Графитовая наночастица из нитрида углерода
Материалы с одномерными наноструктурами, обладающими определенными электронными, химическими и оптическими свойствами, могут иметь скорректированный размер и морфологию. Эта способность одномерных наноструктурированных материалов привела к новому развитию разнообразных подходов к улучшению их фотокаталитической активности [17]. Кроме того, эти одномерные наноструктуры управляют движением электронов в осевом направлении и боковым ограничением электронов. Было продвинуто развитие 2D-материалов от графена до нанолистов из оксидов металлов и халькогенидов металлов, а затем и до 2D ковалентных органических каркасов (g-C3N4).
Соответствующие средства выбора прекурсоров и методов конденсации привели к двум основным типам g-C 3 N 4 структурные полиморфы, и это включает, во-первых, g-C 3 N 4 состоят из конденсированных звеньев s-триазина (кольцо C 3 N 3 ) с периодическим набором одноуглеродных вакансий. Второй тип g-C 3 N 4 состоит из конденсированного три-s-триазина (три-кольцо C 6 N 7 ) субъединицы, связанные через плоские третичные аминогруппы, и это имеет больше периодических вакансий в решетке. G-C 3 N 4 Сети в основном состоят из сегментов на основе дыни (структура второго типа; она состоит из три-s-триазина, рис. 3а), которая термодинамически более стабильна по сравнению с структурами на основе меламина (структура первого типа; она состоит из s-триазин, рис. 3b), как описано расчетами функциональной теории (DFT) [18]. Следовательно, широко распространено мнение, что ядро три-s-триазина является фундаментальным строительным блоком для образования g-C 3 N 4 сеть.
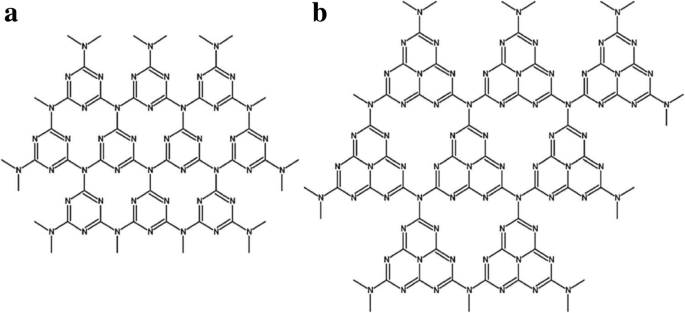
а Три-s-триазин и b три-s-триазин как структурные единицы g-C 3 N 4 . Воспроизведено с разрешения [25, 31]. Авторское право 2008 г., Королевское химическое общество
Структура наночастиц на основе графитового нитрида углерода
g-C 3 N 4 представляют собой класс двумерных (2D) полимерных материалов, состоящих полностью из ковалентно связанных, sp 2 -гибридизованные атомы углерода и азота. Углерод и азот имеют различие в различных валентных состояниях, образующих связь; следовательно, в g-C 3 N 4 , существуют разнообразные структуры валентных связей. Исследования показали, что некоторые C 3 N 4 дефектные структуры и аморфные структуры g-C 3 N 4 остаются метастабильными структурами, но с появлением N вакансий эти два типа конфигурации g-C 3 N 4 Материал обычно уменьшается в объемном модуле. Структурные характеристики, состав материалов и кристалличность g-C 3 N 4 могут быть охарактеризованы и оценены методами XRD, XPS и Рамана. В 1830 году Берцелиус описал общую формулу (C 3 N 3 H) n и Либих также изобрели обозначение «дыня», и эти предсказания привели к дальнейшим исследованиям, сосредоточенным на олигомерах и полимерах нитрида углерода [19, 20]. Кроме того, эти кристаллические структуры были обнаружены и заявлены в экспериментах [21,22,23]. Α-C 3 N 4 ранее обнаружен Yu и соавторами [24]. Графитоподобная нагруженная 2D структура графита C 3 N 4 обычно наблюдается как гетероатомзамещенный азотом графитовый каркас, который в основном включает p-сопряженные графитовые плоскости, и это с sp 2 гибридизация атомов углерода и азота. Кристаллический графит на 3% менее плотен, чем g-C 3 . N 4 . Сдвиг локализации электронов и последующая консолидация связей между слоями из-за замещения гетероатома азота может помочь уточнить межслоевое расстояние g-C 3 N 4 [25].
Электронная структура и свойства g-C 3 N 4
В настоящее время g-C3N4 рассматривается как фотокатализатор нового поколения для восстановления фотокаталитической активности традиционных фотокатализаторов, таких как TiO 2 , ZnO и WO3. Предполагается, что g-C3N4 имеет графитоподобную структуру [26,27,28, 29, 30]. Метод термической поликонденсации обычно используется для получения g-C3N4 и, следовательно, для исследования электронной структуры g-C3N4.
Α-C 3 N 4 ранее обнаружен Yu и соавторами [24]. Эти ученые использовали процедуру расчета модели кластеров квантовой механики и разработали α-C 3 N 4 путем оптимизации электронной структуры g-C 3 N 4 для фотокатализа и др. В структуре альфа-C 3 N 4 , Атомы C и N связаны sp 3 Ключевым моментом была использованная конструкция тетраэдрической структуры g-C3N4. Лю и Коэн ожидали существования бета-C 3 N 4 с помощью концепции группы из первых принципов и подготовленной бета-версии C 3 N 4 на основе β -Si 3 N 4 электронная структура. Затем Лю и Коэн показали, что структура β -C 3 N 4 гексагональный, содержащий 14 атомов в каждой элементарной ячейке.
Выдающееся предсказание Лю и Коэна в 1989 г. о том, что b-полиморф C 3 N 4 будет иметь исключительно высокие значения твердости по сравнению с алмазом, что вызвало энтузиазм в научных исследованиях на сегодняшний день [26]. В 1993 году C 3 N 4 тонких пленок посредством магнетронного нюхания графитовой мишени на подложках Si (100) и поликристаллического Zr в атмосфере чистого азота с учетом структуры C 3 N 4 с аналитической электронной микроскопией и рамановской спектроскопией были синтезированы Ченом и соавторами [27, 31]. Ученые Тетер и Хемли [28] предсказали, что альфа-C 3 N 4 , бета-C 3 N 4 , кубический-C 3 N 4 , псевдокубический-C 3 N 4 , и графит C 3 N 4 демонстрируют ярко выраженную твердость, приближающуюся к твердости алмаза, в своем эксперименте, который они провели 3 года спустя, как уже было описано в соответствии с первопринципными расчетами относительной стабильности, структуры и физических свойств полиморфов нитрида углерода.
Ван с соавторами [26, 32] применили ab initio поиск структуры эволюционного алгоритма для расчета точной структуры g-C3N4, полученного методами термической поликонденсации и синтеза солевого расплава для улучшенного чувствительного к видимому свету фотокатализа. Наиболее стабильная структура 1–3 была предсказана для g-C3N4 на основе гептазина. Порядок фазовой стабильности был 1> 2> 3. В отличие от других слоистых структур, искаженные фазы в g-C3N4 на основе гептазина (см. Рис. 3) были наиболее стабильными. Эта структура способствует повышенной фотокаталитической активности обещанного. В g-C3N4 неподеленные пары электронов азота в основном ответственны за зонную структуру и развитие валентной зоны.
Приготовление наночастиц на основе графитового нитрида углерода
Синтез
Интересная трибологическая и электронная природа графитовых нитридов углерода позволяет разработать метод контролируемого осаждения слоев графитовых нитридов углерода; следовательно, может быть получен нитрид графена. В значительной степени эталонной частицей для сравнения является громоздкий g-C3N4. Эта частица может быть наилучшим образом получена путем выбора богатых азотом прекурсоров без прямой связи C – C, таких как цианамид, дициандиамид, меламин, тиомочевина, мочевина или смеси, с помощью различных методов подготовки (таблицы 1, 2 и 3) для мгновенная, термическая конденсация [33]. Материалы из нитрида углерода - это в основном сыпучие ресурсы с небольшой площадью поверхности, обычно менее 10 м 2 г −1 когда они получены или синтезированы прямой конденсацией азотсодержащих органических предшественников [34].
Мезопористая структура при минерализации и увеличении удельной поверхности помогает точно настроить физико-химические свойства, а затем увеличивает фотокаталитические характеристики нитрида углерода графита (g-C 3 N 4 ). Нанолитье / репликация матриц мезопористого диоксида кремния - это первый метод, используемый для получения графитового нитрида углерода (g-C 3 N 4 ), они славились своей когортой соответствующих углеродных наноструктур [35]. Затем были приложены большие усилия для разработки более инновационных схем для g-C 3 N 4 модификация, которая пришлась по душе жесткому шаблонному методу (табл. 1). Затем Лю и Коэн открыли технику мягких шаблонов (таблица 1) [26], а также другой метод g-C 3 N 4 были также обнаружены схемы модификации, такие как пропитка кислотным раствором, метод ультразвукового диспергирования и химическая функционализация [26]. Эти методы, как описано выше, были хорошим знаком принципа изменения химических свойств поверхности и текстуры g-C 3 N 4 наедине со своим электронным потенциалом.
Термические обработки, такие как физическое осаждение из паровой фазы (PVD) [36], химическое осаждение из паровой фазы (CVD) [37], сольвотермический метод [38] и твердотельная реакция [38], используются для полимеризации большого количества азота и кислорода. -свободные соединения-предшественники, содержащие предварительно связанные структуры ядра C – N (производные триазина и гептазина), и они служат в качестве основных методов для графитового нитрида углерода (gC 3 N 4 ) синтез. Обычно используемые прекурсоры для получения нитрида углерода графита (g-C 3 N 4 ) путем полимеризации включают цианамид [39], дициандиамид [40], меламин [41], мочевину [42], тиомочевину [43], хлорид гуанидиния [44] и тиоцианат гуанидина [45]. Прямое использование выполненных элементов на самом деле является сложной задачей во многих областях; это связано со слабой дисперсностью и обычным характером объемного g-C 3 N 4 . Использование обширных микро / наноструктур и морфологий для приготовления различных видов g-C 3 N 4 был интенсивно исследован учеными за последние несколько лет исследований фотокатализа. Например, ультратонкий g-C 3 N 4 нанолисты, которые были приготовлены расслоением большого количества g-C 3 N 4 материалы [46,47,48] имели отрицательный заряд и могли хорошо диспергироваться в воде.
Отшелушивание термическим окислением, ультразвуковое отшелушивание и химическое отшелушивание хорошо известны как основные методы отшелушивания, используемые для получения g-C 3 N 4 материалы. Мезо-g-C 3 N 4 материалы обладают отличными характеристиками, такими как отличная фотокаталитическая активность за счет большей удельной поверхности (до 830 м 2 г −1 ) и большей пористостью (до 1,25 см 3 г −1 ); кроме того, большее количество активных центров, присутствующих на поверхности, и более высокая избирательность по размеру или форме улучшают их превосходные характеристики. Наиболее важные пути получения мезо-g-C 3 N 4 включают мягкие шаблоны (самосборка) [49, 50] и жесткие шаблоны (нанолитье) [51] (таблица 1 и рис. 4). Меньшие размеры, широко известные как g-C 3 N 4 квантовые точки (КТ) использовались многими выдающимися учеными в их исследованиях по синтезу g-C 3 N 4 [52,53,54,55]. Два основных подхода к синтезу 2D g-C 3 N 4 нанолисты представляют собой расслоение слоистого g-C 3 N 4 твердых тел в отдельно стоящие нанолисты, в основном известные как стратегия «сверху вниз» (рис. 5) и анизотропная сборка органических молекул в 2D (рис. 6), также называемая стратегией «снизу вверх». [56] Что примечательно для разнообразной химической структуры и электронной зонной структуры нанолистов CN, полученные нанолисты CN показали уникальный отклик излучения электрохемилюминесценции (ECL) на многочисленные ионы металлов. Благодаря этому был успешно разработан датчик ECL с быстрым обнаружением множества ионов металлов.

TEM-изображения TCN ( a и b ) и MCN ( c и d ) с использованием жесткого шаблонного подхода. Воспроизведено с разрешения из [120]. Авторские права 2015. Elsevier
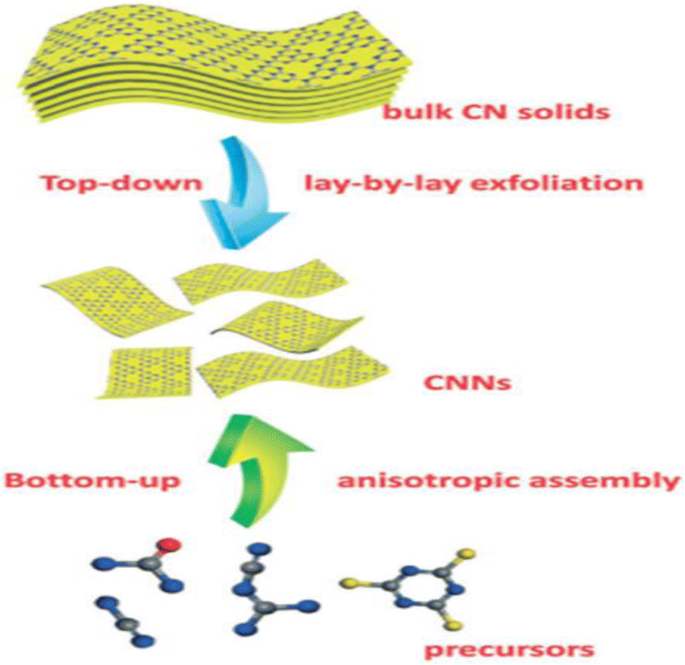
Схематическая иллюстрация синтеза CNN с использованием стратегий «сверху вниз» и «снизу вверх» (воспроизведено из ссылки [121] с разрешения Королевского химического общества)
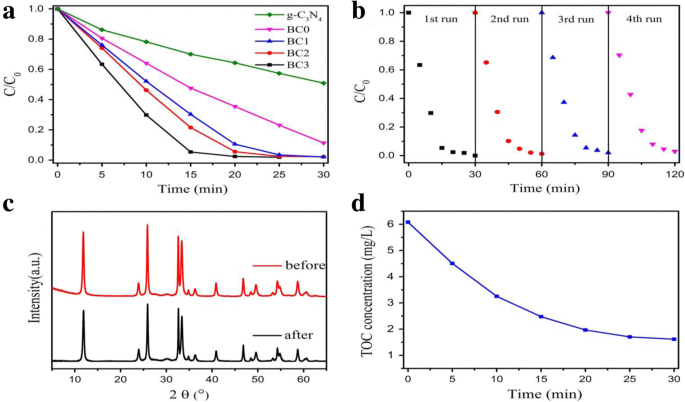
Принципиальная схема получения и улучшенного фотокаталитического действия в видимом свете за счет уменьшения RhB с помощью различных фотокатализаторов в зависимости от времени облучения видимым светом (загрузка фотокатализаторов, 0,5 г / л; начальная концентрация RhB, около 10 мг / л, без модуляции pH). В качестве фотокатализаторов использовали чистый g-C3N4 и a . серия гибридов g-C3N4 / BiOCl, b циклическая деградация RhB по BC3, c Картины XRD фотокатализаторов BC3 до и после фотокаталитического процесса, а также d графики зависимости ТОС от времени разложения. (Воспроизведено из ссылки [122] с разрешения Springer-Verlag GmbH, Германия, 2017 г.)
Методы, используемые при получении наночастиц на основе графитового нитрида углерода
Исследование по синтезу нитрида углерода (g-C 3 N 4 и CN x ) вызвал энтузиазм исследователей со всего мира. g-C 3 N 4 синтезированы пленки с точными фотокаталитическими свойствами [57, 58]. Подходы термической конденсации, сольвотермического, химического осаждения из паровой фазы, с использованием микроволнового излучения, полимеризации и гидротермального синтеза (таблица 2) эффективно используются для получения нитрида углерода для различных целей и анализа в области фотокатализа и др. [9 ].
Методы термической и сольвотермической обработки
Основываясь на реакции поликонденсации между меламином и цианурхлоридом в присутствии никелевого порошка, Ли и исследовательская группа [41] предложили два основных метода синтеза богатых азотом нитридов графита. Эти два метода были сольвотермическими методами с использованием бензола в качестве растворителя и твердыми реакциями без растворителей с термической обработкой (рис. 7). Другие работы многих ученых [59,60,61,62, 63] предполагают, что сольвотермические реакции обычно приводят к образованию кристаллов после промывки и сушки и не требуют обработки после отжига. Эти ученые также предложили увеличить фотокаталитическую активность с помощью этого метода (рис. 8).

SEM-изображения образца B:( a ) частицы оксида алюминия, покрытые нитридом углерода; ( б ) деталь выступающих вмятин из нитрида углерода. Можно наблюдать зазубренную форму листов нитрида углерода, полученных пиролизом. SEM-изображения образца A:( c ) и ( d ) виды частиц оксида алюминия, покрытых нитридом углерода. Воспроизведено с [60]

ПЭМ-изображения и электронограмма mp-C3N4 после удаления наночастиц диоксида кремния. Воспроизведено с разрешения [123]. Авторское право John Wiley &Sons Inc., 2006 г.
Ниу и Ко. также сообщили о морфологических изменениях при использовании сольвотермической техники [64]. Loumagne и соавторы [65] засвидетельствовали физико-химические свойства отложений на основе SiC, достигаемые за счет термического разложения CH3SiCl3 в водороде. Келли и группа [66] сообщили о синтезе TaC с использованием реагентов хлорида тантала (V) и углерода, смешанных в перчаточном боксе, заполненном аргоном, посредством термического процесса. Последовательно, метод термической конденсации, который в основном состоит из системы сопряженного ароматического гептазина с характеристиками сборки графита, был использован несколько моментов для получения g-C 3 N 4 [36]. Использование сольвотермической техники для g-C 3 N 4 Синтез имеет большие выгоды, такие как образование равномерных и мелких частиц, низкое потребление энергии и более высокую экономическую целесообразность по сравнению с устаревшим методом термической конденсации. И наоборот, эти методы по-прежнему требуют много времени и в определенной степени требуют нескольких часов для завершения образования и кристаллизации частиц.
Химическое осаждение из паровой фазы
Исследование Роберто с соавторами [60] показало, что использование химического осаждения из паровой фазы (CVD) для синтеза графитового нитрида углерода посредством реакции между меламином и мочевой кислотой имеет высокую фотокаталитическую активность. Было обнаружено, что образовавшийся графитовый нитрид углерода имел структуру на основе блоков гептазина.
Затем Роберто и его коллеги предположили, что природа этих нитридов углерода проявляет неровную форму (рис. 7), кристалличность и нанометрическую текстуру. Келли и др. [66] сообщил о синтезе TaC с использованием реагентов хлорида тантала (V) и углерода, смешанных под перчаточным боксом, заполненным аргоном, с помощью термической технологии, а затем преобразованных в наночастицы TaC с помощью химической технологии. CVD - один из наиболее полезных методов получения монослойного графена высокого структурного качества для использования в различных устройствах для каталитической активности [67]. Ван и группа [26, 32] впервые получили пленки CN на подложке из Ni методом HFCVD. Поскольку приготовление этих пленок с большей вероятностью приведет к образованию связей C – H и N – H в условиях химического осаждения из паровой фазы, большинство пленок CN являются аморфными. Судя по предыдущим исследованиям, для получения нитридов углерода используются процедуры CVD, поэтому выбор материалов подложки очень важен. Образцы большой площади можно приготовить, подвергая металл воздействию различных углеводородных предшественников при высоких температурах. Доступны различные типы методов CVD, такие как CVD с плазменным усилением, термическое CVD и CVD с горячей / холодной стенкой. Методы CVD в основном состоят из электронного циклотронного резонанса, горячей нити накала, тлеющего разряда постоянного тока, радиочастотного разряда и химического осаждения из газовой фазы с помощью микроволновой плазмы. Смещение вспомогательного химического осаждения из газовой фазы горячей нитью (HFCVD) - один из местных инструментов, используемых при осаждении алмазных и других пленок. Точный механизм образования графена зависит от ростовой подложки, но обычно начинается с роста атомов углерода, которые зарождаются на металле после разложения углеводородов, и зародыши затем разрастаются в большие домены [68]. Недавно производство высококачественного однослойного графена с использованием резистивного нагрева с холодной стенкой CVD также было в 100 раз быстрее, чем традиционное CVD.
Синтез золь – геля
Метод золь-гель-синтеза - это процесс, посредством которого твердый продукт или наноматериал образуется из раствора после превращения гелевого промежуточного продукта. В этом методе синтеза реагенты смешиваются на молекулярном уровне, обеспечивая быстрые реакции и приводя к более однородным продуктам с большей площадью поверхности. Примечательно, что этот метод был использован для синтеза различных типов наночастиц, включая карбид металла и нитридные процессы для фотокатализа [69]. Синтез нитрида металла с использованием золь-гель процессов можно проследить до использования металлорганических соединений (синтезированных из элемента металла и диалкиламина) [70].
Микроволновое отопление
В последнее время микроволновый нагрев широко используется для приготовления тонких химикатов и фармацевтических препаратов по сравнению с методами, описанными выше, поскольку он обеспечивает широкий диапазон реакций и короткое время реакции, которые подходят для производства в промышленных масштабах [71]. Ван и его коллеги использовали простую технику для синтеза g-C 3 N 4 с использованием дешевого / менее дорогого прекурсора, богатого азотом, который затем может быть активным в качестве фотокатализатора для образования H 2 и O 2 под облучением видимым светом для своих исследований. Микроволновое излучение ускоряет химическую реакцию и снижает потребляемую энергию, следовательно, проникая в реакционный сосуд и открывая доступную энергию для реагентов и растворителя с большой скоростью теплопередачи. Техника микроволнового нагрева отличается от традиционных методов, таких как масляные ванны и нагревательные камеры; этот метод более эффективен и надежен. Микроволновое излучение, касающееся нагревания закрытой реакционной системы с сольвотермическим давлением, реагенты могут вступать в реакцию и превращаться в продукты гораздо быстрее, чем при использовании обычного метода. Дай и его коллеги предложили экономичный и экономичный способ синтеза g-C 3 N 4 недавно использовала полимеризацию с помощью микроволн. Затем Дай и его коллеги выяснили, что g-C 3 N 4 получен образец, демонстрирующий субмикросферы и большую площадь поверхности 90 м 2 г −1 , (Рис. 9) и был успешно синтезирован при 180 ° C в условиях микроволнового облучения в течение всего 30 мин, что показало улучшенные фотокаталитические характеристики [71]. Эксперименты, проведенные Ху и соавторами, также показали, что синтезированный с помощью микроволнового излучения g-C 3 N 4 имеет хорошую химическую и термическую стабильность и большую интенсивность излучения, чем у обычного [71]. Ху и его коллеги также заявили, что микроволновая печь синтезировала g-C 3 N 4 работает лучше при фотокатализе в видимом свете.
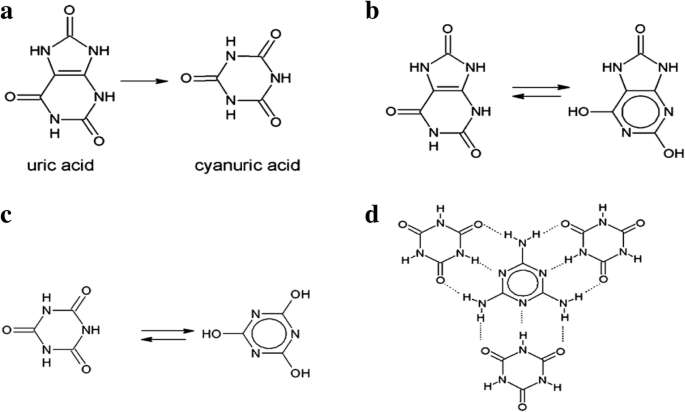
( а ) Термическое разложение мочевой кислоты до циануровой кислоты; ( б ) таутомеры мочевой кислоты; ( c ) таутомеры циануровой кислоты; ( д ) схематическое изображение фрагмента слоя аддукта, называемого циануратом меламина
Физическое осаждение из паровой фазы
Он состоит из магнетронного распыления, осаждения ионным пучком (IBD), реакционного распыления, импульсного лазерного осаждения и т. Д. Реакционное распыление - простейший метод приготовления композитов. Когда этот метод используется для приготовления g-C 3 N 4 , массовая доля азота обычно менее 40%. И наоборот, чтобы сформировать 훽 -C 3 N 4 , система должна состоять из достаточного количества азота, а стехиометрическое соотношение должно достигать 57%. Ниу и его группа [72] достигли уровня g-C 3 N 4 на кремниевой подложке с помощью импульсного лазерного испарения мишени C, вспомогательного осаждения атома азота. Niu et al. Исследования показали, что количество N достигало 40% в пленках, а затем атомов C, N, объединенных неполярной ковалентной связью. Последовательно Sharma et al. [73] и Zhang et al. [74] также провели несколько критических исследований, а затем получили пленки CN аналогичным методом, как обсуждалось. Михайлеску и его коллеги [75] также использовали аммиак вместо N 2 . - изготовили жесткие пленки CN 푥 с одинарной, двойной и тройной связью углерод-азот, а затем выяснили, что его оптическая ширина запрещенной зоны составляет 4,5 эВ. Согласно недавнему исследованию, ученые часто получают смеси пленок, состоящих из нескольких кристаллических фаз.
Чтобы оценить эффективность приготовленного g-C 3 N 4 Фотокаталитическое выделение водорода с использованием кристаллических нитридов углерода (CN) было предложено Таканабе и его группой [76]. Takanabe et al. приобрели нитриды углерода в результате супрамолекулярной агрегации (таблица 3), которая в дальнейшем контролировалась (таблица 3) ионной поликонденсацией в расплаве (IMP) с использованием меламина и 2,4,6-триаминопиримидина в качестве допанта. Есть несколько других методов, похожих на то, что Таканабе и его группа использовали в своем эксперименте, см. Таблицу 3.
Применение графитового нитрида углерода
У этого графитового нитрида углерода есть несколько новых применений, в том числе базовое зондирование, биомедицинские приложения, очистка сточных вод и окружающей среды, использование солнечной энергии и его использование в производстве устройств.
Использование солнечной энергии
Увеличение видимой чувствительной активности нитрида углерода зависит не только от управления структурой молекул, синтеза и методов получения CN, но также зависит от способности изменять электронные структуры этих материалов. Обычно при облучении видимым светом нитриды углерода могут использоваться для изготовления фотоэлектрода и, таким образом, генерирования фототока. Эта способность g-C 3 N 4 происходит из-за исключительной обратимой природы протонирования и депротонирования. Один из лучших подходов - использование солнечного топлива из CO 2 и вода (производимая большинством фотокатализаторов) для производства H 2 , углеводороды, синтез-газ для энергии и др. [77, 78]. Было предложено, чтобы g-C 3 N 4 имеет потенциал быть безметалловыми и масштабируемыми фотокатализаторами для использования в видимом свете в зависимости от применяемой структуры, синтеза и техники приготовления. Недавняя работа Лю и его команды [79] предложила новую разработку метода жертвенного шаблона для создания мезопористого g-C 3 N 4 сферы и высокопроизводительная схема. Этот предложенный метод может быть использован для синтеза g-C 3 N 4 стержни, и это лучше всего подходит для регенерации NADH (рис. 10a – c) для успешного производства энергии и др.
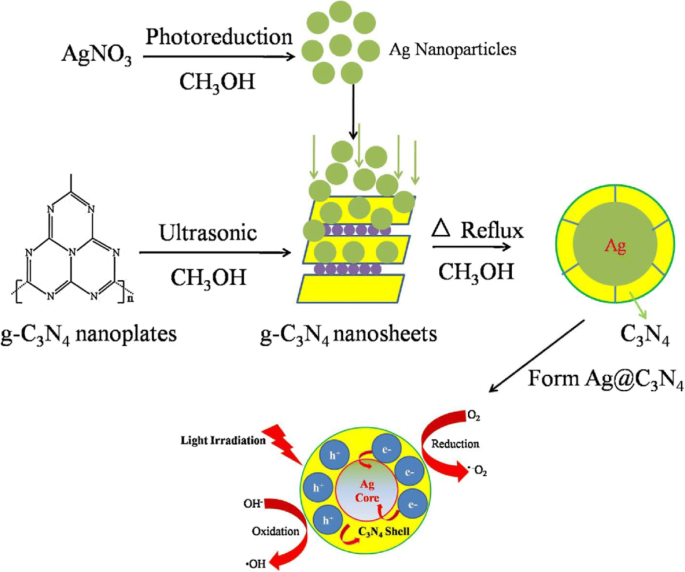
Схематический рисунок, иллюстрирующий путь синтеза (метод шаблонов) и механизм разделения зарядов и фотокаталитический процесс на фотокатализаторах C3N4 и Ag @ C3N4 при световом облучении. Воспроизведено с разрешения [124]. Авторское право Elsevier, 2014 г.
Сточные воды и очистка окружающей среды
Большинство процессов в нефтехимической, нефтехимической, текстильной и пищевой промышленности приводят к загрязнению окружающей среды, а точнее водоемов [80]. В производстве текстиля, фотоматериалов и полиграфических материалов используются органические красители, которые в процессе окрашивания проникают в большую часть водной среды [81]. Несмотря на вредное воздействие этих красителей на здоровье человека и животных, их биологическая и химическая деградация является сложной задачей [82, 83]. Из-за этой угрозы существует необходимость в разработке улучшенного процесса окисления для обработки загрязненной питьевой воды и неразлагаемых материалов [84, 85]. Большинство исследований [86,87,88,89,90] доказали, что использование полупроводников, таких как g-C 3 N 4 для фотокатализа - лучший метод очистки сточных вод и окружающей среды из-за их менее вредного характера [86,87,88,89,90]. g-C 3 N 4 наиболее известны как потенциальные фотокатализаторы для разложения множества загрязнителей [16, 90, 91], при этом фотофизические потенциалы исходного нитрида изменяются путем легирования гетероатомами, образования гетеропереходов с другими материалами и улучшения текстуры для увеличения площади поверхности и пористости . Структура, синтез и методы получения g-C 3 N 4 Нанолисты также определяют эффективность фотокатализатора и его применение при очистке сточных вод. Ультратонкий g-C 3 N 4 нанолисты, полученные из большого количества g-C 3 N 4 путем эксфолиации в метаноле обнаруживают повышенную фотокаталитическую активность (рис. 11) в отношении разложения метиленового синего (МБ) [92]. Синтез и приготовление кандидата путем легирования металлов, таких как Cu и Fe [93,94,95, 96], и неметаллов, таких как B, C, O или S [97,98,99,100], и совместного легирования [ 101,102,103] широко используется многими учеными для очистки воды и окружающей среды. Многообещающим решением проблемы удаления загрязнений из окружающей среды [104,105,106] является комбинация благородных металлов и g-C 3 N 4 [107,108,109,110,111,112].
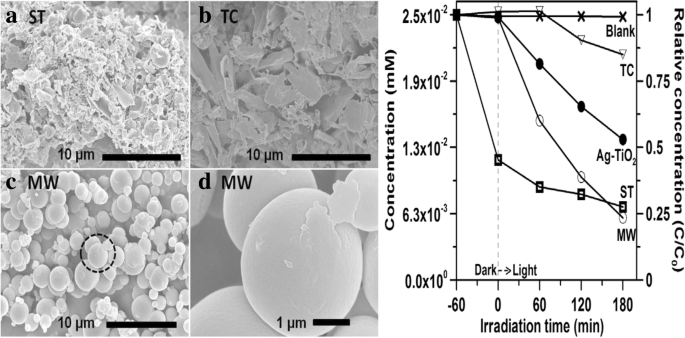
СЭМ-изображения образцов (а) ST, (b) термической конденсации (TC) и (c) микроволнового синтеза (MW); (d) увеличение образца MW; Фотокаталитическая деструкция раствора МО на образцах MW, ST, TC C3N4 и Ag-TiO2, облученных видимым светом. В эксперименте был проведен холостой тест, в котором раствор облучали без добавления катализатора. Воспроизведено с разрешения [125]. Авторские права, 2017 г., Elsevier
Таким образом, невозможность применения в сточных водах и загрязнении окружающей среды большинства хорошо подготовленных фотокатализаторов объясняется некоторыми из их сдерживающих факторов, включая высокую стоимость, малый масштаб, небольшую фотокаталитическую активность и заставляющую задуматься переработку. Разумно, что в области восстановления окружающей среды g-C 3 N 4 , TiO 2 - и наноматериалы на основе ZnO имеют наиболее многообещающее применение благодаря их низкой стоимости, высокой фотокаталитической активности и отсутствию вторичного загрязнения окружающей среды [3].
Биомедицинские и сенсорные приложения
Для увеличения способности g-C 3 N 4 Для использования зондирования, биотерапии и биовизуализации необходимо изменить молекулярную структуру, тем самым улучшив работу с материалом в воде. Из-за легкой фотолюминесценции, настоятельно рекомендуется для использования в биологических целях, g-C 3 N 4 наноматериал - очень важный кандидат для биомедицинских и сенсорных приложений. Применение g-C 3 N 4 для зондирования, биотерапии и биовизуализации в основном учитывает его структуру, синтез и препаративные механизмы. Чжан с соавторами [53] предположили, что ультратонкие нанолисты g-C3N4 могут быть использованы в качестве биомаркеров для маркировки клеточных мембран. g-C 3 N 4 был также предложен Лином и компанией. стать потенциальными фотосенсибилизаторами и pH-чувствительными лекарственными наноносителями для визуализации и терапии рака.
Перспективы на будущее
Исходя из обсуждения, будущие исследования соединения на основе g-C3N4 могут быть сосредоточены на синтезе инновационных частиц на основе наночастиц g-C3N4, которые реагируют на мониторинг морфологии, оценку практичности фотокатализа и эффективности традиционного синтеза и препаративных стратегий g- Соединение на основе наночастиц C3N4, а затем изучение применения различных частиц на основе наночастиц g-C3N4 в очистке промышленных сточных вод, их эффективное применение при использовании солнечной энергии, очистке окружающей среды, биомедицинских и сенсорных приложениях путем полной оценки их фотокаталитической способности, стоимости, энергии потребление и возможность повторного использования.
Выводы
В заключение, этот мини-обзор представляет собой кульминацию текущих достижений в области структуры и методов приготовления полнотелого g-C 3 N 4 наноразмерный материал. Понятно, что g-C 3 N 4 продемонстрировал, что является одним из наиболее благоприятных участников, подходящих для разработки схем и сборки инновационных композитных фотокатализаторов. Таким образом, нет уверенности в том, что массовое продвижение g-C 3 N 4 наночастицы будут развиваться в ближайшем будущем. В связи с этим необходимы дополнительные исследования, чтобы в полной мере использовать исключительную структуру, синтез, свойства и методы получения g-C 3 N 4 наночастицы.
Сокращения
- g-C 3 N 4 :
-
Графитовый нитрид углерода
- TiO 2 :
-
Оксид титана
- ZnO:
-
Оксид цинка
Наноматериалы
- 10 основных свойств алюминия и его применения
- Оксид гафния, его структура и применение
- Свойства композитов на основе смол и волокон и почему они полезны
- Каковы области применения и свойства марганцевой стали?
- Получение и магнитные свойства легированных кобальтом наночастиц шпинели FeMn2O4
- Раскрытие атомной и электронной структуры углеродных нановолокон с набором чашек
- Наножидкости TiO2 - Часть 1:Приготовление и свойства
- Графен и полимерные композиты для суперконденсаторов:обзор
- Влияние воды на структуру и диэлектрические свойства микрокристаллической и наноцеллюлозы
- Получение наноструктуры Au @ TiO2 - оболочка и ее применение для разложения и обнаружения метиленового синего



