Исследование из первых принципов адсорбционного поведения малых молекул на пента-графене
Аннотация
Поведение малых молекул CO, H 2 при адсорбции газа О, Н 2 S, NH 3 , SO 2 , и NO на чистом пента-графене (PG) были исследованы с использованием расчетов из первых принципов, чтобы изучить их потенциал для использования в качестве передовых газочувствительных материалов. Результаты показывают, что, за исключением CO, H 2 О, Н 2 S, NH 3 , и SO 2 физически адсорбируются на поверхности пента-графена со значительной энергией адсорбции и умеренным переносом заряда, в то время как NO склонен к химической адсорбции на поверхности пента-графена. Более того, электронные свойства PG могут быть эффективно изменены после H 2 О, Н 2 S, NH 3 , SO 2 , и NO адсорбируются, а пента-графен может использоваться в газовых сенсорах через механизм переноса заряда.
Фон
Зондирование газов, особенно загрязненных или токсичных газов, всегда было в центре внимания исследований, связанных с приложениями в областях мониторинга загрязнения окружающей среды, промышленного контроля, сельскохозяйственного производства и медицинской диагностики [1]. В последнее время предсказывается и синтезируется все больше двумерных материалов [2,3,4]. Двумерные материалы широко исследуются и используются в качестве газочувствительных элементов, поскольку они демонстрируют удивительные свойства, такие как большая площадь поверхности, сверхвысокая подвижность носителей и низкий электрический шум [5]. Сообщалось, что электронные свойства двумерных материалов могут измениться после того, как на них адсорбируются определенные молекулы газа [6, 7].
Среди двумерных материалов особенно привлекают внимание графен и его аналоги благодаря своим замечательным физическим свойствам и потенциалу для применения как в наноэлектронике, так и в наномеханике [8,9,10,11,12]. Хотя графен широко считается одним из наиболее подходящих материалов-хозяев для электронных устройств следующего поколения [13], стабильный sp 2 гибридизация углеродных связей и отсутствие зазора делают его неэффективным для адсорбции газа, что является невыгодным для конструкции газовых датчиков. Более того, графен - это проводник, обладающий отличной электропроводностью [8]. По сравнению с полупроводниками трудно измерить информацию о сопротивлении в процессе адсорбции газа, а графен нечувствителен к изменениям концентрации газов. Таким образом, графен должен быть функционализирован, чтобы открывать запрещенную зону и действовать как полупроводник [10]. В целях ограничения экспериментальных характеристик, адсорбционное поведение молекул на поверхности графена широко исследовалось с помощью расчетов из первых принципов, которые имеют значение для применения графена [14,15,16].
Пента-графен (PG), который может отслаиваться от объемного углерода T12, является одним из самых недавно предложенных аллотропов графена и состоит из повторяющихся углеродных пятиугольных структур [17]. Некоторые исследования предсказывают, что PG устойчива при фиксированных постоянных решетки [17, 18]. Он имеет сотовую структуру и является перспективным безметалловым недорогим катализатором низкотемпературного окисления CO [19]. PG, допированный азотом, проявляет очень высокую каталитическую активность и более конкурентоспособен со многими катализаторами на основе металлов и углерода для низкотемпературного окисления CO из-за очень малого энергетического барьера на стадии ограничения скорости [20]. Также сообщалось, что PG, легированный переходными металлами, является потенциальным материалом для хранения водорода [21]. Кроме того, в отличие от графена, PG представляет собой собственный полупроводник с квазипрямой запрещенной зоной с шириной запрещенной зоны в диапазоне 1,52–4,48 эВ [8, 17, 22], что подразумевает огромный потенциал для применения в полупроводниковых газовых сенсорах. Кроме того, PG имеет уникальную гибридную структуру связи, содержащую как sp 3 и sp 2 углеродные связи. Благодаря тетраэдрическому характеру sp 3 В результате гибридизации углеродных связей PG не является идеально плоским, а скорее колеблется вне плоскости в виде периодических гофрированных форм [17], указывая на большее количество возможных положений для адсорбции газа в качестве чувствительного элемента.
До настоящего времени исследования взаимодействия малых молекул газа с первичными ПГ были немногочисленны. Из-за ограничений экспериментальных методов в этом исследовании были проведены расчеты по теории функционала плотности (DFT) для исследования адсорбционного поведения малых молекул газа (т. Е. CO, H 2 О, Н 2 S, NH 3 , SO 2 , и NO) на новом углеродном материале PG. Это исследование поможет работникам анализировать и прогнозировать характеристики PG, применяемого в датчиках газа.
Методы
В этом исследовании расчеты структурных оптимизаций были выполнены расчетами из первых принципов на основе DFT [23], реализованного в Dmol 3 код [24]. Предполагается, что приближение локальной плотности (LDA) подходит для изучения систем газ-молекула-адсорбция [25, 26], и LDA-PWC был выбран для структурной оптимизации в этом исследовании. Чтобы избежать пренебрежения ван-дер-ваальсовыми взаимодействиями при изучении адсорбции молекул газа, был использован метод Ортмана, Бехстедта и Шмидта [27]. Сетка Монкхорста-Пак 2 × 2 × 1 [28] использовалась для интеграции зоны Бриллюэна, в которой допуск самосогласованного поля был установлен как 1 × 10 - 5 Ха. Система достигнет основного состояния, когда точность схождения энергии для максимального изменения энергии, максимальной силы и максимального смещения будет 1 × 10 - 5 Ha, 0,002 Ha / Å и 0,005 Å соответственно. Были проведены многоядерные параллельные вычисления [29], и при расчетах адсорбции NO использовалась спиновая поляризация. Сверхъячейка 3 × 3 с вакуумным пространством 30 Å [21] была смоделирована на основе элементарной ячейки, содержащей два sp 3 -гибридизированный атом углерода (C1) и четыре sp 2 -гибридизованные атомы углерода (C2) [17], см. рис. 1, где атомы C1 и C2 выделены черными и серыми сферами соответственно. Молекулы газа располагались горизонтально к подложке на начальном расстоянии 3,5 Å. Чтобы получить наиболее благоприятные позиции адсорбции молекул газа, были исследованы четыре возможных места, а именно вершина атома C1 (T1), вершина атома C2 (T2), середина канавок в PG (T 3 ), и противоположное положение T 2 (Т 4 ), как показано на рис. 1.
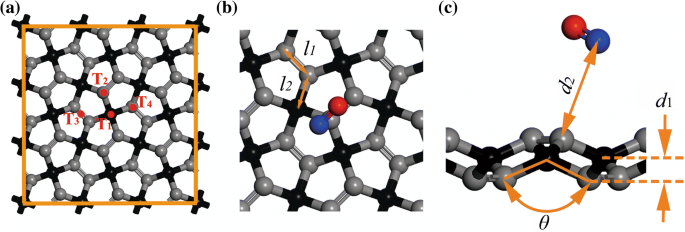
Структура и геометрия ПГ: а 3 × 3 суперячейка, b вид спереди на элементарную ячейку и c вид сбоку на адсорбат-атомы ПГ. Расстояние между двумя атомами C2, расстояние между атомами C1 и C2, толщина PG и ангел C2-C1-C2 определяются как l 1 , l 2 , d 1 , и θ соответственно
Чтобы количественно оценить адсорбционную способность системы, помимо LDA-PWC, энергия адсорбции ( E а ), перенос заряда ( Q ) и расстояние адсорбции ( d 2 , как показано на рис. 1), были рассчитаны с использованием функционалов обобщенного приближения градиента (GGA) с помощью Perdew-Wang 1991 (PW91) и Perdew-Burke-Ernzerh (PBE) в исследовании. г 2 определяется как ближайшее атомное расстояние между PG и молекулой газа в равновесном состоянии. Q обозначает заряд по Малликену молекулы газа [30, 31], а отрицательное значение означает перенос заряда от PG к молекуле газа. Энергия адсорбции рассчитывается
$$ {E} _a \ kern0.5em =\ kern0.5em {E} _ {\ left (\ mathrm {PG} \ kern0.5em + \ kern0.5em \ mathrm {молекула} \ right)} \ kern0.5em - \ kern0.5em {E} _ {\ mathrm {PG}} \ kern0.5em - \ kern0.5em {E} _ {\ mathrm {молекула}}, $$ (1)где E (молекула PG +) , E PG , и E молекула - полные энергии равновесной системы адсорбат-ПГ, изолированного ПГ и изолированной молекулы газа соответственно. При расчетах электронной структуры адсорбционных систем расчеты DFT с использованием обменно-корреляционного функционала PBE с GGA были использованы для более высокой точности [2, 32].
Результаты и обсуждение
После структурной оптимизации расчетные структурные параметры первичного PG, представленные в этой статье ( l 1 =1,342 Å, l 2 =1,551 Å, θ =133,9 °, d 1 =0,612 Å) согласуются с результатами предыдущей работы [17]. Выбрав самый низкий E (молекула PG +) или E а в четырех позициях адсорбции T 1 в Т 4 (см. Таблицу S1 Дополнительного файла 1), наиболее благоприятные конфигурации адсорбции для газов на монослое PG показаны на рис. 2, а наиболее благоприятные позиции адсорбции (т.е. T 1 , Т 2 , Т 3 , или Т 4 ) перечислены в таблице 1. Результаты расчетов в нижеследующем тексте получены на основе этих наиболее благоприятных конфигураций адсорбции. Недавние исследования показали, что монослой InSe, графен и синий фосфор имеют большие перспективы для использования в газовых сенсорах [14, 33, 34]. В настоящем исследовании рассчитанное E а значения CO, H 2 O и NH 3 составляют –0,531, –0,900 и –1,069 эВ (см. табл. 1) соответственно, а для InSe - 0,120, –0,173 и –0,185 эВ соответственно [33]. Для CO, H 2 О, NH 3 , и NO на поверхности графена, рассчитанное E а значения составляют -0,014, -0,047, -0,031 и -0,029 эВ соответственно [14]. Между тем, E а значения для H 2 S и SO 2 газы на PG составляют - 1,345 и - 1,212 эВ соответственно, что намного больше, чем - 0,14 и - 0,20 эВ соответственно для голубого фосфора [34]. Очевидно, что рассчитанное E а Значения этих газовых молекул на PG намного больше, чем полученные из других материалов, что указывает на то, что эти газовые молекулы легко адсорбируются на поверхности PG [35]. Учитывая, что рассчитанное E а значение CO намного меньше, чем у других газов, адсорбция CO может быть самой слабой. Между тем, энергия адсорбции NO в таблице 1 меньше, чем у некоторых из этих физадсорбированных (нековалентных) адсорбатов, таких как H 2 S, NH 3 , и SO 2 . Это можно объяснить тем, что, в отличие от физической адсорбции, химическая адсорбция NO вызывает явную деформацию PG, которая потребляет дополнительную энергию и снижает расчетную энергию адсорбции E а , как представлено в дополнительном файле 1. Аналогичным образом очевидная деформация также может наблюдаться при химической адсорбции NO 2 на поверхности сурьмы [5], что может привести к относительно низкой энергии адсорбции. Кроме того, кроме NO, значения d 2 перечисленные в таблице 1, очевидно, больше суммы ковалентных радиусов соответствующего атома в молекуле газа и атома C в PG (т.е. l C-O =1,38 Å, l C-H =1,07 Å, l C-N =1,46 Å, l C-S =1,78 Å) [36], показывая, что эти газовые молекулы имеют тенденцию к физической адсорбции. Что касается НЕТ, значение d 2 в адсорбционной системе составляет 1,541 Å, что находится в диапазоне ковалентных связей, что указывает на то, что в этом случае могут существовать химические связи.
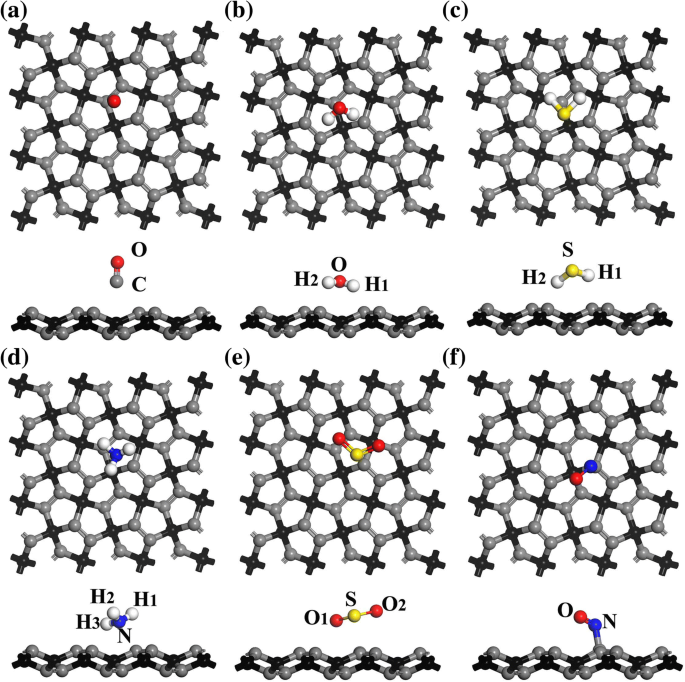
Виды сверху и сбоку наиболее подходящих конфигураций адсорбции для a CO, b H 2 O, c H 2 S, d NH 3 , e SO 2 , и f НЕТ на PG. Серые, красные, белые, желтые и синие сферы представляют собой атомы C, O, H, S и N соответственно
Предыдущие исследования InSe и фосфида бора показали, что адсорбированные молекулы изменяют удельное сопротивление подложки, действуя как акцепторы или доноры заряда [33, 37]. Q значения для CO, H 2 О, Н 2 S, NH 3 , SO 2 , и NO на поверхности PG составляют 0,023, 0,082, 0,133, 0,169, - 0,109 и - 0,03 э (см. Таблицу 1), соответственно, что указывает на то, что газы CO, H 2 О, Н 2 S и NH 3 жертвовать электроны PG, пока SO 2 и NO получают электроны от PG. Стоит отметить, что Q значения CO, H 2 О, NH 3 , и NO на поверхности InSe составляют 0,006, 0,014, - 0,025 и 0,018 э соответственно [33], а для CO, H 2 О, NH 3 , а NO на поверхности графена равны 0,012, - 0,025, 0,027 и 0,018 э соответственно [14], что указывает на то, что усиление или потеря электронов молекулами газа на PG более очевидно, чем на InSe и графене. Более того, хотя между NO и PG может происходить химическая адсорбция, перенос заряда составляет всего -0,030 э. Это можно объяснить тем фактом, что распределение заряда по Малликену для атомов N и O сильно различается (см. Таблицу S2 в Дополнительном файле 1) до и после химической адсорбции. Электроны усиления атома O компенсируют потерю электронов атома N, в результате чего общий перенос заряда NO невелик, в то время как взаимодействие электронов между NO и PG все еще очевидно. Согласно механизму восприятия переноса заряда небольших молекул газа на поверхности InSe и InN [33, 38], предполагается, что PG может иметь большой потенциал для использования в газовых сенсорах, основанных на механизме переноса заряда.>
Кроме того, расчеты адсорбции газа на PG также были выполнены с использованием двух функционалов GGA, PW91 и PBE. Расчетные значения E а , Q , и d для молекул газа на PG приведены в таблице 2. Значения E а значения, рассчитанные PW91 и PBE, меньше, чем рассчитанные LDA, тогда как PW91 и PBE дают больший d 2 по сравнению с LDA. В отличие от LDA, GGA обычно имеет тенденцию недооценивать энергию адсорбции и переоценивать расстояние связи, что согласуется с результатами предыдущих работ [26, 31]. Стоит отметить, что тенденции результатов этих трех функционалов согласуются. Например, рассчитанные значения E а CO являются наименьшими, а расчетные значения E а из H 2 S и SO 2 больше, чем у других молекул газа. Кроме того, рассчитанные значения d 2 NO для функционалов LDA, PW91 и PBE составляют 1,514, 1,592 и 1,591 Å, соответственно, которые все находятся в диапазоне ковалентных связей [36].
Чтобы лучше понять влияние молекул газа на электронные свойства PG, была рассчитана плотность состояний (DOS) системы молекула-PG, см. Рис. 3. Очевидно, вблизи уровня Ферми ( E f , например, в диапазоне от - 2,5 до 2,5 эВ) очевидны вклады электронных уровней H 2 О, Н 2 S, NH 3 , SO 2 , и NO в адсорбционные системы, что указывает на то, что существование этих газовых молекул может иметь большое влияние на электронные свойства PG [5, 37]. Например, для H 2 S, очевидный вклад электронных уровней находится при 0 эВ; см. рис. 3c. Что касается CO на поверхности PG, орбитальные пики CO в адсорбционной системе расположены при -8,0, -5,7, -2,9 и 4,0 эВ, и нет очевидного орбитального вклада вблизи E f . Кроме того, запрещенная зона также является критическим фактором при определении электронных свойств материалов [26, 34].
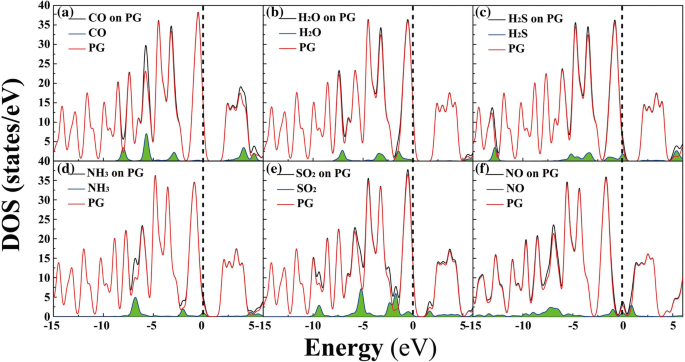
Полная плотность электронных состояний (DOS) для систем молекула-PG (черный) и прогнозируемая DOS для малых молекул (синяя линия с зеленой тенью) и PG (красный) в адсорбционной системе: a CO, b H 2 O, c H 2 S, d NH 3 , e SO 2 , и f НЕТ. Уровень Ферми установлен на ноль (см. Пунктирную линию)
Ширина запрещенной зоны и соответствующая структура зоны адсорбционных систем показаны на рис. 4, где ширина запрещенной зоны CO, H 2 О, Н 2 S, NH 3 , SO 2 , NO на PG составляют 2.15, 2.02, 1.86, 1.81, 1.61 и 0 эВ соответственно. Напротив, ширина запрещенной зоны исходного PG составляет 2,21 эВ (см. Дополнительный файл 1:Рисунок S2). Очевидно, за исключением CO, газовая адсорбция H 2 О, Н 2 S, NH 3 , SO 2 , и NO имеют очевидное влияние на электронные свойства PG, и это согласуется с результатами DOS. Все эти результаты могут указывать на то, что, за исключением CO, электронные свойства PG могут быть эффективно изменены после H 2 О, Н 2 S, NH 3 , SO 2 , и NO адсорбируются, что очень важно для обнаружения газов.
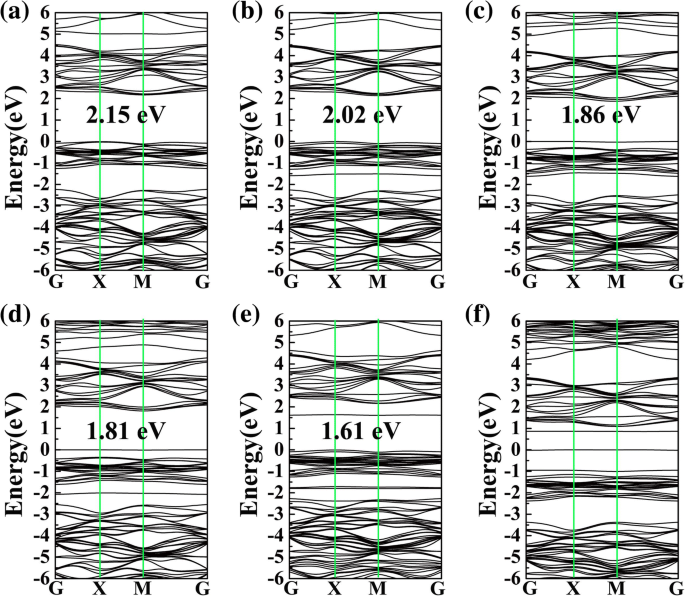
Ленточные структуры СО ( а ), H 2 O ( b ), H 2 S ( c ), NH 3 ( д ), SO 2 ( е ) и НЕТ ( f ) на поверхности PG
Учитывая, что d 2 значение NO на PG находится в диапазоне связывания, и что электронные уровни NO в системе в основном локализуются около E f , предполагается, что происходит химическая адсорбция. Для более глубокого понимания механизма адсорбции между NO и PG, прогнозируемая плотность состояний (PDOS) NO на PG и функция локализации электронов (ELF) показаны на рис. 5. Ясно, что пики PDOS N <я> р и O p атомы в основном расположены при –6.9, –0.9, 0 и 0.8 эВ; таким образом, в NO происходит внутримолекулярная гибридизация, как показано на рис. 5а. Между тем, можно наблюдать орбитальное перемешивание между NO и атомом C PG вблизи уровня Ферми, которое в основном вносится за счет C s , С p , N с , Н п , и O p орбитали. Орбитальное смешение индуцирует химическую связь между N в NO и C в PG, как показано на рис. 5b; таким образом, PG можно использовать для обнаружения или катализирования газа NO [5, 39]. Кроме того, чтобы подтвердить тип адсорбции других молекул газа, также рассчитываются КНЧ других адсорбционных систем, см. Дополнительный файл 1:Рисунок S3. Очевидно, что для CO H 2 О, Н 2 S, NH 3 и SO 2 , между молекулами газа и субстратом отсутствуют химические связи, что указывает на тенденцию к физической адсорбции в этих системах.
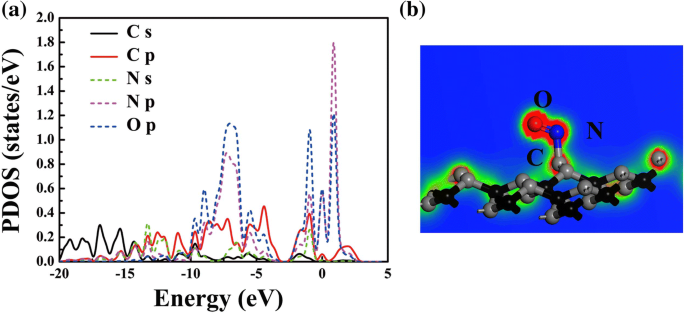
Атом спроектировал DOS ( a ) и функция локализации электронов (ELF) NO-PG ( b )
Выводы
Таким образом, H 2 О, Н 2 S, NH 3 , и SO 2 газы физически адсорбируются на монослое PG со значительной энергией адсорбции и умеренным переносом заряда. При слабой физической адсорбции, небольшой энергии адсорбции и переносе заряда чистый PG не подходит для обнаружения CO. Для этих молекул газа на поверхности PG, CO, H 2 O и H 2 S и NH 3 жертвовать электроны PG, а SO 2 и NO получают электроны от PG. Более того, вблизи уровня Ферми очевидны вклады электронных уровней H 2 О, Н 2 S, NH 3 , SO 2 и NO для DOS адсорбционных систем, указывая на то, что электронные свойства PG могут быть эффективно изменены после H 2 О, Н 2 S, NH 3 , SO 2 , и NO адсорбируются. Кроме того, адсорбция NO на PG показывает сильную тенденцию к химической адсорбции, и, таким образом, PG можно использовать для обнаружения или катализа газообразного NO. Таким образом, Pristine PG имеет большой потенциал в области обнаружения газов.
Сокращения
- 2D:
-
Двумерный
- DFT:
-
Функциональная теория плотности
- DOS:
-
Плотность состояний
- ELF:
-
Функция электронной локализации
- GGA:
-
Обобщенное приближение градиента
- LDA:
-
Приближение локальной плотности
- PBE:
-
Пердью – Берк – Эрнцерх
- PDOS:
-
Прогнозируемая плотность состояний
- PG:
-
Пента-графен
- PW91:
-
Пердью-Ван 1991
- PWC:
-
Корреляционная связь Пердью – Ванга
Наноматериалы



