Низкий туннельный распад соединений одной молекулы алкана с концевым йодом
Аннотация
Одним из ключевых вопросов при разработке молекулярных электронных устройств является понимание переноса электронов в переходах одиночных молекул. В этой работе мы исследуем перенос электронов в одиночных молекулярных соединениях алканов с йодными концевыми группами, используя метод разрыва соединений на основе сканирующего туннельного микроскопа. Результат показывает, что проводимость экспоненциально уменьшается с увеличением длины молекулы с константой распада β . N =0,5 на –CH 2 (или 4 нм −1 ). Важно отметить, что туннельный распад этих молекулярных контактов намного ниже, чем у молекул алкана с тиолом, амином и карбоновой кислотой в качестве якорных групп, и даже сравним с таковым у конъюгированных молекул олигофенила. Низкий туннельный распад объясняется небольшой высотой барьера между молекулой алкана с концевыми йодными группами и Au, что хорошо подтверждается расчетами методом DFT. Работа предполагает, что туннельный распад может быть эффективно настроен группой закрепления, которая может управлять производством молекулярных проводов.
Фон
Понимание электронного транспорта в переходах одиночных молекул имеет решающее значение для разработки молекулярных электронных устройств [1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16 ]. Модель нерезонансного туннелирования часто использовалась для описания процесса переноса электронов через небольшую молекулу, где основными параметрами являются контактная проводимость, длина молекулы и константа туннельного распада [17, 18]. В большинстве молекулярных систем константа распада тесно связана с электронными свойствами органического скелета. Например, сопряженные молекулярные системы имеют низкий туннельный распад, в отличие от несопряженных [17, 19]. Поскольку туннельный распад определяется высотой барьера между уровнем Ферми электрода и самой низкой незанятой молекулярной орбиталью (НСМО) или самой высокой занятой молекулярной орбиталью (ВЗМО) молекулярных контактов [17, 20], можно настроить уровень энергии молекулы ближе к уровню Ферми, чтобы добиться низкого затухания [21,22,23,24].
В соединениях одиночных молекул якорная группа играет важную роль в контроле электронного взаимодействия между органическими скелетами и электродами [21, 23, 24, 25]. Серия измерений проводимости для молекул на основе алканов показала значительное влияние различных якорных групп на геометрию связывания, вероятность образования контактов, контактную проводимость и даже канал проводимости (через НСМО или ВЗМО) молекулярных контактов [21,22, 23,24,25]. Поскольку якорная группа может регулировать граничные орбитали в молекулярном соединении, туннельный распад молекулы также может регулироваться якорной группой [24]. Однако в этой области было проведено ограниченное исследование.
Здесь мы сообщаем о переносе электронов молекулами алканов, оканчивающихся йодной группой, с использованием разрывных контактов сканирующей туннельной микроскопии (STM-BJ) (рис. 1) [26, 27]. Измерения одиночной молекулярной проводимости показывают, что проводимость экспоненциально уменьшается с увеличением длины молекулы, а константа распада молекул алкана с йодной группой намного ниже, чем у аналогов с другими якорными группами. Различные константы туннельного распада для молекул алкана с различными якорными группами объясняются высотой барьера между молекулой и электродом.
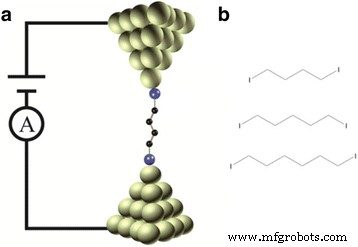
Принципиальная схема сканирующей туннельной микроскопии break junction (STM-BJ) и молекулярных структур. а Схема STM-BJ с молекулярным переходом. б Молекулярные структуры молекул алкан-йода
Методы
1,4-Бутандиодо, 1,5-пентандиодо и 1,6-гександиодо были закуплены у Alfa Aesar. Все растворы готовили на этаноле. В качестве подложки использовалось золото (111), а в качестве наконечников - наконечники из золота, нарезанные механическим способом. Перед каждым экспериментом Au (111) подвергался электрохимической полировке и осторожному отжигу в бутановом пламени, а затем сушился азотом.
Подложку Au (111) погружали в свежеприготовленный раствор этанола, содержащий 0,1 мМ целевых молекул, на 10 мин. Измерение проводимости проводилось на модифицированном Nanoscope IIIa STM (Veeco, США) с использованием метода STM-BJ при комнатной температуре [28,29,30], который просто измерял проводимость переходов одиночных молекул, образованных многократным перемещением наконечник внутрь и наружу с постоянной скоростью. Во время этого процесса молекулы могли закрепиться между двумя металлическими электродами и образовать единые молекулярные соединения. Для статистического анализа собраны тысячи таких кривых. Все эксперименты проводились при фиксированном напряжении смещения 100 мВ. Поскольку молекулы с йодом в качестве закрепляющей группы являются светочувствительным материалом, эксперимент проводился в режиме затенения.
Результаты и обсуждение
Измерение проводимости одиночных молекулярных соединений алкана с йодной группой
Впервые измерения проводимости были выполнены на Au (111) с монослоем 1,4-бутандиодо с помощью STM-BJ. На рис. 2а приведены типичные кривые проводимости, демонстрирующие ступенчатый характер. Кривые проводимости показывают плато при 1 G 0 , что свидетельствует об образовании стабильного атомного контакта Au. Плато при значении проводимости 10 −3,6 G 0 (19,47 нс) также встречается помимо 1 G 0 , за счет образования молекулярного стыка. Гистограмма проводимости также может быть получена путем обработки логарифмом и биннированием значения проводимости для более чем 3000 трасс проводимости, а затем интенсивность гистограммы проводимости была нормализована по количеству используемых трасс и показывает пик проводимости при 10 - 3.6 G 0 (19,44 нс) (рис. 2б). Они показывают, что группа йода может служить в качестве эффективной закрепляющей группы, образующей молекулярные соединения. Однако это значение меньше, чем значение одиночной молекулярной проводимости 1,4-бутандиамина с амином в качестве закрепляющей группы, что может быть связано со слабым взаимодействием между йодом и Au-электродом [31].
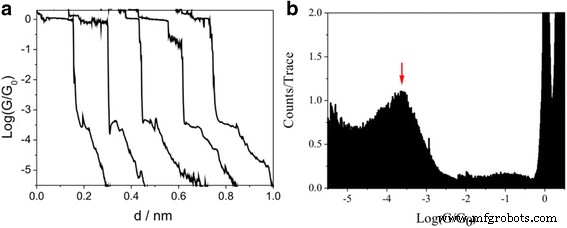
Одномолекулярная проводимость переходов Au – 1,4-бутандиод – Au. а Типичные кривые проводимости переходов Au – 1,4-бутандиод – Au, измеренные при смещении 100 мВ. б Гистограмма проводимости 1,4-бутандиодо контактов с контактами Au
По сравнению с 1,4-дииодбутаном, выраженные пики при 10 −3,8 G 0 (12,28 нс) и 10 −4,0 G 0 (7,75 нс) обнаружены для 1,5-пентандиодо и 1,6-гександиодо, соответственно (рис. 3). Значения проводимости уменьшаются с увеличением длины молекулы. Между тем, значения проводимости 1,5-пентандио и 1,6-гександиодо меньше, чем у 1,5-пентандиамина и 1,6-гександиамина соответственно [31], что может быть вызвано различным взаимодействием в алкандиамине. на основе молекулярных переходов между йодом и аминовыми якорными группами, связывающимися с золотыми электродами [32].
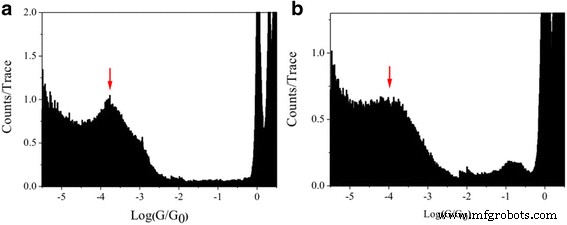
Одномолекулярная проводимость 1,5-пентандиод и 1,6-гександиодо с Au электродом. Гистограмма проводимости в логарифмическом масштабе отдельных молекулярных переходов с a 1,5-пентандиодо и b 1,6-гександиодо
Двумерные гистограммы проводимости также были построены для этих молекулярных переходов (дополнительный файл 1:рисунок S1) и выдают аналогичные значения проводимости одномерных гистограмм. Обычно расстояние отрыва молекулярных стыков увеличивается с увеличением длины молекулы. Мы также анализируем расстояние от значения проводимости 10 −5.0 G 0 до 10 −0,3 G 0 как показано на рис. 4, и расстояния разрыва 0,1, 0,2 и 0,3 нм найдены для 1,4-бутандиодо, 1,5-пентандиодо и 1,6-гександиодо, соответственно. Здесь расстояния разрыва получены из максимального пика гистограммы расстояний разрыва [33]. Сообщалось, что после разрыва контакта Au – Au существует расстояние возврата 0,5 нм для Au [34, 35]; таким образом, абсолютные расстояния для этих молекулярных переходов между электродами могут составлять 0,6, 0,7 и 0,8 нм, которые обнаружены для 1,4-бутандиодо, 1,5-пентандиодо и 1,6-гександиодо, соответственно. Эти расстояния сопоставимы с длиной молекул. Eder et al. сообщили, что адсорбция монослоя 1,3,5-три (4-иодофенил) бензола на Au (111) может вызвать частичное дегалогенирование [36]; однако гораздо большее значение проводимости для этих ковалентных контактных молекулярных переходов Au – C можно найти для молекул с четырьмя (около 10 −1 G 0 ) и шесть (больше 10 −2 G 0 ) –CH 2 - единицы [37]. Таким образом, мы предлагаем, чтобы текущие исследуемые молекулы контактировали с Au через контакт Au – I.
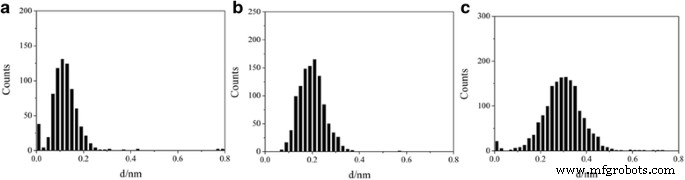
Расстояния разрыва для алканов с концевыми йодными группами. Разрывные дистанции а 1,4-бутандиод, b 1,5-пентандиодо и c 1,6-гександиодо получено из кривых проводимости между 10 -5,0 G 0 и 10 −0,3 G 0
Константа туннельного затухания одиночных молекулярных соединений алкана с концевыми йодными группами
При текущем смещении проводимость этих молекул можно выразить как G = G c ехр (- β N N ). Здесь G - проводимость молекулы и G c - контактная проводимость, определяемая взаимодействием между анкерной группой и электродом. N - метиленовое число в молекуле, а β N - константа туннельного распада, которая отражает эффективность связи электронного транспорта между молекулой и электродом. Как показано на рис. 5, мы построили шкалу натурального логарифма проводимости в зависимости от количества метилена; константа туннельного затухания β N 0,5 на –CH 2 определяется по наклону линейного фитинга. Этот туннельный распад очень невелик в молекулах на основе алканов. Для молекул на основе алканов β N обычно находится около 1,0 на –CH 2 для тиола (SH) [23, 38], в то время как около 0,9 и 0,8 на –CH 2 определены для амина (NH 2 ) [23, 31] и карбоновая кислота (COOH) соответственно [39]. Таким образом, туннельный распад с йодом показывает самое низкое значение среди тех якорных групп с трендом β N (тиол)> β N (амин)> β N (карбоновая кислота)> β N (йод), что может быть связано с различием в выравнивании энергетических уровней молекул относительно уровня Ферми Au электрода [23, 31]. Туннельный распад 0,5 на –CH 2 также можно преобразовать в 4 нм −1 , что сопоставимо с олигофенилами с 3,5–5 нм -1 [40, 41].
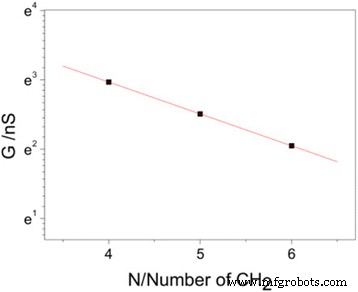
Одномолекулярная проводимость в зависимости от длины молекулы для алканов с концевыми йодными группами. Логарифмические графики зависимости проводимости одной молекулы от длины молекулы для алканов с концевыми йодными группами
β N для соединений металл-молекула-металл можно просто описать следующим уравнением [17, 20, 38],
$$ {\ beta} _N \ \ alpha \ \ sqrt [2] {\ frac {2 m \ varPhi} {h ^ 2}} $$
где м - эффективная масса электрона и 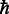 - это уменьшенная постоянная Планка. Φ представляет собой высоту барьера, которая определяется энергетической щелью между уровнем Ферми и уровнями энергии молекул в переходе. Очевидно, что β N значение пропорционально квадратному корню из высоты барьера. Таким образом, мы можем предположить, что молекулы алканов с концевыми йодными группами имеют малую величину Φ с помощью Au-электрода.
- это уменьшенная постоянная Планка. Φ представляет собой высоту барьера, которая определяется энергетической щелью между уровнем Ферми и уровнями энергии молекул в переходе. Очевидно, что β N значение пропорционально квадратному корню из высоты барьера. Таким образом, мы можем предположить, что молекулы алканов с концевыми йодными группами имеют малую величину Φ с помощью Au-электрода.
Высота барьера одиночных молекулярных соединений с разными группами якоря
Принимая - (CH 2 ) 6 - в качестве основы мы выполнили грубые расчеты (см. Детали вычислений в дополнительном файле 1) для исследования пограничных молекулярных орбиталей комплексов с четырьмя атомами Au на обоих концах, включая 1,6-гександитиол (C6DT), 1,6- гександиаминb (C6DA), 1,6-гександикарбоновая кислота (C6DC) и 1,6-гександиодо (C6DI). Как показано в таблице 1, HOMO и LUMO составляют -6,18 и -1,99 эВ, соответственно, для C6DT, в то время как HOMO (6,02 эВ) и LUMO (-1,85 эВ) найдены для C6DA. Между тем, уровни энергии HOMO и LUMO рассчитаны для C6DC (-6,33 и -2,58 эВ) и C6DI (-6,22 и -2,61 эВ).
Для уровня Ферми Au электрода необходимо учитывать влияние адсорбции молекул. В условиях вакуума чистое золото дает работу выхода 5,1 эВ [42]; Между тем, очевидно, что это значение может быть изменено за счет адсорбции молекул. Kim et al. [43] и Юань и др. [44] обнаружили, что работа выхода Au составляет около 4,2 эВ (4,0–4,4 эВ) на адсорбированных самоорганизующихся монослоях (SAM), измеренная с помощью ультрафиолетового фотоэлектронного спектрометра (UPS). Low et al. также исследовали электронный транспорт молекул TOTOT на основе тиофена (LUMO - 3,3 эВ, HOMO - 5,2 эВ) и TTO p TT (LUMO - 3,6 эВ, HOMO - 5,1 эВ) с Au в качестве электрода (T, O и O p обозначают тиофен, тиофен-1,1-диоксид и окисленный тиенопиролодион соответственно) [45]. Результаты показывают, что уровень Ферми Au находится посередине LUMO и HOMO. Таким образом, мы можем сделать вывод, что уровень Ферми Au может быть около среднего уровня энергии LUMO и HOMO, которые составляют -4,25 и -4,35 эВ, установленные с помощью TOTOT и TTO P ТТ соответственно. Уровень Ферми Au - 4,25 и - 4,35 эВ аналогичен измеренному ИБП с - 4,2 эВ [43]. В соответствии с вышеизложенным, мы будем использовать -4,2 эВ в качестве уровня Ферми Au-электрода с адсорбцией молекулы.
Предполагая, что уровень Ферми составляет -4,2 эВ для Au с SAM, C6DT и C6DA представляют собой перенос электронов с преобладанием ВЗМО, в то время как перенос электронов с преобладанием НСМО предлагается для C6DC и C6DI. Таким образом, высота барьера Φ может быть определено как 1,98 эВ (C6DT), 1,82 эВ (C6DA), 1,62 эВ (C6DC) и 1,59 эВ (C6DI) (таблица 1). Тенденция изменения высоты барьера между молекулой и Au составляет Φ C6DT (тиол)> Φ C6DA (амин)> Φ C6DC (карбоновая кислота)> Φ C6DI (йод), что согласуется с тенденцией туннельного распада ( β ). Таким образом, необычно низкий туннельный распад может быть связан с небольшой высотой барьера между молекулами алканов с концевыми йодными группами и Au.
Выводы
В заключение, мы измерили проводимость молекул на основе алканов с йодной группой, контактирующих с Au-электродами, методом STM-BJ при комнатной температуре. Туннельный распад β N 0,5 на –CH 2 был обнаружен для молекул с Au-электродами, что намного ниже, чем у молекул на основе алканов с другими якорными группами. Это может быть вызвано небольшой высотой барьера между молекулой алкана с йодной группой на конце и Au. Текущая работа показывает важную роль группы закрепления в электрических характеристиках одиночных молекулярных контактов, которые могут регулировать туннельный распад молекулярных контактов и направлять производство молекулярной проволоки.
Сокращения
- HOMO:
-
Наивысшая занятая молекулярная орбиталь
- LUMO:
-
Самая низкая незанятая молекулярная орбиталь
- SAM:
-
Самособирающиеся монослои
- STM-BJ:
-
Сканирующая туннельная микроскопия на разрыв соединения
- ИБП:
-
Ультрафиолетовая фотоэлектронная спектроскопия
Наноматериалы
- Европейский исследовательский совет финансирует исследования одномолекулярных устройств путем манипулиро…
- Поверхностный эффект на транспортировку нефти в наноканале:исследование молекулярной динамики
- Фотолюминесцентные свойства полиморфных модификаций низкомолекулярного поли (3-гексилтиофена)
- Моделирование молекулярной динамики и имитация алмазной резки церия
- Температурная зависимость ширины запрещенной зоны в MoSe2, выращенном методом молекулярно-лучевой эпитаксии
- Серебряный затворный электрод с УФ-отверждением для струйной печати с низким электрическим сопротивлением
- DFB квантовые каскадные лазеры с низким энергопотреблением, излучающие субстрат
- Исследование влияния направления удара на абразивный нанометрический процесс резания с помощью молекулярно…
- Исследование фрикционного поведения графена на золотых подложках в наномасштабе с помощью молекулярной дин…
- Причины низкого коэффициента мощности



