Повышение селективности амперометрического преобразователя с использованием наноразмерных пленок фенилендиамина
Аннотация
В данной работе исследованы условия нанесения полупроницаемой мембраны на основе полифенилендиамина (ППД) на амперометрические дисковые платиновые электроды. Ограничивая доступ мешающих веществ к поверхности электрода, мембрана предотвращает их влияние на работу датчика. Сравнивались два метода осаждения мембран электрополимеризацией - при переменном потенциале (циклическая вольтамперометрия) и при постоянном потенциале. Было показано, что циклическая вольтамперометрия проще в выполнении и обеспечивает лучшие свойства мембраны. Проанализирована зависимость эффективности мембраны ППД от количества циклических вольтамперограмм и концентрации фенилендиамина. Показано, что воздействия мешающих веществ (аскорбиновая кислота, дофамин, цистеин, мочевая кислота) на работу сенсора можно полностью избежать с помощью трех циклических вольтамперограмм в 30 мМ фенилендиамине. С другой стороны, при работе с разбавленными образцами, то есть при более низких концентрациях электроактивных веществ, целесообразно снизить концентрацию фенилендиамина до 5 мМ, что приведет к более высокой чувствительности преобразователей к перекиси водорода за счет более тонкого слоя PPD. . Мембрана PPD была протестирована при непрерывной работе и при хранении в течение 8 дней и оказалась эффективной в сенсоре и биосенсорах.
Фон
Биосенсоры - это новые аналитические устройства; использование которых является альтернативой хроматографии, спектроскопии и колориметрии. Биосенсоры намного дешевле и проще в использовании, чем эти традиционные методы, однако часто уступают им по аналитическим характеристикам. В настоящее время активно ведутся исследования в области биосенсорики [1].
Согласно классическому определению Международной ассоциации исследователей фундаментальной и прикладной химии, биосенсор - это интегрированное устройство на основе рецептора и преобразователя, способное проводить количественный или полуколичественный анализ с использованием элемента биологического распознавания [2]. По типу преобразователя биосенсоры делятся на несколько групп (электрохимические, оптические, пьезоэлектрические и т. Д.), Среди которых электрохимические биосенсоры являются одной из самых больших групп и, в свою очередь, делятся на амперометрические, потенциометрические, кондуктометрические и импедиметрические [3]. .
Одной из важных аналитических характеристик биосенсоров является их избирательность, то есть способность идентифицировать только целевое соединение. Селективность биосенсора определяется селективностью биологического материала и селективностью преобразователя. В основном ферменты и антитела, используемые в электрохимических биосенсорах в качестве биоматериала, очень селективны, тогда как электроды, которые служат преобразователями, довольно неселективны. Селективность биосенсора имеет особое значение при работе с реальными биологическими жидкостями или другими сложными образцами; поэтому его исследование является необходимым этапом в разработке биосенсоров.
В сыворотке крови, моче, спинномозговой жидкости и т. Д. Присутствуют мешающие вещества, которые могут вступать в химические реакции на поверхности датчиков, что приводит к ложным результатам измерения целевого вещества биосенсором. Основными мешающими факторами в биологических образцах являются аскорбиновая кислота, цистеин, гомоцистеин, мочевая кислота, дофамин, глутатион и т. Д. Их концентрации в сыворотке крови человека показаны в таблице 1.
Существует два основных подхода к предотвращению окисления мешающих веществ на поверхности электрода - уменьшение рабочего потенциала за счет введения дополнительных веществ в биоселективную мембрану или нанесение дополнительных полупроницаемых мембран, которые обеспечивают избирательный доступ целевого вещества к поверхности электрода [ 4]. Нанесение полупроницаемых мембран методически проще и незначительно влияет на работу биосенсора.
В биосенсорах перекись водорода окисляется или восстанавливается на электроде, и, таким образом, генерируется сигнал биосенсора. Поэтому актуальной является разработка нанопористых пленок, проницаемых для перекиси водорода и препятствующих проникновению других веществ. Среди этих мембран значительное внимание привлекают полимерные пленки на основе фенилендиамина (ФД) [5]. Мембрана на основе полифенилендиамина (PPD) имеет нанопоры; их размер достаточен для проникновения низкомолекулярных соединений, в том числе перекиси водорода, через мембрану к поверхности электрода. С другой стороны, мембрана не пропускает через себя или окисляет более крупные вещества, такие как аскорбиновая кислота или дофамин. Таким образом, мембрана улучшает селективность по перекиси водорода, что, в свою очередь, увеличивает точность биосенсора. В нескольких работах были изучены различные изомеры ПД и методы полимеризации ПД. В частности, мембраны PPD формировали на покрытых рутением микроэлектродах из углеродного волокна методом электроосаждения при постоянном потенциале (+0,7 В) при создании биосенсоров на основе глюкозооксидазы, лактатоксидазы и глутаматоксидазы [6]. Были протестированы три изомера PD; результаты с мета-изомером были лучшими. Поскольку некоторая чувствительность к аскорбиновой кислоте все еще оставалась, была добавлена аскорбатоксидаза, чтобы полностью устранить ее. В [7] авторы исследовали мембраны PPD, нанесенные на цилиндры из Pt – Ir, методами CV или амперометрии с постоянным потенциалом. Чувствительность к аскорбиновой кислоте заметно снижалась при окислении мембран на основе мета- и орто-изомеров при постоянном потенциале, тогда как чувствительность к пероксиду водорода снижалась всего на 10%. Результаты, полученные с мембранами PPD, нанесенными на палладиевые дисковые электроды, сильно различались [8]. Электроосаждение м -PD путем CV вызывал образование пленок с трехкратной более высокой проницаемостью для пероксида водорода по сравнению с m -Окисление ПД при постоянном потенциале. Таким образом, m Было показано, что -PD предпочтительнее среди всех изомеров. Недавно опубликованный датчик перекиси водорода с CV-осаждением o Пленка -PD с наночастицами Au [9] продемонстрировала хорошее избегание мешающих эффектов. В целом можно сделать вывод, что m -PD превосходит другие для всех электродов, тогда как процедура полимеризации PD должна быть оптимизирована в каждом конкретном случае. Кроме того, мембраны на основе ПД могут также использоваться в датчиках без биологического элемента. Как недавно было показано, бычий сывороточный альбумин может быть обнаружен сенсором на основе конъюгированных сополимеров PD и других ароматических соединений (наблюдалось тушение флуоресценции белка после связывания с сополимером) [10].
Таким образом, целью данной работы было сравнение различных методов m -осаждение фенилендиамина и выбор оптимальной процедуры формирования ПФД на платиновых дисковых электродах.
Методы
Материалы
Аскорбиновая кислота, цистеин, мочевая кислота, дофамин, перекись водорода, м -фенилендиамин и HEPES были приобретены у Sigma-Aldrich Chemie (США). Все остальные химические вещества были из год. оценка.
Образцы сыворотки крови человека получены из Киевского городского научно-практического центра нефрологии и гемодиализа (Украина).
Дизайн амперометрических преобразователей
В данной работе самодельные платиновые дисковые электроды служили амперометрическими преобразователями. Платиновая проволока диаметром 0,4 мм и длиной 3 мм была запаяна на одном конце стеклянного капилляра с внешним диаметром 3,5 мм. Открытый конец проволоки являлся рабочей поверхностью преобразователя. Внутренний конец платиновой проволоки был припаян сплавом Вуда к одному концу серебряной проволоки внутри капилляра; другой его конец был подключен к потенциостату. Электроды использовались многократно; перед использованием их рабочая поверхность обрабатывалась HCl в течение 30 с, промывалась этанолом и шлифовалась наждачной бумагой П1500 ПС 8А.
Методы измерения
Спектры поглощения образцов в УФ и видимой областях измеряли на спектрометре Thermo Evolution 600 в диапазоне длин волн 200–900 нм в режиме диффузного отражения с использованием интегральной сферы. Стандарт диффузного отражения Spectralon и платиновый диск использовались в качестве холостых образцов для м -фенилендиаминный порошок и слой PPD на поверхности Pt электрода соответственно.
Для электрохимических измерений рабочие электроды помещали в классическую электрохимическую ячейку со вспомогательным (платиновая проволока) и эталонным (Ag / AgCl в насыщенном KCl) электродами, подключенными к потенциостату PalmSens (Palm Instruments BV, Нидерланды). Использование восьмиканального мультиплексора (от того же производителя), подключенного к потенциостату, позволило одновременно контролировать сигналы с восьми электродов; однако в своей работе мы обычно использовали три электрода из-за небольшого размера рабочей ячейки.
Хроноамперометрические измерения (метод «амперометрического детектирования») проводили при комнатной температуре в открытой стеклянной ячейке объемом 3 мл при постоянном перемешивании магнитной мешалкой и постоянном потенциале 0,6 В относительно электрода сравнения Ag / AgCl. Во всех экспериментах в качестве рабочего буфера использовали десять миллимоляров HEPES, pH 7,4. Концентрации субстрата в рабочей ячейке получали добавлением аликвот исходных растворов (50 мМ перекиси водорода, 20 мМ аскорбиновой кислоты, 3 мМ цистеина, 4,5 мМ мочевой кислоты, 2,1 мМ дофамина). Новые растворы были приготовлены непосредственно перед экспериментом. Все электроактивные вещества, кроме мочевой кислоты, растворялись в рабочем буфере; мочевая кислота из-за ее малой растворимости была растворена в дистиллированной воде с 5 мМ NaBrO 3 . Фенилендиамин растворяли в 40 мМ фосфатном буфере, pH 7,4.
Циклическую вольтамперометрию проводили в той же измерительной ячейке без перемешивания. Начальный потенциал составлял 0 В, конечный потенциал +0,9 В, скорость сканирования (скорость изменения потенциала) 20 мВ / с, а шаг изменения потенциала 5 мВ.
Все эксперименты проводились в трех повторностях. Данные в таблицах и на рисунках представляют собой среднее значение экспериментов ± стандартное отклонение, вычисленное программой OriginLab OriginPro 8.5.
Результаты и обсуждение
Чтобы подтвердить причины нанесения дополнительной мембраны на амперометрический преобразователь для повышения его селективности по перекиси водорода, необходимо было проверить чувствительность и селективность этого преобразователя в отношении возможных помех.
Биосенсоры можно использовать для измерений как неразбавленных, так и разбавленных образцов. Вариант разбавления зависит от концентрации анализируемого вещества и чувствительности биосенсора:если биосенсор может идентифицировать целевое вещество в концентрациях, которые в десятки раз ниже фактических в образцах, последнее следует разбавить, чтобы уменьшить содержание помех и, таким образом, повысить точность массива. Кроме того, он позволяет в десятки раз уменьшить объем субстрата, необходимый для измерений.
Иногда концентрация анализируемого вещества слишком мала или разведение нежелательно по техническим причинам. Для лучшего понимания функции амперометрического преобразователя использовались электроактивные материалы трех концентраций:(1) релевантные для сыворотки крови, (2) в 20 раз ниже, чем (1), т.е. 20-кратное разведение, и (3) 100- кратное разбавление. Отклики биосенсора на электроактивные вещества трех концентраций были получены с использованием неизолированного преобразователя перед нанесением пленки PPD, и была рассчитана чувствительность преобразователя (таблица 2). Как видно, чувствительность к дофамину и аскорбиновой кислоте была самой высокой, а к цистеину - самой низкой. Однако аскорбиновая и мочевая кислоты могут рассматриваться как основные мешающие факторы из-за их существенно более высоких концентраций в биологических образцах. Отклик преобразователя на эти вещества на порядок больше, чем отклик на целевое вещество - перекись водорода. Поэтому неизолированный преобразователь непригоден для измерений в биологических образцах из-за сильного воздействия помех. С другой стороны, после 100-кратного разбавления реакция на цистеин и дофамин стала незначительной, а реакция на все помехи в целом составила лишь около 20% реакции на перекись водорода, что означает, что в некоторых случаях датчик может быть используется даже без дополнительных модификаций.
В настоящее время имеется лишь фрагментарная информация о методах нанесения мембран PPD на преобразователи. Поэтому на следующем этапе работы было оценено, какой из двух наиболее распространенных и перспективных методов более осуществим.
В первом методе мембраны PPD наносили на поверхность платинового дискового электрода путем электрополимеризации молекул мономера фенилендиамина с использованием переменного потенциала (циклическая вольтамперометрия). Преобразователи с электродами сравнения и вспомогательными электродами помещали в рабочую ячейку с раствором фенилендиамина и получали ряд циклических вольтамперограмм [7]. Пример эксперимента показан на рис. 1. Во время первой циклической вольтамперограммы (ЦВА) наблюдалось значительное увеличение тока при потенциале от 0,5 до 0,9 В из-за окисления фенилендиамина. Во время второго и последующих ВАМ ток значительно снизился, что указывает на более низкую скорость электрополимеризации. Однако, как показали следующие эксперименты, образование PPD-мембраны продолжалось на протяжении всего CV.
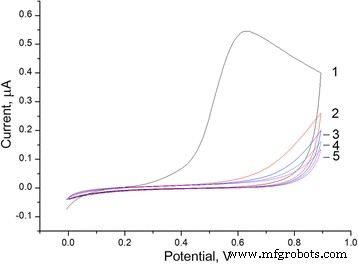
Циклические вольтамперограммы, полученные при электрополимеризации фенилендиамина на поверхности преобразователя
Второй метод осаждения мембран PPD заключается в окислении фенилендиамина при постоянном потенциале +0,7 В в течение фиксированного времени (40 мин) [11]. Сравнение откликов преобразователей при использовании обоих методов осаждения показано в таблице 3. В дальнейшем отклики на электроактивные вещества без мембраны PPD были приняты за 100%. Мембраны, нанесенные обоими методами, достаточно эффективно препятствовали интерференции - наблюдалась лишь слабая чувствительность к цистеину. С другой стороны, чувствительность преобразователя к перекиси водорода после вольтамперометрии увеличилась в 2,6 раза. Это можно объяснить электроактивацией платины во время вольтамперометрии, но не действием мембраны PPD. Такое повышение чувствительности к перекиси водорода наблюдалось также после получения циклических вольтамперограмм в фосфатном буфере без фенилендиамина. После осаждения мембраны при постоянном потенциале электроактивации не было обнаружено и реакции на перекись водорода не изменились. Таким образом, было обнаружено, что использование циклической вольтамперометрии является предпочтительным по трем причинам:меньшее время для одного осаждения (20 против 40 минут), более эффективное препятствование цистеину и увеличение реакции на перекись водорода.
Однако у циклической вольтамперометрии есть один недостаток - вольтамперограммы можно одновременно получать только на одном электроде (даже с использованием мультиплексора), тогда как осаждение через мембрану при постоянном потенциале позволяет одновременно подключать 8–16 рабочих электродов (в зависимости от типа мультиплексора). Поэтому дальнейшая работа должна быть направлена на оптимизацию условий циклических вольтамперограмм для сокращения времени предварительной обработки преобразователя.
Электрополимеризация PD с помощью CV и амперометрии с постоянным потенциалом, как предполагается, происходит разными путями через довольно сложный механизм [12]. Таким образом, CV включает в себя высокий приложенный потенциал, что приводит к образованию менее сопряженных олигомеров PD. По этой причине предполагается, что при полимеризации ПД методом ЦВ поры больше, а проницаемость слоя ППД выше по сравнению с полимеризацией при постоянном потенциале [8, 13]. Однако, как отмечалось в разделе «Предпосылки», разные авторы пришли к противоречивым выводам о предпочтительном методе осаждения частичных разрядов, и во многих случаях CV давал хорошие результаты. По нашему мнению, как CV, так и амперометрия с постоянным потенциалом могут обеспечить создание мембран PPD с хорошими селективными свойствами, и оптимизация необходима для каждого конкретного случая.
Мембрана PPD была отчетливо видна на поверхности электрода в виде однородной прозрачной золотисто-коричневой пленки. Чтобы подтвердить, что это действительно PPD, полимеризация PD была дополнительно подтверждена спектроскопией. Спектр диффузного отражения пленки в УФ-видимом диапазоне (рис. 2) демонстрирует интенсивные полосы поглощения при 222 и 315 нм, аналогичные полосам мономера и относящиеся к электронным переходам в ароматических кольцах [14], тогда как безликая абсорбция при 400–800 нм, постоянно уменьшающийся с длиной волны, соответствует π - π * электронные переходы в сильно сопряженной ароматической системе проводящего полимера PPD.
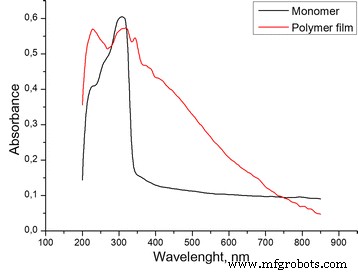
УФ-видимые спектры диффузного отражения м -фенилендиамин и мембрана PPD, образованная на Pt электроде
Для лучшей интерпретации полученных результатов было бы полезно оценить размер пор в мембранах PPD, полученных разными методами. Однако прямое определение размера пор в мембране PPD практически невозможно, так как мембрана состоит из множества слоев PD, а поры в нижних слоях могут иметь разный размер. Киллоран и О’Нил определили, что толщина эффективной мембраны от м -PD составлял 15 нм, и площадь поперечного сечения одной цепи олигомерного полимера, оцененная del Valle et al. составляла 1 нм [7, 15]. Таким образом, мембрана PPD содержит примерно 15 слоев полимера. Поскольку мембрана PPD обладает гидрофобными и изолирующими свойствами, мембрана должна иметь перфорирующие нанопоры, которые простираются к поверхности электрода и позволяют обходить молекулы пероксида водорода, в противном случае H 2 О 2 не может окисляться и генерировать амперометрический сигнал. Поры определенно неоднородны, и минимальный диаметр пор должен быть меньше 1 нм, чтобы исключить электроактивные молекулы, и, таким образом, довольно сложно анализировать поры даже с помощью электронного или атомно-силового микроскопа. По этим техническим причинам гораздо проще оценить эффективность мембраны PPD, оценив проницаемость мембраны для различных молекул. Такой косвенный подход широко распространен и позволяет сравнивать практические характеристики разных мембран.
Эффективность осажденных мембран PPD была протестирована с использованием различного количества циклических вольтамперограмм (рис. 3).
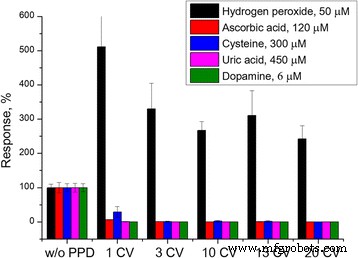
Эффективность мембран PPD, нанесенных с использованием разного количества CVA
ППД-мембраны, нанесенной одним ЦВА, было явно недостаточно для устранения влияния мешающих факторов. Однако здесь эффект электроактивации платины был наиболее сильным. При дальнейшем увеличении числа вольтамперограмм отклик на помехи уменьшился, но вместе с тем снизилась и чувствительность преобразователя к перекиси водорода, вероятно, из-за слишком толстого слоя PPD, затрудняющего диффузию вещества. Трех CVA было достаточно для полного исчезновения ответов на дофамин и мочевую кислоту и значительного уменьшения ответов на аскорбиновую кислоту и цистеин. Поэтому за оптимальные были взяты три ЦВА, а концентрация фенилендиамина была увеличена до полного устранения интерферентного воздействия (рис. 4).
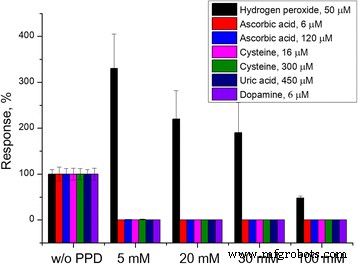
Эффективность мембран PPD, осажденных при различных концентрациях фенилендиамина
Примечательно, что использования 5 мМ фенилендиамина было достаточно для устранения реакции на помехи в небольших концентрациях, остающихся после разбавления образца, но недостаточных для работы с неразбавленными образцами. Повышения концентрации фенилендиамина до 20 мМ и трех ЦВА оказалось достаточно для полного устранения воздействия цистеина и снижения ответов на аскорбиновую кислоту до минимального уровня (0,1% ответа на аскорбиновую кислоту без мембраны PPD). Использование более высокой (до 100 мМ) концентрации фенилендиамина привело к двукратному снижению чувствительности преобразователя к перекиси водорода, вероятно, из-за слишком толстого слоя PPD. Таким образом, нанесение PPD-мембраны с использованием трех CVA в 30 мМ фенилендиамине является оптимальной процедурой. Поскольку одна вольтамперограмма длилась около 2 минут, осаждение мембраны на один датчик длилось 6 минут.
Затем была изучена стабильность мембраны PPD. После нанесения мембран PPD сенсоры помещали в рабочий буфер на 2 часа и измеряли реакции на пероксид водорода, аскорбиновую кислоту и цистеин для оценки изменений проницаемости мембран (рис. 5). Было обнаружено, что отклики на перекись водорода во время работы немного увеличились, тогда как небольшие отклики на помехи стали еще меньше. Вероятно, это произошло потому, что аскорбиновая кислота и цистеин постепенно забивали несколько крупных пор в слое PPD. Этот эксперимент продемонстрировал, что мембрану PPD можно использовать без существенной потери селективности по перекиси водорода в течение как минимум 2 часов.
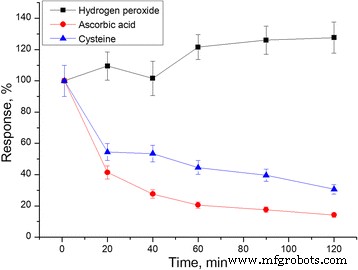
Стабильность мембраны PPD в течение 2 часов. Ответы на три вещества были нормализованы к первоначальному ответу на соответствующее вещество после осаждения PPD
Была исследована стабильность при хранении мембраны PPD. Датчики с нанесенными мембранами из ППД хранились в сухом виде в течение 8 суток при –18 ° С; периодически датчики размораживали и измеряли реакцию на перекись водорода, аскорбиновую кислоту и цистеин (рис. 6). За этот период чувствительность сенсоров к перекиси водорода увеличилась в 2,5 раза; чувствительность к аскорбиновой кислоте и цистеину не изменилась. Этот эффект можно объяснить медленным набуханием мембраны PPD, что привело к улучшению диффузии перекиси водорода через слой PPD.
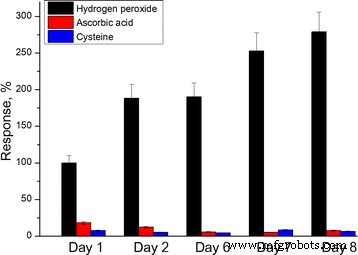
Стабильность при хранении мембраны PPD. Ответы были нормализованы до ответа на H 2 О 2 в первый день
Наконец, эффективность мембраны PPD была подтверждена при анализе реальных биологических образцов. Датчики без мембран после добавления сыворотки крови в рабочую ячейку демонстрировали слабые сигналы из-за наличия электроактивных соединений. Однако после нанесения мембраны никаких откликов получено не было. Аналогичные результаты были получены с лизатом нейронов. Эти эксперименты демонстрируют эффективность разработанного метода нанесения ППД на платиновые дисковые электроды и возможность использования модифицированных преобразователей для работы со сложными биологическими образцами.
Полезно сравнить метод осаждения PPD, разработанный в этой работе, с методами, описанными ранее (Таблица 4).
Как видно, представленный метод является наиболее быстрым и блокирующие свойства полученной мембраны лучше или, по крайней мере, не хуже, чем у других мембран PPD.
Выводы
Нами исследованы условия нанесения полупроницаемой мембраны на основе полифенилендиамина с целью уменьшения влияния мешающих веществ на работу биосенсора. Было показано, что электрополимеризация фенилендиамина методом циклической вольтамперометрии протекает легче и обеспечивает лучшие свойства мембраны по сравнению с электрополимеризацией при постоянном потенциале. Исследована зависимость эффективности мембраны ППД от количества циклических вольтамперограмм и концентрации фенилендиамина. Показано, что влияние мешающих веществ на работу сенсора можно полностью исключить при использовании трех циклических вольтамперограмм в 30 мМ фенилендиамине. С другой стороны, при работе с разбавленными образцами, то есть с более низкими концентрациями электроактивных веществ, целесообразно снизить концентрацию фенилендиамина до 5 мМ, что приведет к более высокой чувствительности преобразователя к перекиси водорода из-за более тонкого слоя PPD. Мембрана PPD может использоваться без существенной потери ее селективности по перекиси водорода в течение не менее 2 часов непрерывной работы и может храниться не менее 8 дней. Было показано, что датчик с мембраной PPD нечувствителен к электроактивным веществам, присутствующим в биологических образцах, и может быть использован для создания биосенсора.
Наноматериалы
- С# с использованием
- Продвижение к 7 нм
- Использование углов для улучшения будущего электроники
- Умный бетон с использованием наночастиц
- Обзор применения биосенсоров и наносенсоров в агроэкосистемах
- Высокопроизводительное производство качественных нановолокон с использованием модифицированного электрос…
- Получение и оптические свойства пленок GeBi с использованием метода молекулярно-лучевой эпитаксии
- Удаление антибиотиков из воды с помощью полностью углеродной трехмерной нанофильтрационной мембраны
- Дизайн бионического кохлеарного базилярного мембранного акустического датчика для частотной селективности…
- Производство эффективных органических-неорганических перовскитных солнечных элементов в окружающем воздух…



