Наножидкости TiO2 - Часть 1:Приготовление и свойства
Аннотация
Как новое поколение рабочей жидкости, наножидкости долгое время считались горячей темой исследований в последние три десятилетия. Многие обзорные статьи содержат исчерпывающие и систематические обзоры разработки и современного состояния наножидкостей. На сегодняшний день становится все труднее предоставить исчерпывающий обзор всех видов наножидкостей из-за огромного количества соответствующей литературы. И многие противоречия и несоответствия в приведенных аргументах наблюдались в различных наножидкостях. Между тем систематических или всеобъемлющих обзоров по определенному виду наножидкости недостаточно. Поэтому в данном обзоре основное внимание уделяется исследованию одного из самых горячих видов, а именно. TiO 2 наножидкость, которая привлекла большое внимание ученых из-за ее интересных и всеобъемлющих свойств, таких как потрясающая дисперсность, химическая стабильность и нетоксичность. Поскольку предварительным условием является приготовление наножидкостей, а физические свойства являются критическими факторами для дальнейшего применения, в этой первой части обзора суммируются недавние исследования по получению, стабильности и физическим свойствам TiO 2 наножидкости.
Обзор
Фон
Разработка наножидкостей
Поскольку теплопередающая способность жидкостей обычно намного ниже, чем у твердых металлов или металлических соединений, ожидается, что теплопередача жидкости может быть улучшена за счет суспендирования в ней твердых частиц. Однако у суспензий с частицами миллиметрового или микрометрового размера появились некоторые недостатки, такие как плохая диспергируемость, агрегация и осаждение, а также прилипание к внутренней поверхности системы, что могло легко привести к ухудшению характеристик теплопередачи, увеличению мощности откачки, и даже трубный блок. Новая возможность преодолеть эти недостатки была обнаружена, когда появилось новое поколение подвески, а именно. наножидкость была предложена Чоем в 1995 году [1].
Нанофлюид - это новый вид разбавленной суспензии, содержащей наночастицы, по крайней мере, одномерный размер которых меньше 100 нм. Когда размеры частиц в суспензии достигают нанометрового уровня, ожидается, что суспензия может достичь лучших тепловых свойств и одновременно оставаться более стабильной, чем смесь миллиметровых или микрометровых частиц / жидкости. Стабильная наножидкость также может получить лучшую ликвидность, и иногда ее можно рассматривать как однофазную жидкость. Следовательно, одна из самых больших проблем, с которыми сталкиваются наножидкости, - это подготовка и стабильность, которые являются основными предпосылками для достижения хороших теплофизических свойств и дальнейших инженерных приложений. Соответственно, исследования наножидкостей в целом можно разделить на следующие направления:подготовка и исследование стабильности [2, 3], физические свойства, такие как теплопроводность [4,5,6,7,8] и анализ вязкости [9,10 , 11,12], исследования теплопередачи [13, 14], инженерные приложения [15,16,17,18], а также теоретический анализ или разработка моделей [19,20,21,22,23,24,25].
В последние два десятилетия, особенно в последние 10 лет, исследования наножидкостей стремительно увеличивались благодаря их захватывающим свойствам, и многие исследователи проводили экспериментальные или теоретические исследования различных аспектов наножидкостей [26,27,28,29]. Чтобы проиллюстрировать это, на рис. 1 можно увидеть тенденцию к росту числа публикаций, содержащих «наножидкости или наножидкости» в названии, взятом из «паутины науки». Этот рисунок ясно показывает, что исследования наножидкостей растут настолько быстро, что публикации в 2016 г. собрали 21,9% от общего числа за последние два десятилетия. Если бы область поиска была уменьшена до полного текста и содержала больше поисковых баз данных, результаты могли бы увеличиться в несколько раз. Таким образом, становится все труднее предоставить исчерпывающий обзор всех видов наножидкостей из-за огромного количества соответствующей литературы. А за последние 2 года несколько обзоров были сосредоточены на одном аспекте свойства или определенном виде наножидкости, чтобы предоставить более полные обзоры. Например, в таблице 1 показаны последние обзоры некоторых специализированных аспектов наножидкостей, таких как:
- (1)
Подготовка или характеристика [30,31,32]
- (2)
Некоторые виды наночастиц (Al 2 О 3 , TiO 2 , CuO, графен, УНТ, гибридные наножидкости) [32,33,34,35,36,37,38]
- (3)
Определенные виды базовой жидкости (вода, ЭГ, смесь ЭГ / вода, масло) [39,40,41,42]
- (4)
Одно или несколько физических свойств (теплопроводность, вязкость, удельная теплоемкость) [43,44,45,46,47]
- (5)
Определенные характеристики (принудительная, природная, конвекционная теплопередача при кипении, падение давления, миграция частиц) [48,49,50,51,52,53]
- (6)
Некоторые специализированные приложения (теплообменники, солнечные коллекторы, охлаждение) [54,55,56,57,58,59,60,61,62]
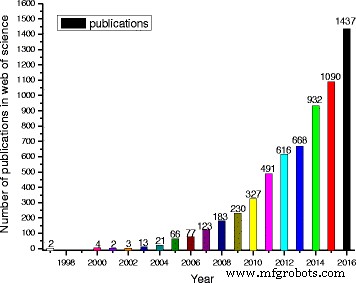
Количество публикаций, содержащих «наножидкости или наножидкости» в названии, взятых из «Web of Science»
Преимущества TiO 2 Наножидкости
Приведенные выше введения в Таблицу 1 демонстрируют возможность и важность обзоров по некоторым специализированным направлениям наножидкостей, поскольку они могут предоставить относительно полную и подробную информацию по определенному аспекту. Как один из наиболее распространенных видов TiO 2 наножидкости привлекли большое внимание ученых благодаря своим превосходным физическим и химическим свойствам. Во-первых, TiO 2 широко используется в области печати, косметики, очистки воздуха и т. д. и является общепризнанным безопасным материалом, не токсичным для человека. Учитывая безопасность этой наножидкости, Taghizadeh-Tabari et al. [63] применили TiO 2 –Водная наножидкость в пластинчатом теплообменнике для предприятий пастеризации молока. Во-вторых, TiO 2 обладает исключительной химической стабильностью, устойчивостью к кислотам, щелочам и эрозии большинства органических растворов. В-третьих, TiO 2 наночастицы производятся в более крупном промышленном масштабе, что делает их относительно экономичными [64]. В-четвертых, TiO 2 Наночастицы относительно хорошо распределяются как в полярных, так и в неполярных основных жидкостях, особенно при добавлении надлежащего диспергатора. Ян и др. [65] исследовали дисперсионную стабильность 20 типов наночастиц в растворе аммиак – вода. Результаты показали, что анатаз TiO 2 был наиболее стабильным оксидом металла без поверхностно-активного вещества, и его стабильность можно было дополнительно улучшить, добавив соответствующее поверхностно-активное вещество. В отчете Силамбарасана и др. [66] абсорбционная способность TiO 2 наножидкости очень мало изменились после 10 дней хранения, как показано на рис. 2. Такое небольшое изменение абсорбционной способности указывает на то, что стабильность TiO 2 наножидкости, которые они приготовили, были довольно замечательными. Обобщая доступную литературу, можно сделать вывод, что TiO 2 наночастицы, как правило, лучше распределяются, чем другие обычные наночастицы оксидов металлов. Поскольку диспергирование наночастиц в жидкости является наиболее важной предпосылкой для применения наножидкостей, многие исследователи выбрали TiO 2 наножидкости в качестве объектов исследования.
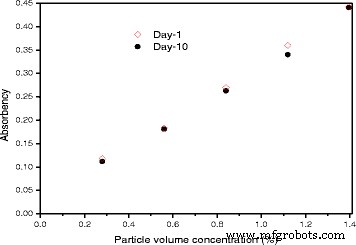
Поглощение как функция объемной концентрации частиц на 1-й и 10-й день [66]. Воспроизведено с разрешения Elsevier
Поскольку подготовка наножидкостей является необходимым условием, а физические свойства являются критическими факторами для разработки и создания приложений, связанных с энергетикой, цель двух обзоров - систематически обобщить результаты последних исследований TiO 2 наножидкости, включая приготовление, стабильность, физические свойства и энергетические приложения. Подробное схематическое изображение двух обзоров по приготовлению, свойствам и применению TiO 2 Наножидкости показаны на рис. 3. Настоящий обзор организован с точки зрения определенного вида наножидкости, который считается одним из наиболее близких к практическому применению. И основная цель этой статьи - предоставить исследователям полезное справочное руководство для обновления знаний об исследовательском статусе TiO 2 . наножидкости и указать на критические проблемы и полезные рекомендации для будущих направлений исследований.
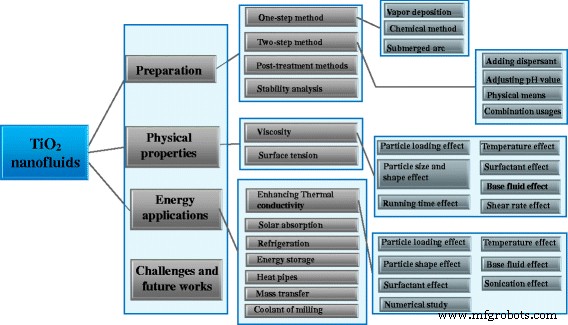
Схематическое изображение приготовления, свойств, применения и проблем TiO 2 наножидкости
Подготовка TiO 2 Наножидкости
Одношаговый метод
Как правило, можно выделить два основных метода подготовки:одноэтапные и двухэтапные. Одноэтапный метод реализуется путем суспендирования наночастиц в требуемой рабочей жидкости, сопровождающей процесс их образования. Одноэтапный метод можно подразделить на физические и химические методы. Физический метод включает осаждение из паровой фазы, лазерную абляцию и дугу под флюсом. Химический метод означает производство наножидкостей путем химической реакции. Как правило, вышеуказанные методы используются как методы получения сухих наночастиц. Однако эти методы можно превратить в одностадийные методы приготовления наножидкостей, заменив коллекторы сухих частиц соответствующими контейнерами для базовой жидкости.
Отложение паров
Осаждение из паровой фазы - распространенный физический метод приготовления наножидкости. Типичное устройство для этого метода можно увидеть на рис. 4 [67]. Объемный твердый материал для приготовления наночастиц нагревается и испаряется в контейнере низкого давления, заполненном инертным газом, а затем пар сырья охлаждается закручивающейся пленкой жидкости и оседает в базовых жидкостях. Осаждение из паровой фазы обычно используется при приготовлении металлических наножидкостей, но этот метод редко применяется для TiO 2 наножидкости из-за высокой температуры кипения. Однако этот метод можно улучшить, используя электрический нагрев для достижения высокой температуры. Ли и др. [68] использовали метод одностадийного импульсного проволочного испарения (PWE) для приготовления наножидкостей на основе этиленгликоля (EG), содержащих TiO 2 . наночастицы. Они приложили импульсное напряжение 25 кВ к тонкому проводу и перегрели его, чтобы он испарился в плазму за несколько миллисекунд. Затем плазма взаимодействовала с кислородом аргона и конденсировалась в наночастицы. Наконец, они получили TiO 2 наножидкости, позволяя наночастицам напрямую контактировать с ЭГ внутри стенки камеры.
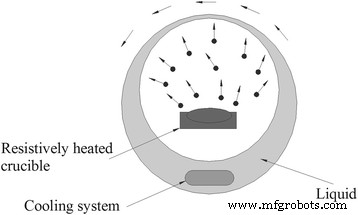
Типичное устройство метода осаждения из паровой фазы для приготовления наножидкостей. Перерисовано на основе ссылки [67]
Метод подводной дуги
Метод подводной дуги может обеспечить и поддерживать еще более высокую температуру для приготовления TiO 2 наножидкости. Chang et al. [69] изготовили новую систему синтеза под флюсом для производства TiO 2 . наножидкости. Их устройство в основном состоит из блока дуговой напыления, вакуумного пространства и систем контроля температуры и давления, что показано на рис. 5. В этом устройстве объемный TiO 2 твердое вещество испарялось методом дугового разряда в вакууме, а затем газообразный TiO 2 был быстро охлажден до мелкодисперсного твердого вещества изолированной жидкостью. Они пришли к выводу, что этот метод более известен, чем аэрозольные методы, потому что приготовленные наножидкости имели более высокую дисперсионную стабильность и могли рассматриваться как ньютоновские жидкости. Zhang et al. [70] усовершенствовал метод подводной дуги за счет оптимизации системы управления параметрами реакции, охлаждающей циркуляции и размера устройства с подводной дугой. На основе оптимизированной системы они могут производить более стабильный и более мелкий TiO 2 суспензия с хорошей воспроизводимостью размера частиц. И адсорбционные характеристики их TiO 2 наночастицы лучше коммерческих.
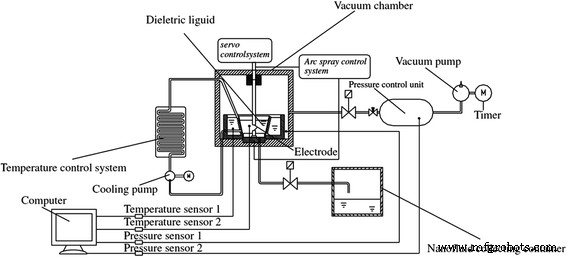
Схематический рис. усовершенствованной системы синтеза наножидкостей под флюсом (ISANSS) [40]. Воспроизведено с разрешения Японского института металлов и материалов
Химический метод
Химический метод заключается в получении наножидкостей путем химической реакции и обычно включает метод соосаждения и метод преобразования прекурсора. Обычный химический метод синтеза TiO 2 наножидкости основаны на прекурсоре TiO (OH) 2 осадка в результате химической реакции неорганических солей титана и аммиака с водой, затем прокаливаются для получения TiO 2 пудра. Некоторые исследования показали, что наножидкости, полученные химическим методом, имеют лучшую стабильность и более высокую теплопроводность, чем те, которые получены двухступенчатым методом [71]. Еще одна отличительная черта этого метода - управляемость микроструктуры наночастиц. Обычный метод регулировки заключается в контроле таких параметров, как температура синтеза, значение pH, время обработки в ультразвуковой ванне и добавки [72]. Однако этот метод в основном используется для приготовления TiO 2 порошок путем сушки жидкости в результате сложной жидкой среды в этом методе не подходит для детального применения наножидкостей. А когда TiO 2 порошки могут стабильно суспендироваться в требуемой базовой жидкости, изменяя объем жидкости без процесса сушки, этот метод будет многообещающим при условии, что новые параметры жидкой среды, такие как кислотность или щелочность и концентрация электролита, близки к исходной жидкости для приготовления.
В одностадийном методе отсутствуют процессы сушки и диспергирования, которые могут привести к агломерации наночастиц. Поэтому обычно считается, что одностадийный метод позволяет получить более стабильные наножидкости [73]. Однако есть и недостатки, ограничивающие область применения одношагового метода. Например, осаждение из паровой фазы нельзя использовать для приготовления наножидкостей, содержащих высококипящие или некристаллические наночастицы. Методы лазерной абляции и вакуумной заглубленной дуги являются дорогостоящими и требуют критических условий. Химический метод обычно требует определенных условий реакции, таких как требуемое значение pH и температура. И он может легко синтезировать некоторые побочные продукты в жидкостях [74]. Например, Sonawane et al. [75] использовали золь-гель метод для синтеза анатаза TiO 2 . наночастицы с постоянным значением pH 5. Раствор прекурсора включал изопропоксид титана и изопропанол, а также бидистиллированную воду. Можно сделать вывод, что эта смесь с таким специфическим значением pH и сложным химическим составом не может быть использована в качестве теплопередающих наножидкостей. Поэтому они высушили синтезированный TiO 2 наночастицы, а затем повторно диспергировали их в требуемых основных рабочих жидкостях, включая воду, ЭГ и парафиновое масло, с помощью ультразвуковой обработки для получения требуемых наножидкостей. Можно сделать вывод, что одностадийный метод вряд ли будет использоваться для некоторых наножидкостей с конкретными ингредиентами, особенно для наножидкостей с чистой водой, маслом, хладагентом и т. Д. В качестве основных жидкостей, а также для прикладных систем, содержащих летучий газ.
Двухэтапный метод
В двухэтапном методе процессы производства наночастиц и их суспендирования в требуемой базовой жидкости выполняются независимо. Двухэтапный метод широко используется для TiO 2 наножидкости, поскольку методы синтеза TiO 2 наночастицы практически достигли промышленных масштабов производства. На рисунке 6 показана типичная процедура двухэтапного метода. Сухие наночастицы сначала синтезируются химическими или физическими методами, а затем суспендируются в необходимых базовых жидкостях. Однако, поскольку сильная сила взаимодействия частиц может привести к столкновению и агрегированию наночастиц, им довольно трудно стабильно и равномерно суспендироваться в базовой жидкости. Поэтому обычно используются некоторые методы диспергирования для обеспечения хорошей стабильности и доступности наножидкостей.
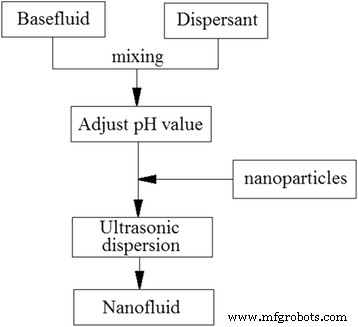
Типичная процедура двухэтапного метода приготовления наножидкостей [35]. Воспроизведено с разрешения Elsevier
В таблице 2 представлена сводка соответствующих исследований методов получения TiO 2 . наножидкости в последние годы. Можно видеть, что типы базовой жидкости включают воду, EG, хладагент, органические растворители и т. Д. В общем, в двухэтапном процессе приготовления широко использовались три основных метода диспергирования и суспендирования наночастиц в базовых жидкостях.
Добавление диспергатора
Первый метод диспергирования заключается в модификации поверхности частиц путем добавления диспергатора, который, как ожидается, предотвратит агрегацию наночастиц за счет электростатического отталкивания или стерических препятствий молекул диспергатора [76]. Можно отметить, что в существующих отчетах наиболее часто используемым поверхностно-активным веществом был CTAB. И другие виды, включая SDBS, SDS, PVP, олеиновую кислоту, уксусную кислоту и PEG, также использовались в некоторых исследованиях. В 2012 году Мо и др. [77] использовали двухэтапный метод для приготовления двух видов наножидкостей путем суспендирования стержнеобразного рутила TiO 2 и сферический анатаз TiO 2 в воду. Они заметили, что наножидкости могут оставаться стабильными в течение 286 часов при использовании SDS в качестве диспергатора. В следующем году они сравнили влияние на дисперсию трех различных поверхностно-активных веществ, включая SDBS, PVP и CTAB [78]. И они обнаружили, что в этом объеме экспериментальных исследований, когда массовое соотношение SDBS и наночастиц диоксида титана составляет 0,3, они могут получить лучшую дисперсию наножидкости. Накаяма и Хаяси [79] использовали двухэтапный метод для диспергирования высокой загрузки TiO 2 наночастицы в органической базовой жидкости с помощью модификации поверхности пропионовой кислотой и н-гексиламином. Они обнаружили, что модификация поверхности может улучшить дисперсию наножидкостей, что показало лучший эффект при двухэтапном методе, чем при одноэтапном методе. Характеристики TiO 2 полученные ими наночастицы не изменяются, и их можно хорошо применять для различных жидкостей на основе органических растворителей.
Регулировка значения pH
Второй метод диспергирования заключается в регулировании среды диспергирования путем регулирования значения pH базовой жидкости. Этот метод заключается в обеспечении наночастиц более высоким дзета-потенциалом путем регулирования подходящего значения pH жидкости, что, как ожидается, позволит избежать контакта наночастиц из-за более высокого электростатического отталкивания [76]. Ли и Сан [80] исследовали влияние значения pH на агрегационное поведение TiO 2 наночастицы в моно- и бинарных базовых жидкостях с помощью SRFA и Fe (III). Они обнаружили, что адсорбция SRFA значительно улучшила стабильность суспендирования TiO 2 наночастицы при значениях pH 4, 6 и 8, и они думали, что это в основном вызвано резким ростом отрицательных зарядов на поверхности частиц. He et al. [81] обнаружили, что стабильность TiO 2 наножидкости можно значительно улучшить, установив значение pH базовой жидкости до 11, при котором может быть сформирован высокий дзета-потенциал 45 мВ для предотвращения повторной агломерации и осаждения и возможного последующего загрязнения медной трубки. Наножидкости с оптимальным значением pH могут оставаться стабильными в течение нескольких месяцев. Также Vakili et al. [82] и Сен и др. [83] установили значение pH базовой жидкости до 11 и обнаружили, что TiO 2 наножидкости могут иметь лучшую дисперсионную стабильность в этих сильно щелочных условиях.
Физические средства
Третий метод диспергирования равносилен разрушению агломератов частиц физическими средствами, например механическим перемешиванием, ультразвуковыми волнами и шариковым измельчением с перемешиванием. Предполагается, что эти методы генерируют кавитационные колебания, которые могут приводить к эффектам сдвига, разрушения и диспергирования [84]. Общепризнано и доказано, что наножидкости будут более стабильными после надлежащей сверхзвуковой вибрации, и это можно еще раз доказать, обобщив стабильность дисперсии TiO 2 наножидкости. Из Таблицы 2 видно, что почти все процессы подготовки включали в себя некоторые физические процедуры. Ли и др. [85] диспергированный TiO 2 наночастиц в раствор МДЭА для приготовления TiO 2 –MEDA – H 2 О наножидкости. Они обнаружили, что наножидкости могут оставаться стабильными в течение 48 часов при механическом перемешивании без добавления диспергатора. Таджик и др. [86] исследовали влияние различных типов ультразвука (непрерывных или прерывистых импульсов) на поведение суспензии TiO 2 на водной основе. наножидкости. Результаты показали, что непрерывные импульсы имеют лучший эффект прерывания, чем прерывистые, в то время как последние не могут разделить некоторые большие скопления. Silambarasan et al. [66] экспериментально исследовали влияние шаровой мельницы с перемешиванием и обработки ультразвуком на поведение суспензии смеси на водной основе, содержащей субмикронный TiO 2 . частицы. Они обнаружили, что шариковая мельница с перемешиванием может производить стабильные суспензии, содержащие субмикронные частицы, а обработка ультразвуком может быть дополнительно применена для управления транспортным поведением TiO 2 подвески. Лонго и Зилио [87] сравнили влияние механического перемешивания и ультразвуковых волн на дисперсионные характеристики TiO 2 . –Воды и Al 2 О 3 –Водные наножидкости. Они заметили, что обработка ультразвуком при 25 кГц в течение 48 часов показала лучшую эффективность диспергирования, чем простое механическое перемешивание. После обработки физическим диспергированием оба типа наножидкостей могут оставаться стабильными более 1 месяца.
Комбинированное использование
Обычно комбинации методов диспергирования с добавлением поверхностно-активного вещества, изменением значения pH основных жидкостей и ультразвуковой вибрацией используются в двухэтапном методе для достижения лучших характеристик диспергирования наножидкостей. Лю и др. [88] диспергированный TiO 2 наночастицы (25 нм) в воде для получения стабильного TiO 2 наножидкости. Для получения стабильного TiO 2 использовали три обработки, включая добавление PEG1000 в качестве диспергатора, ультразвуковую вибрацию и регулирование значения pH до 4–5 или 9–10. наножидкости. Fedele et al. [89] использовали комбинированный метод диспергирования, включающий добавление уксусной кислоты в качестве диспергатора и доведение значения pH до диапазона от 1,86 до 3,07 в соответствии с массовыми долями наночастиц, а также подходящую обработку ультразвуком; они заметили, что наножидкости могут оставаться стабильными в течение по крайней мере 35 дней, потому что средний размер частиц оставался приблизительно постоянным в течение этих периодов. Ghadimi et al. [90] приготовили чрезвычайно стабильный TiO 2 на водной основе. наножидкости путем добавления уксусной кислоты и доведения pH до 5, а также ультразвуковой вибрации. Они нашли TiO 2 наножидкости оставались стабильно взвешенными после 1 года хранения. Есть также несколько других примеров комбинированного использования трех техник. Из таблицы 2 видно, что Mo et al. [77, 78], Kim et al. [91], Mushed et al. [92], Jarahnejad et al. [93], Ghadimi et al. [90], а Саид и др. [94] использовали все три метода диспергирования для достижения наилучшего эффекта диспергирования.
Однако изменение значения pH основных жидкостей серьезно ограничит диапазон применения TiO 2 наножидкости в качестве теплоносителей из-за коррозии и безопасности в кислых и щелочных условиях. Таким образом, все больше исследователей более склонны использовать два других метода диспергирования, а именно. добавление диспергентов и физических средств для потенциальных применений в реальных системах. Wu et al. [95] и Ян и др. [74] предназначен для нанесения TiO 2 наножидкости в аммиачно-водопоглощающие холодильные системы. Метод изменения значения pH недоступен, поскольку базовая жидкость имеет определенный диапазон pH, определяемый концентрацией аммиака. Поэтому они использовали PAA или PEG1000 в качестве диспергатора в сочетании с ультразвуковой вибрацией для повышения стабильности TiO 2 . наножидкости и добились хороших эффектов. Чтобы применить наножидкости в компрессионных холодильных системах, Peng et al. [96] добавил TiO 2 наночастиц в R141b для приготовления нанохладагента с размером частиц 25, 40, 60 и 100 нм соответственно. Нанохладагент обрабатывали ультразвуком с помощью ультразвукового процессора в течение 20 мин. И они думали, что этот шаг важен для достижения хорошего диспергирования наночастиц в объемном хладагенте. Также они экспериментально изучили влияние анионных, катионных и неионных поверхностно-активных веществ на стабильность нанохладагента. И они заметили, что тип поверхностно-активного вещества является важным фактором для размера частиц в стационарном состоянии. Kayhani et al. [97] использовали поверхностно-активное вещество гексаметилдисилазан и методы ультразвуковой вибрации, приготовили сухой TiO 2 сначала наночастицы, а затем добавляли в дистиллированную воду с обработкой ультразвуковыми колебаниями (400 Вт и 24 кГц) в течение 3–5 часов. Они обнаружили, что приготовленные наножидкости могут оставаться стабильными в течение нескольких дней, и не происходит седиментации. Ян и др. [98] обнаружили, что использование поверхностно-активного вещества SDBS в диапазоне низких концентраций и ультразвуковой вибрации может улучшить поведение суспендирования TiO 2 на основе водного аммиака. наножидкости.
Методы последующей обработки
Помимо обычного одноэтапного или двухэтапного метода, были также предложены некоторые методы последующей обработки для приготовления наножидкостей. Некоторые лучше диспергированные наножидкости могут быть получены из некоторых плохо диспергированных необработанных жидкостей, содержащих агломерированные наночастицы, с помощью некоторых специальных обработок, таких как разрушение или удаление агломерированных наночастиц из необработанной жидкости.
Hwang et al. [99] заметили, что эффекты мешалки, ультразвуковой ванны и ультразвукового дезинтегратора ограничены для улучшения дисперсии наножидкостей. Они использовали гомогенизатор высокого давления для удаления наножидкости, и этот процесс можно увидеть на рис. 7. В их исследованиях начальный средний диаметр частиц может быть уменьшен, по крайней мере, на один порядок величины после повторной обработки с помощью гомогенизатор высокого давления. И они обнаружили, что гомогенизатор высокого давления показал лучший эффект среди всех средств физического диспергирования, использованных в их исследовании.
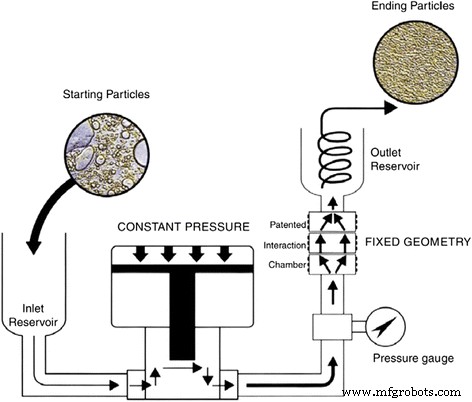
Принципиальная схема гомогенизатора высокого давления для получения наножидкостей [99]. Воспроизведено с разрешения Elsevier
Ян и др. [100] использовали метод оптимизации для приготовления наножидкостей. Оптимизирующий процесс улучшения диспергирования наножидкостей показан на рис. 8. Они удалили хорошо взвешенные наножидкости из основной массы более концентрированных наножидкостей, а затем восстановили удаленные части до требуемых концентраций путем разбавления добавленных базовых жидкостей. Коэффициент разбавления был основан на том, что впитывающая способность наножидкости прямо пропорциональна ее концентрации. И они наблюдали отложения и измеряли различную впитывающую способность, чтобы оценить эффект от метода. Результаты показали, что как для рутила, так и для анатаза TiO 2 наножидкостей, оптимизированный метод может значительно улучшить их дисперсию и произвести более стабильный TiO 2 наножидкости.
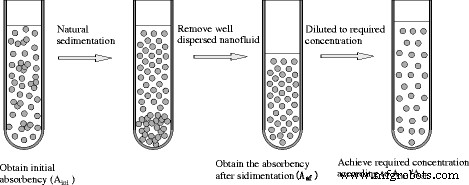
Оптимизация процесса улучшения дисперсности наножидкостей [132]. Воспроизведено с разрешения Taylor &Francis
Есть некоторые противоречия или несоответствия в аргументах относительно приготовления наножидкостей. Во-первых, вопрос о том, следует ли применять одноэтапный метод или двухэтапный метод, является несоответствием. Ожидается, что одностадийный метод позволит достичь лучшей стабильности дисперсии, поскольку он позволяет избежать процессов сушки и диспергирования наночастиц. Однако для побочных эффектов одноэтапного метода, таких как побочный продукт, среда специального раствора кажется более фатальной, что серьезно ограничивает область применения наножидкостей. Поэтому двухэтапный метод более широко используется из-за большой адаптируемости и значительного улучшения методов диспергирования TiO 2 наночастицы. В целом, для получения TiO 2 рекомендуется использовать двухэтапный метод с соответствующей последующей обработкой. наножидкости.
Другой спор заключается в том, следует ли использовать поверхностно-активное вещество при приготовлении наножидкостей. The presence of appropriate surfactant can improve the dispersion stability but also may bring some side effects such as a decrease in thermal conductivity, increases in viscosity, and foaming ability. Due to the potential advantages such as reduction in surface tension and improvement in re-dispersible property, the surfactant with low concentration is suggested to be used when it not brings obvious decrease in thermal conductivity or increase in viscosity and foaming ability. In addition, the influence of surfactant on thermal conductivity and viscosity of nanofluids is also a controversy in current studies.
Stability of Nanofluids
Stability research is generally followed the preparation to achieve the optimal dispersion craft since it is closely related to the effectiveness and practicability of nanofluids. The great amount of aggregations in the unstable nanofluids can easily cause sedimentation and adsorption on the inner surface of the system, which will probably result in the degradation of heat transfer efficiency, raising of pumping power, and even blocking up in system pipe blocks.
It can be found from Table 2 that the stable times of different researchers thought were variously distributed in the range of several hours to 1 year. A most stable nanofluid was obtained by a combined use of adding surfactant, controlling pH value, and ultrasonic vibration by Ghadimi et al. [90]. Also, the particles’ loading in their experiment was very low at 0.1 wt.%, which was also another contribution for the long-term stability. Without adding surfactant, the nanofluids can also achieve a better dispersion stability by adjusting the pH value of the liquid to a suitable value. For example, He et al. [81] and Longo et al. [87] observed that the TiO2 nanofluids can keep stable for months by adjusting the pH to 11 with the help of ultrasonic vibration. Also, some TiO2 nanofluids with good dispersion stability were prepared only through physical means in some research. Padmanabhan et al. [101] used a magnetic stirring to prepare R134a and mineral oil-based TiO2 nanofluids that can keep stable for 6 months. This is likely because the particles’ loading employed in their study is very low (0.1 g/L) and the high viscosity of the R134a and mineral oil base fluid can also provide a superior dispersion condition. This conclusion can also serve as proved by Palabiyik et al.’s results [102]. They obtained a TiO2 nanofluids stable for several months by the help of sonication with a higher viscosity propylene glycol as base fluid. The similarity is that they were both using organic solvent of high viscosity as base fluids and the best ones was only treated by physical means. Also, it can be seen that TiO2 nanoparticles have a comprehensive dispersivity in both polar aqueous solution and nonpolar organic solution.
However, the above judgments on dispersion stability of various TiO2 nanofluids are not very objective and accurate because most of the results showed the least stable time. Moreover, there is no uniform standard for evaluating the stability of nanofluids, and the stability evaluating methods in different research were sufficiently different. Current evaluation methods of stability of nanofluids mostly consisted of observing the stratification or sedimentation and testing the zeta potential, particles’ size, or absorbency. Mansel et al. [103] used the sedimentation observation method and zeta potential method to evaluate the stability of TiO2 –water nanofluids in different pH values. They observed that in low or high pH value, the TiO2 –water nanofluids can obtain good stability. Mo et al. [78] used zeta potential method to investigate the stability of TiO2 –water nanofluids with three different surfactants SDBS, PVP, and CTAB, respectively. By comparing the value of zeta potential, they obtained the optimal kind of surfactant and the best dispersion of nanofluid. Wei et al. [104] used sedimentation, zeta potential (ζ), and size analysis to evaluate the stability of diathermic oil-based TiO2 nanofluids. They found that there was not obvious sedimentation and the zeta potential (ζ) and size analysis also showed good results. They thought the TiO2 nanofluids they prepared were very stable and can be used to enhance heat transfer for a fluid system. Li et al. [105] used sedimentation observation to investigate the stability of TiO2 –MDEA–water nanofluids. They found that after a specific period of mechanical agitation, the sedimentation was reduced and the stability of nanofluids was improved. However, the ultrasonic vibration will deteriorate the stability of TiO2 –MDEA–water nanofluids. For this reason, only mechanical agitation was employed in their research. Ян и др. [74] investigated the dispersion behavior of 20 types of nanoparticles in binary base fluid of ammonia–water by measuring the absorbency of nanofluids, and they defined ratio of varying absorbency to quantitatively compare the suspending stability of different kinds of nanoparticles, dispersant, and base fluid mixtures. They observed that the new defined index was more applicable than conventional means because it could directly compare the suspending behavior of various kinds of nanofluids. While the method of observing the stratification or sedimentation is restricted for nanofluids in different colors or without distinctly stratification after standing. The results showed that the anatase and rutile TiO2 nanofluid were the most stable metal oxides without any surfactant. And when adding optimal dispersant, anatase TiO2 nanofluid was still the most stable one.
Generally, the combination of several stability evaluating methods is employed to investigate the stability of nanofluids more accurately. Silambarasan et al. [66] used method of measuring the particle size distribution, zeta potential, and microscopy of grain size methods to characterize the suspending stability of TiO2 nanofluids. By those methods, they prepared remarkably stable TiO2 nanofluids whose absorbency changed very little after 10 days. Tajik et al. [86] used sedimentation observation and microscopy of grain size to investigate the roles of ultrasonic wave types on the suspending behavior of nanofluids. And they found that the pulses in discontinues type could not smash some big clusters or aggregations since the sedimentation occurred after 48 h of storage.
Physical Properties of TiO2 Nanofluids
The physical properties of TiO2 nanofluids are focused on the viscosity and thermal conductivity. Also, a few papers investigated the surface tension. Using nanofluids to enhance the thermal conductivity is a typical application in heat transfer filed. Therefore, the thermal conductivity of TiO2 nanofluids will be introduced in part 2 of the reviews. In part 1, the viscosity and surface tension are introduced as follows.
Viscosity
Viscosity is an essential parameter for nanofluids especially for flow and heat transfer applications because both the pressure drop and the resulting pumping power are depended on the viscosity. Viscosity describes the internal resistance of a fluid to flow, and it is an important property for all thermal and flow applications for nanofluids. The nanofluids with higher viscosity will result in higher flow resistance and lower flow velocity, which also induce the decrease of the heat transfer. To obtain flow velocity and heat transfer efficiency, more pumping powers are needed which induce more energy consumption. Moreover, for some mass transfer application of nanofluids, viscosity plays more important roles than thermal conductivity because the viscosity determines the mass transfer resistance of molecules entering the liquid surface and the diffusion coefficient in the liquid. Murshed and Estellé [106] provide a state-of-the-art review on the viscosity of various nanofluids. They found that the experimental data from various literatures are greatly scattered and not consistent even for the same nanofluids. This review will discuss in detail the influence factors on the viscosity of TiO2 nanofluids to provide an exhaustive knowledge on this topic.
Particle Loading Effect
Many literatures have concerned the volume concentration effect on the viscosity of TiO2 nanofluids. Table 3 shows the particle loading dependence of the viscosity of TiO2 nanofluids in different research. It can be observed that the viscosity of the TiO2 nanofluids increases with the increase of the particle loading. However, some works showed that the viscosity ratio varies linearly with variation of volume concentration, but some other results showed the viscosity ratio variation is parabolic. The viscosity enhancements of TiO2 nanofluids were greatly distinguishing in various researches. For example, in Vakili et al. [82], Arulprakasajothi et al. [107], Duangthongsuk and Wongwises [108], Saleh et al. [109], and Mahbubul et al.’s [110] results, the increments of viscosity were below ten times of the volume percentage of the added particles. However, He et al. [111] and Turgut et al.’s [112] results showed that the viscosities were increased by more than 100 times of the volume percentage of the TiO2 particles added. There are also many results distributed between the values in the above two extreme cases. Therefore, it can be concluded that the influence of particle loading on the viscosity of TiO2 nanofluids is more complex than that on thermal conductivity due to the widespread data in various studies.
Temperature Effect
Besides the volume concentration effect, the temperature effect on the viscosity of TiO2 nanofluids is also widely studied by many researchers. He et al. [111] prepared four different concentration TiO2 –H2 O nanofluids with 20 nm TiO2 and measured the viscosities of TiO2 –H2 O nanofluids and deionized water with different temperatures. They observed that the TiO2 –H2 O nanofluids were Newtonian fluids, which were the same as Chang and Liu’s finding [69], and the viscosities varied inversely with the temperature of the TiO2 –H2 O mixture system. Ling et al. [113] also measured the viscosities of the TiO2 –H2 O nanofluids with different mass fractions, when temperature varied from 15 to 40 °C. They found that the viscosity of the nanofluids increased when fluids thicken and decreased with the increment of the temperature exponentially. Лю и др. [114] figured that the viscosities of TiO2 –H2 O nanofluids increase remarkably with the volume fraction of nanoparticles and vary oppositely to the temperature of the TiO2 –H2 O nanofluids greatly with similar experimental method. Based on the value of the viscosities, they also propose an amended suspension viscosity formula. Some research results showed that the viscosity of nanofluids is a function of volume loading and temperature as well as base fluid viscosity. Yiamsawas et al. [115] measured the viscosity of TiO2 –water with a volume loading varied from 1 to 8% at a high-temperature range of 15 to 60 °C. By comparisons with previous studies, they proposed a useful correlation for practical applications which indicated that the viscosity of nanofluids is a function of volume loading and temperature as well as the base fluid’s viscosity.
Comparing with the absolute viscosity, the varieties of relative viscosity at different temperatures were more impressive for researchers. Jarahnejad et al. [93] carried out a detailed study on the effect of temperature on the viscosity and the relative viscosity of TiO2 соответственно. And the results are shown in Fig. 9. It can be found that compared to base water, the average viscosities of TiO2 nanofluids increased by 17, 50, and 78% for 3, 6, and 9 wt.% of particles’ loading, respectively, at 20 °C. The viscosity of nanofluids with different particle loading decreased as the temperature increased, while the relative viscosity remained nearly constant with the temperature. The observation of independent of temperature can be also included in some other research. Fedele et al. [89] presented the characterization of water-based nanofluids where TiO2 ranging between 1 and 35% in mass. They concluded that the relative viscosity was independent from temperature for all the particle loading employed. And the nanofluids at 1 wt.% exhibited a water-like behavior within the experimental error. But this observation was invalid at the higher concentrations (+243% for 35 wt.% at 343 K). Also, Silambarasan et al. [66] found that the temperature has a smaller effect on the relative viscosity since the viscosity of TiO2 suspensions was reproducible even after repeated and alternating heating and cooling processes. And they attributed the reason to the effect of particles’ temperature-dependent intermolecular forces in the suspension. However, some different results can also be observed. Teng et al. [116] found that the relative viscosity increased from 8.2 to 16% when the temperature varied from 10 to 40 °C for the TiO2 nanofluids with 0.5 wt.% of particle loading. Cieśliński et al. [117] found that the relative viscosity of thermal oil-based TiO2 nanofluids remained constant when the temperature varied from 20 to 40 °C, but had a nearly linear increase with the increase of temperature when exceeding 40 °C. Yapici et al. [118] observed that the effect temperature was different for different shear rate. The relative viscosity measured was independent of the temperature at a higher shear rate region. However, for lower shear rate region, a great temperature dependency behavior of viscosity of TiO2 nanofluids was exhibited especially at high temperatures
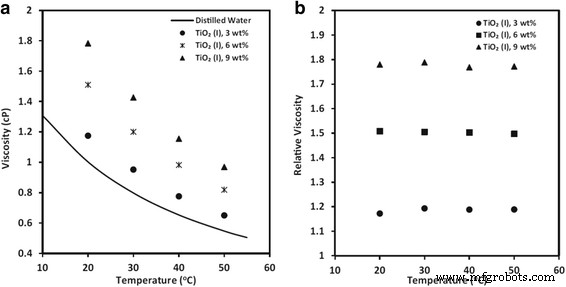
Dynamic viscosity (a ) and relative viscosity (b ) for TiO2 water-based nanofluids at different temperatures [93]. Reproduced with permission from Springer
Particle Size and Shape Effect
The particle size and shape effects on the viscosity of TiO2 nanofluids were not investigated as widely as that of particles’ loading or temperature. In particular, Chen et al. [64, 119] investigated experimentally the viscosity of spherical (25 nm) and rod-like (10 × 100) TiO2 nanoparticle-based nanofluids with water and EG as base fluid, respectively. They found that the viscosity of TiO2 nanofluids was more sensitive to the rod-like particles than spherical particles. It can be seen from Table 3 that the viscosity was increased by 0.5–23% when adding 0.1–1.86 vol.% of spherical TiO2 nanoparticles, while increased by 1–82% when adding 0.1–0.6 vol.% of rod-like TiO2 наночастицы. The same observation can also be found for EG-based nanofluids.
Surfactant Effect
The surfactants have been observed to have great effects on the viscosity of TiO2 nanofluids in some recent research. Jarahnejad et al. [93] investigated the effect of two kinds of surfactant trioxadecane acid and poly carboxylate on the viscosity of TiO2 nanofluids respectively. Their results of the dynamic viscosity of 9 wt.% TiO2 –water nanofluids with different surfactants vs. temperature are shown in Fig. 10. The results demonstrated only a very slight increase was found in the viscosity of nanofluids even with the highest particle loading viz. 9 wt.%. However, the two kinds of surfactants could greatly increase the viscosity of nanofluids in the temperature range of 20–50 °C, especially for trioxadecane acid. The similar effect of surfactant on viscosity can also be observed in Ghadimi and Metselaar’s report [90], in which they found SDS can also increase the viscosity of TiO2 nanofluids with 0.1 wt.% particle loading. It was also observed there were important roles of SDS in the long-term dispersion stability of TiO2 nanofluids. Therefore, they still suggested that the dispersion method of adding surfactant and ultrasonic vibration to be adopted in the preparation of nanofluids.
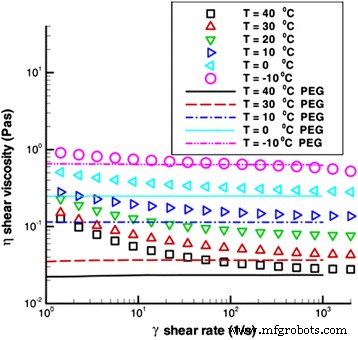
Dynamic viscosity of 9 wt.% TiO2 –water nanofluids with different surfactants vs. temperature [93]. Reproduced with permission from Springer
However, the above results cannot prove that all kinds of surfactant will result in high viscosity for nanofluids. Figure 11 shows the viscosity of TiO2 nanofluids with PEG600 as surfactant measured by Bobbo et al. [120]. It can be seen that the viscosity of base water will not increase but decrease slightly when adding PEG600 at 0.02 or 0.2% loadings. Also, the viscosity of nanofluid containing 0.01% TiO2 nanoparticles and 0.02% PEG600 was a little lower than that of the base water. However, for higher loading of PEG, the viscosity will be greatly increased whether or not containing nanoparticles. It can be seen from Fig. 11 that the nanofluids containing 2% PEG600 and 1% TiO2 nanoparticles showed a viscosity higher than 7% in respect to water, which was analogous at each temperature. The above observation showed the viscosity of nanofluids can be lower than the base fluid in some cases, which also occurred in SWCNT nanofluids in their experiment. The decline of viscosity of fluid when adding surfactant or nanoparticles was also been found in some other research. Ян и др. [121] found that emulsifier OP-10 can reduce the viscosity of ammonia–water in lower concentrations. Ling et al. [122] observed that adding SDBS or OP-10 in TiO2 nanofluids with a lower loading can induce a slight drop in viscosity. Therefore, it is an important issue to choose the suitable surfactants to improve the dispersion stability without increasing the viscosity significantly.
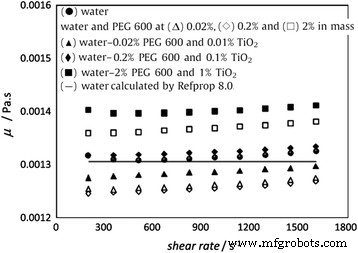
The viscosity of TiO2 nanofluids with PEG600 as surfactant [120]. Reproduced with permission from Elsevier
Base Fluid Effect
The information about base fluid effect on viscosity can be illuminated though Chen et al.’s study [119], in which they found the relative increments of viscosity of water-based TiO2 nanofluids were distinctly higher than that of EG based. It seemed that the higher viscosity the base fluid could result in lower increment in viscosity. Mahbubul et al. [110] found that the viscosity of R123 was increased by only 5.2% when adding 2 vol.% TiO2 наночастицы. Sen et al. [78] and Yapici et al. [118] found relative increments of viscosity about 20 times of the particles’ volume percentages. It also seems that TiO2 nanoparticles are more suitable in the organic liquid because a lower relative increment in viscosity can be obtained especially at the higher temperature. Yiamsawas et al. [123] conducted experiments on a mixture with TiO2 nanoparticles and EG/water (20/80 wt.%) in which the volume loading ranged from 0 to 4% and temperature ranged from 15 and 60 °C. They used the experimental data to present a useful correlation to predict the viscosity.
Shear Rate Effect
Another main distinction on the viscosity of TiO2 nanofluids in different research is that whether the fluids were Newtonian fluids in different shear rates. A typical Newtonian nanofluid can be found in foregoing Fig. 11. However, it can be observed from Table 3 that more than half of the results showed that the TiO2 nanofluids in their work are Newtonian fluids, but some others come to the opposite conclusion. Research on rheological characteristic has demonstrated that whether or not the TiO2 nanofluids exhibit Newtonian behavior is also affected by other factors, including the base fluid type, temperature, and particle loading. A quintessential example can be found in Chen et al.’s research [64], where they measured the viscosity of four types of nanofluids made of TiO2 nanoparticles (25 nm) and TiO2 nanotubes (10 nm × 100 nm) dispersed in water and EG. They found that EG–TiO2 nanofluids exhibited Newtonian behavior, whereas water–TiO2 , water–TNT, and EG–TNT nanofluids exhibited non-Newtonian behavior. They indicated that the rheology behavior of TiO2 nanofluids is affected by their specific ingredient and environment, such as particles’ shape and liquid circumstance. The rheological characteristic of TiO2 nanofluids is also related to the temperature. Yapici et al. [118] investigated the rheological characteristic of 9 wt.% TiO2 –water nanofluids with different surfactants vs. temperature. The results are shown in Fig. 12. It can be observed that the base fluid PEG was a typical Newtonian fluid in all kinds of temperature. However, TiO2 –PEG200 nanofluids were nearly Newtonian fluid at a lower temperature and higher shear rate, but it changed into non-Newtonian fluid at higher temperature and lower shear rates. Also, in Said et al.’s results [94], the TiO2 nanofluid with 0.1 vol.% loading was Newtonian fluid at 55 °C, whereas it was non-Newtonian below this temperature for 0.3 vol.% particle loading.

Shear rate dependency of viscosity as a function of temperature for 5 wt.% TiO2 –PEG200 nanofluids [118]. Reproduced with permission from Springer
Running Time Effect
When the nanofluids are actually used in a running system, the time-dependent properties of nanofluids should be a crucial issue for the sustainable application. However, this matter has not been widely studied because of the faultiness in the development of nanofluids. It is generally considered that the thermal and rheological properties of nanofluids will be deteriorated due to the aggregation of nanoparticles after running a long time in the system. However, an opposite result in the time-dependent viscosity of TiO2 nanofluids can be observed in Said et al.’s research [94]. Their results for viscosity of TiO2 –water nanofluid with different volume loading and temperature as well as running time are shown in Fig. 13. It can be observed that the viscosity of fresh samples and the stale samples after running in a flat plate solar collector for 1 month were distinctly different. The viscosity of TiO2 nanofluids was decreased after undergoing the alternative variations in temperature and flow rate in the cycle. This observation was quite interesting and could not be explained anywhere else in the literature. They thought this finding could open new research scope for the applications of nanofluids for a long-term use.
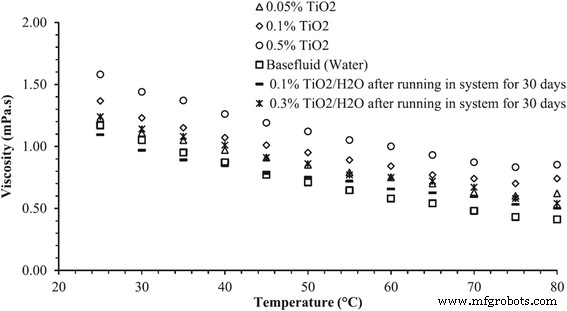
Viscosity of TiO2 –water nanofluid with different volume concentrations and different temperatures [94]. Reproduced with permission from Elsevier
An inconsistency in viscosity of TiO2 nanofluids is quite evident. The intensities of growth in viscosity of TiO2 nanofluids with particle loadings greatly differ in various studies. And there is not yet a universal agreement on the effect of temperature, base fluid, and surfactant on viscosity of TiO2 nanofluids. Moreover, the biggest controversy on viscosity of nanofluid is that whether nanofluid is Newtonian fluid or not. The results in Table 3 exhibit that a substantial part of TiO2 nanofluids in their work are Newtonian fluids, but also, some others exhibit non-Newtonian behavior. The pronounced differences in different samples are mainly due to the complex influence factors on the rheological property. The shear rate has been proved to have great effect on the rheological property, and also, it has combined effect with other factors including temperature, shearing time, particle loading, base fluid type, and particle shape [124], which make it rather difficult to predict whether a nanofluid is Newtonian fluid or not except by experimental means.
Surface Tension of Nanofluids
The research on surface tension of TiO2 –H2 O nanofluids is much less than that of thermal conductivity or viscosity. Some results showed that adding TiO2 nanoparticles had little effect on the surface tension of nanofluids. Лю и др. [125] prepared TiO2 –H2 O nanofluids whose particle size ranged from 11 to 50 nm and the surface tensions TiO2 –H2 O nanofluids were investigated experimentally. They found the surface tension had no obvious change with the increase in particle loading because the surface tension of nanofluids (1% mass fraction) increased only 1.6% compared with deionized water. Hu et al. [126] found the surface tension of TiO2 –H2 O nanofluids increases slightly when adding nanoparticles. And the surface tension decreased as an increase in temperature. Buschmann and Franzke [127] found that no obvious variation occurs when adding a high-volume fraction (5 vol.%) of TiO2 nanoparticles in water. Tian and Wang [128] measured the surface tension of TiO2 –water nanofluids by Jolly balance and abruption method. They found that the surface tension behavior of TiO2 –water nanofluid was the same as water viz. the surface tension decreased as the temperature increases. However, the variation of surface tension is related to the content of nanoparticles. When the content of nanoparticles increases rapidly, the decrease rate of surface tension of TiO2 –water nanofluids will slow down. Ян и др. [129] observed that nanoparticles have little effect but the surfactant can greatly change the surface tension of nanofluids, when the loading of surfactant is below the critical micelle concentration (CMC). And they explained this appearance as follows:The effect of surfactant on the surface tension of liquid is much greater than that of nanoparticles. When adding nanoparticles into a fluid containing surfactant whose loading is below CMC, the “free” surfactant will be absorbed on the surface of nanoparticles and then immersed in the liquid, which can weaken the reducing effect of surfactant on the surface tension of liquids.
However, some results also revealed that the nanoparticles played an indispensable role in the surface tension of nanofluids. Chinnam et al. [130] measured the surface tensions of Al2 О 3 , ZnO, TiO2 , and SiO2 nanofluids with a mixture of 60% propylene glycol and 40% water as base fluids, respectively. They only used one average particle size of 15 nm for TiO2 nanofluid due to limiting of manufacturer. They presented a single correlation as a function of volume loading and particle size as well as temperature for all the nanofluids by statistical analysis based on the experimental results. The experimental and fitting results related to TiO2 nanofluids are shown in Fig. 14. It was observed that the surface tension of nanofluids decreased as the temperature and particle volume loading increase and the correlation perfectly fitted the experimental data. In addition, they also observed that the surface tension decreased as the particle size decrease for a certain loading and temperature of nanofluids except the ZnO nanofluid.
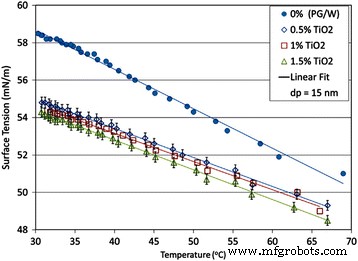
Variation of measured surface tension values of the TiO2 nanofluids with temperature [130]. For different volumetric concentrations up to 1.5% and containing 15 nm particles. Reproduced with permission from Elsevier
Although the surface tension study of nanofluid is not as prevalent as studies in thermal conductivity or viscosity, surface tension is also an important parameter which can affect the film flow especially the initial infiltration of film and the probability of forming channel flow. Due to the effect of surfactant on surface tension of nanofluids is greater than nanoparticles, some researchers thought that the reduction in surface tension by surfactant SDBS can produce a superior enhancement of pool boiling performance in R141b-based nano-refrigerant [131].
Conclusions
The first part of the review focuses on the preparation and two properties viz. viscosity and surface tension of TiO2 nanofluids. It can be concluded that although one-step method is expected to achieve better dispersion stability, the side effects of the one-step method such as producing by-product and requiring special solution environment seem more fatal because they severely restrict the application scope of nanofluids. Suitable treatments such as adding dispersant, adjusting pH values, and physical means (stirring and sonication) used singly or in combination can greatly improve the dispersion stability. And the two-step method is recommended to be employed with appropriate post-treatment for the preparation of TiO2 nanofluids.
Particle loading is positively correlated to the viscosity, but the effects of other factors are not unified. The viscosities greatly differ in different researches which make the viscosity models hard to predict the experimental value, and hence, the experimental mean is firstly recommended. The surface tension of TiO2 nanofluids is more sensitive to surfactant than nanoparticles. The surfactant with low concentration is suggested to be used when it not brings obvious increase in viscosity and foaming ability due to the potential advantages such as reduction in surface tension and improvement in re-dispersible property.
Наноматериалы
- Свойства и использование вольфрамового флюса
- Свойства и применение тантала
- Свойства и соединения рения.
- Получение и магнитные свойства легированных кобальтом наночастиц шпинели FeMn2O4
- На пути к наножидкости TiO2 - Часть 2:Приложения и проблемы
- Подготовка и фотокаталитические характеристики фотокатализаторов LiNb3O8 с полой структурой
- Структурные и оптические свойства в видимой и ближней инфракрасной области спектра TiO2, легированного хромом…
- Магнитные поли (N-изопропилакриламид) нанокомпозиты:влияние метода получения на антибактериальные свойства
- Свойства и назначение:Алюминий Бронза
- Свойства и состав чугуна



