Сенсибилизированные Bi2Se3 нанотрубки TiO2 для фотогенерированной катодной защиты нержавеющей стали 304 в видимом свете
Аннотация
Диоксид титана (TiO 2 ) массивы нанотрубок, связанные с узкозонным полупроводником - селенидом висмута (Bi 2 Se 3 ) - показало значительное улучшение свойств фотокатодной защиты нержавеющей стали 304 в видимом свете. Би 2 Se 3 / TiO 2 нанокомпозиты были успешно синтезированы с использованием простого двухэтапного метода, включая метод электрохимического анодирования для получения чистого TiO 2 и метод химического осаждения из ванны для синтеза Bi 2 Se 3 наноцветки. Морфология и структура композитных пленок исследованы методами растровой электронной микроскопии, энергодисперсионной спектроскопии, рентгеновской фотоэлектронной спектроскопии и рентгеновской дифракции. Кроме того, влияние Bi 2 Se 3 Также исследовали влияние на фотоэлектрохимические и фотокатодные защитные свойства композитных пленок. Плотность фототока Bi 2 Se 3 / TiO 2 нанокомпозитов был значительно выше, чем у чистого TiO 2 в видимом свете. Сенсибилизатор Bi 2 Se 3 улучшено эффективное разделение фотогенерированных электронно-дырочных пар и свойства фотокатодной защиты TiO 2 . При освещении видимым светом Bi 2 Se 3 / TiO 2 нанокомпозиты, синтезированные методом химического осаждения из ванны с Bi 3+ (0,5 ммоль / л) продемонстрировали оптимальные характеристики фотогенерируемой катодной защиты для нержавеющей стали 304.
Фон
В качестве важного конструкционного материала нержавеющая сталь широко применяется в важных проектах во многих областях благодаря своей превосходной коррозионной стойкости. Однако нержавеющие стали могут подвергаться серьезной коррозии при использовании в определенных агрессивных средах, таких как кислотные среды, а также в хлоридсодержащих или высокотемпературных условиях [1,2,3,4]. За последние несколько десятилетий были разработаны обширные исследования и применения традиционных методов защиты от коррозии, включая нанесение покрытий [5, 6], использование протекторного анода [7] и катодную защиту с подаваемым током [8, 9]. Тем не менее, экологическая и долговечная антикоррозионная технология по-прежнему остается основной задачей. В качестве новой технологии защиты от коррозии фотокатодная защита была впервые предложена Юань и Цудзикава в 1995 году [10], прежде чем она привлекла внимание исследователей коррозии [11,12,13,14].
Диоксид титана (TiO 2 ) является важным фотоэлектрическим материалом с хорошими свойствами фотоэлектрического преобразования и фотокатализа и широко используется в катализаторах [15], солнечных элементах [16] и газовых сенсорах [17] из-за его низкой стоимости, нетоксичности и стабильных химических свойств. TiO 2 и TiO 2 композиты на основе фотогенераторов используются для катодной защиты:многообещающий метод защиты от коррозии, который в последние годы быстро развивается [18,19,20,21,22,23]. Однако ширина запрещенной зоны (3,2 эВ) TiO 2 ограничивает фотоотклик только ультрафиолетовой областью, что значительно снижает коэффициент использования солнечной энергии. Кроме того, фотоиндуцированные носители заряда в чистом TiO 2 наночастицы обладают очень коротким сроком службы из-за быстрой рекомбинации фотовозбужденных электронно-дырочных пар, что снижает эффект фотокатодной защиты чистого TiO 2 фильмы. Таким образом, как преодолеть указанные выше недостатки TiO 2 стала широко изучаемой темой. Было проведено множество исследований по приготовлению TiO 2 с неметаллическими элементами (F, N и S) [12, 24, 25], атомами металлов (Fe, Co, Cu и Ce) [26,27,28,29] и некоторыми узкозонными нанополупроводниками (Ag 2 O, ZnSe, WO 3 , CdS, Ag 2 S, CdSe и Bi 2 S 3 ) [30,31,32,33,34,35,36] для улучшения разделения носителей и использования света TiO 2 .
Селенид висмута (Bi 2 Se 3 ) является прямозонным слоистым полупроводником и важным членом V 2 VI 3 составная семья. Он имеет высокий коэффициент поглощения в видимой и ближней инфракрасной областях света с узкой запрещенной зоной (0,35 эВ) [37]. В качестве важного халькогенида n-типа Bi 2 Se 3 обладает многими важными характеристиками, такими как высокая электропроводность [38], заметные термоэлектрические свойства [39], светочувствительность [40], электрохимические свойства [41] и фотопроводимость [42]. Кроме того, Bi 2 Se 3 является популярным топологическим изолятором [43,44,45] и обладает уникальным свойством проводящих поверхностных состояний и изолированных объемных состояний. Качественный Би 2 Se 3 наноструктуры были приготовлены с использованием метода физического осаждения в высоком вакууме, химического осаждения из паровой фазы, осаждения атомных слоев, импульсного лазерного осаждения и метода пар-жидкость-твердое тело при высокой температуре [44,45,46,47,48,49]. Эти синтетические методы для Bi 2 Se 3 требуют сложного изготовления, что приводит к высокой стоимости производства. В этой статье вышеуказанные проблемы преодолеваются за счет использования недорогого и простого метода осаждения Bi 2 в химической ванне. Se 3 осаждение наноцветов на TiO 2 . Комбинация n-Bi 2 Se 3 / н-TiO 2 гетеропереход как эффективный фотоанод впервые применен для фотогенерируемой катодной защиты 304ss. Морфология, структура и свойство оптического поглощения Bi 2 Se 3 / TiO 2 нанокомпозиты были изучены методами сканирующей электронной микроскопии (SEM), рентгеновской дифракции (XRD), энергодисперсионной рентгеновской спектроскопии (EDS), рентгеновской фотоэлектронной спектроскопии (XPS) и спектров диффузного отражения в УФ-видимой (УФ-видимой) области. соответственно.
Методы
Все химические вещества, использованные в этом исследовании, были аналитической чистоты и использовались без дополнительной очистки в том виде, в котором они были получены. Все водные растворы были приготовлены с использованием деионизированной воды.
Подготовка TiO 2 Фильм
Ti-фольгу (20 мм × 10 мм × 0,3 мм; чистота> 99,9%) полировали с использованием смеси, содержащей NH 4 F (2,25 г), H 2 O (12,5 мл), H 2 О 2 (30 мас.%, 30 мл) и HNO 3 (68 мас.%, 30 мл), а затем куски Ti очищали деионизированной водой и этанолом. TiO 2 Пленка была приготовлена на Ti-фольге методом анодного окисления, описанным в литературе [50]. Пластина Pt была выбрана в качестве катода, а фольга Ti была анодом при 20 В в течение 1 часа в растворе этиленгликоля, содержащем NH 4 . F (0,22 г), H 2 O (4 мл) и этиленгликоль (40 мл) при температуре окружающей среды. После этого образцы промывали деионизированной водой и этанолом. Наконец, образцы были отожжены при 450 ° C в течение 2 часов и охлаждены на воздухе до получения TiO 2 фильм.
Синтез Bi 2 Se 3 на TiO 2 Фильм
Би 2 Se 3 был приготовлен методом напыления в химической ванне. В экспериментальной методике 8 ммоль нитрилотриуксусной кислоты (H 3 NTA) и 0,4 ммоль Bi (NO 3 ) 3 · 5H 2 O добавляли к деионизированной воде (400 мл) с образованием хелата висмута с Bi 3+ концентрация 1,0 ммоль / л в смешанном растворе. К вышеуказанному раствору добавляли два миллимоля аскорбиновой кислоты в качестве восстанавливающего реагента, а затем осторожно по каплям добавляли гидроксид аммония до тех пор, пока pH смеси не довелось примерно до 8,6-8,9 и смешанный раствор не стал бесцветным и прозрачным. Наконец, Na 2 SeSO 3 (20 мл, 30 ммоль / л) вводили в указанный выше раствор. Во всех описанных выше экспериментах водные растворы тщательно перемешивали магнитной мешалкой до получения гомогенного раствора. Затем TiO 2 субстрат погружали в конечный раствор (40 мл) в стакан (100 мл). Затем химический стакан, покрытый пищевой пленкой, переносили в печь, нагретую до температуры 80 ° C, на 200 мин для получения Bi 2 Se 3 наноцветок на TiO 2 субстрат. Наконец, образец вынули из стакана и несколько раз промыли деионизированной водой и этанолом, а затем дали высохнуть на окружающем воздухе. Таким образом, Bi 2 Se 3 -чувствительный TiO 2 пленки были получены и помечены Bi 2 Se 3 / TiO 2 -1.0. Для простоты разные количества Bi 2 Se 3 на TiO 2 субстраты обозначены как Bi 2 Se 3 / TiO 2 -γ в этой статье, где γ обозначает концентрацию Bi 3+ в H 3 НТА и Би (NO 3 ) 3 · 5H 2 О раствор. При постоянном количестве других реагентов Bi 2 Se 3 / TiO 2 -0,5 и Bi 2 Se 3 / TiO 2 -0,25 были получены для Bi 3+ концентрации 0,5 ммоль / л и 0,25 ммоль / л соответственно. Влияние разных количеств Bi 2 Se 3 В статье исследованы фотоэлектрохимические и фотокатодные защитные свойства композитных пленок.
Анализ морфологии и композиции
Сканирующая электронная микроскопия (SEM, Hitachi S-4800, Япония) использовалась для исследования морфологии полученных пленок. Для определения химического состава Bi 2 Se 3 / TiO 2 нанокомпозиты. UV-Vis DRS (Japan Hitachi UH4150) использовали для определения светопоглощения образцов. Кристаллический фазовый состав образцов охарактеризован на рентгеновском дифрактометре (XRD, Германия Bruker AXSD8) с использованием Cu K α излучение (γ =1,54056 Å) от 10 ° до 80 °.
Фотоэлектрохимические измерения
Как показано на рис. 1, для фотоэлектрохимических измерений использовалась соединительная система, включающая фотолизные и электролитические ячейки, а для соединения двух ячеек вместе использовалась протонообменная мембрана. Ячейка для фотолиза содержала 0,1 моль / л Na 2 Смешанный раствор S и 0,2 моль / л NaOH, который играл роль жертвенного агента для содействия разделению электронов и дырок [33, 51], а раствор NaCl 0,5 моль / л использовался в качестве электролита для электролитической ячейки. В электролитической ячейке была принята трехэлектродная система с Pt фольгой в качестве противоэлектрода (CE), насыщенным каломельным электродом в качестве электрода сравнения (RE) и 304ss в качестве рабочего электрода (WE). Би 2 Se 3 / TiO 2 Образцы нанокомпозита, помещенные в ячейку для фотолиза, соединялись медной проволокой с электродом из 304ss, погруженным в электролитическую ячейку. Источник света в видимом диапазоне света облучали ксеноновой лампой высокого давления (PLS-SXE 300 C, Beijing Perfectlight Company, Китай). Изменения в кривых потенциала холостого хода (OCP) и фототока измерялись с помощью системы потенциостата / гальваностата / ZRA Gamry (GAMRY 3000, Gamry Instruments, США) до и во время светового облучения.
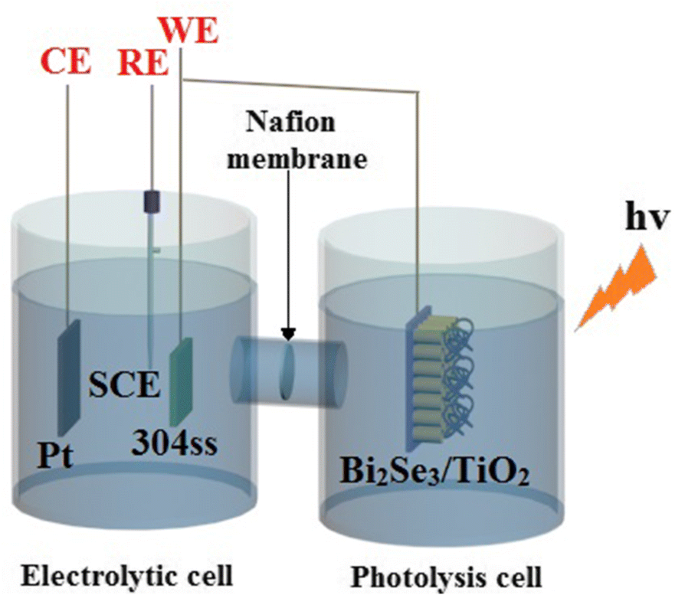
Схематические изображения экспериментальной установки, используемой для фотоэлектрохимического анализа
Результаты и обсуждение
Характеристика чистого TiO2 и Bi2Se3 / TiO2
На рис. 2а показаны типичные вид сверху и топография поперечного сечения для TiO 2 . пленки, полученные методом анодирования. TiO 2 Массивы нанотрубок демонстрируют нанопористую структуру, состоящую из хорошо упорядоченных нанотрубок и нанотрубок высокой плотности со средним внутренним диаметром и длиной приблизительно 55 нм и 680 нм, соответственно. Как показано на рис. 2b – d, TiO 2 поверхности нанотрубок были успешно модифицированы Bi 2 Se 3 с помощью метода осаждения из химической ванны для различных концентраций Bi 3+ . Для Би 2 Se 3 / TiO 2 -0,25, Би 2 Se 3 нанофластинки были спорадически распределены и неравномерно агрегированы по TiO 2 нанотрубки (рис. 2б). Когда концентрация Bi 3+ составляла 0,5 ммоль / л, Bi 2 Se 3 был почти полностью составлен из похожих на цветы узоров гибких ультратонких нано-чешуек диаметром примерно 800 нм, не блокирующих сопло TiO 2 нанотрубок или повреждая их (рис. 2в). Би 2 Se 3 наноцветки, которые, по наблюдениям, были равномерно распределены на поверхности TiO 2 продемонстрировали внутреннюю сшитую структуру для ультратонких нано-чешуек, которая эффективно предотвращает агрегацию ламелей и поддерживает длительный срок службы архитектур, как показано на рис. 2c. После концентрирования Bi 3+ был увеличен до 1,0 ммоль / л, количество и диаметр Bi 2 Se 3 количество наноцветов значительно увеличилось, и агломерация наноцветов заблокировала нанотрубки, как показано на рис. 2d. Соответствующий EDS-спектр Bi 2 Se 3 / TiO 2 Пленки -0,5, показанные на фиг. 2e, показали, что характерные пики для Ti, O, Bi и Se были отмечены с атомным процентным содержанием Bi и Se, равным 0,9% и 1,3%, соответственно. Как известно, погрешность измерения теста EDS увеличивается с уменьшением содержания тестового элемента. Итак, допустимо, чтобы атомное соотношение Bi и Se было близко к 2:3.

Изображения SEM для a чистый TiO 2 , b Би 2 Se 3 / TiO 2 -0,25, с Би 2 Se 3 / TiO 2 -0,5 и d Би 2 Se 3 / TiO 2 -1,0; е Спектр ЭДС для Bi 2 Se 3 / TiO 2 -0,5 фильмов
На рис. 3а показаны рентгеновские дифракционные спектры чистого TiO 2 . (кривая а) и Bi 2 Se 3 / TiO 2 -1,0 нанокомпозитов (кривая б). Помимо пиков подложки Ti, дифракционные пики при 25,38 °, 38,03 °, 48,01 °, 54,05 °, 55,17 °, 62,71 ° и 70,44 ° хорошо согласовывались с плоскостями решетки (101), (004), (200), (105), (211), (204) и (220) анатаза TiO 2 соответственно (JCPDS 21-1272). За исключением TiO 2 пики, характерные дифракционные пики при 29,35 ° и 74,90 ° были привязаны к плоскостям решетки (015) и (0216) ромбоэдрического кристалла Bi 2 Se 3 (JCPDS 33-0214). Однако явного пика Bi 2 нет. Se 3 / TiO 2 -1,0 из-за низкого содержания Bi 2 Se 3 нанесен на TiO 2 и спектры XRD согласуются с результатами SEM и EDS. Рентгеновская фотоэлектронная спектроскопия (XPS) была использована для дальнейшего определения химического состава и состояний Bi 2 Se 3 / TiO 2 нанокомпозиты. Как показано на рис. 3b, XPS выявил наличие компонентов Bi, Se, Ti и O в дополнение к примесям C из-за случайного загрязнения углеводородами. На рисунке 3c показаны положения пиков Ti 2p при 458,7 и 464,5 эВ, что указывает на то, что оксиды титана в основном состояли из TiO 2 . [52]. Как показано на рис. 3d, семафоры O 1s совпадают с двумя гауссовыми пиками:максимум при более низкой энергии связи (530,0 эВ) приписывается решеточному кислороду (O L ) в Bi 2 Se 3 / TiO 2 нанокомпозитов, а второй с более высокой энергией связи (531,5 эВ) был получен из адсорбированного кислорода (O A ), включая слабосвязанные кислородные или гидроксильные группы. Существование O A было связано с образованием кислородных вакансий на поверхности нанокомпозитов, что могло улучшить свойства фотоэлектрического преобразования Bi 2 Se 3 / TiO 2 нанокомпозиты в фотокатодной защите [53]. На рисунке 3e показано, что 4f 7/2 асимметричный пик для Bi разделен на два пика (157,5 и 159,4 эВ) с Bi 4f 5/2 Спектр аналогично разделен на две полосы при 162,8 и 164,7 эВ соответственно. Положение нижних пиков (157,5 эВ и 162,8 эВ) хорошо согласуется с таковыми в Bi 2 . Se 3 , причем более высокие пики соответствуют оксиду висмута при 159,4 и 164,7 эВ [54, 55]. Можно сделать вывод, что небольшое количество металлического висмута окислилось в процессе синтеза с помощью Bi 2 Se 3 модификация чистого TiO 2 . Как показано на рис. 3f, два пика были назначены на 3d 3/2 и 3d 5/2 основные уровни Se при 55,1 и 54,2 эВ, соответственно, что указывает на то, что Se существует в форме Se 2- [56].
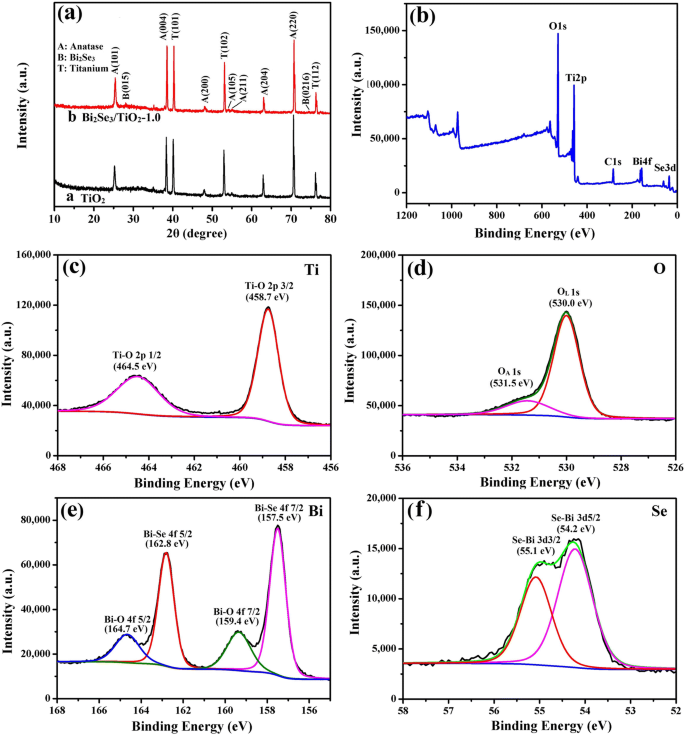
а Картины XRD для чистого TiO 2 и Bi 2 Se 3 / TiO 2 -1,0 нанокомпозитов; б общий спектр обзора, c Ti 2p, d O 1s, e Bi 4f и f Se 3d XPS-спектры Bi 2 Se 3 / TiO 2 -1,0 нанокомпозитов
На рисунке 4 показаны светопоглощающие способности чистого TiO 2 . и Bi 2 Se 3 / TiO 2 -1,0 нанокомпозитов. Характерный край поглощения для чистого TiO 2 составляла примерно 380 нм в УФ-области из-за запрещенной зоны анатаза TiO 2 (3,2 эВ) (кривая а). Выраженная адсорбция наблюдалась для Bi 2 . Se 3 / TiO 2 нанокомпозиты в области видимого света (350–800 нм) (кривая b), обладающие более высокой способностью поглощения видимого света, чем у чистого TiO 2 за счет включения Bi 2 Se 3 наноцветок. Это явление можно объяснить тем, что Bi 2 Se 3 возбуждается в видимом свете из-за своей узкой запрещенной зоны (0,35 эВ), а электроны и дырки образуются в его зоне проводимости (CB) и валентной зоне (VB). Следовательно, добавление Bi 2 Se 3 эффективно увеличивает способность Bi 2 поглощать видимый свет Se 3 / TiO 2 нанокомпозиты.
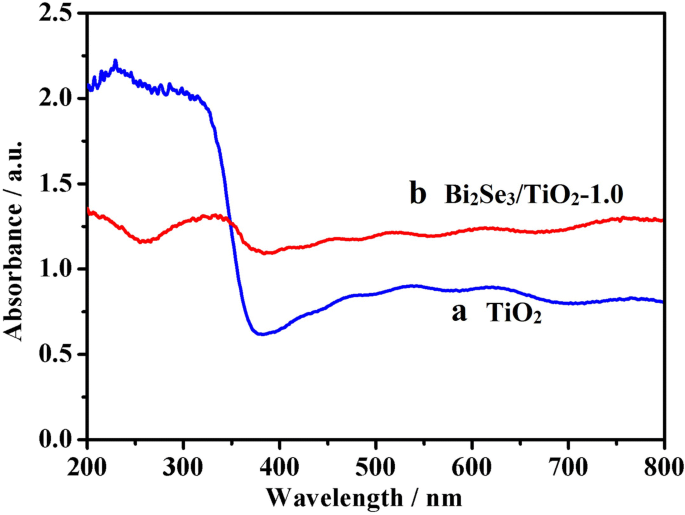
Спектры поглощения в УФ и видимой областях для TiO 2 (а) и Bi 2 Se 3 / TiO 2 -1,0 (б)
Характеристики фотокатодной защиты чистого TiO2 и Bi2Se3 / TiO2
Как показано на рис. 5, кривые OCP для 304ss в сочетании с чистым TiO 2 и Bi 2 Se 3 / TiO 2 Нанокомпозитные фотоаноды измерялись в прерывистом видимом свете, при этом реакция ОСР на освещение вызывалась и сдвигалась к отрицательному потенциалу для всех связанных электродов. В начальной фазе включения света ОСР для всех связанных электродов показала отрицательный сдвиг за короткое время, что было связано с переносом возбужденных фотоэлектронов из чистого TiO 2 и Bi 2 Se 3 / TiO 2 нанокомпозита к электроду 304ss [1, 57]. Следовательно, относительно стабильные значения ОСР можно объяснить балансом между созданием и рекомбинацией фотогенерированных электронов [32]. После выключения облучения значения ОСР для Bi 2 Se 3 / TiO 2 нанокомпозиты возвращались к исходным значениям с меньшей скоростью по сравнению с чистым TiO 2 . Это явление может быть связано с эффектом электронного пула Bi 2 Se 3 / TiO 2 нанокомпозиты, которые могут накапливать фотоиндуцированные электроны под действием света и медленно высвобождать эти электроны без облучения светом. При облучении видимым светом значение ОСР для 304ss составляло приблизительно -450 мВ в сочетании с TiO 2 . (кривая a), и значения OCP для 304ss в сочетании с Bi 2 Se 3 / TiO 2 -0,25 (кривая b), Bi 2 Se 3 / TiO 2 -0,5 (кривая d) и Bi 2 Se 3 / TiO 2 -1,0 (кривая в) достигла - 905 мВ, - 996 мВ и - 958 мВ соответственно. Эти результаты показали, что 304ss был катодно поляризован после связывания с Bi 2 Se 3 / TiO 2 нанокомпозитов и что хорошая катодная защита для 304ss может быть обеспечена за счет Bi 2 Se 3 / TiO 2 фотоаноды. Как показано на Рис. 5d, 304ss, соединенный с Bi 2 Se 3 / TiO 2 -0,5 обладал наибольшим отрицательным потенциалом, что указывает на лучшие характеристики фотокатодной защиты для 304ss. Этот результат может быть вызван тем, что активные центры и сбор света увеличиваются с увеличением Bi 2 Se 3 содержание. Однако чрезмерное количество Bi 2 Se 3 частицы служили сайтами рекомбинации для электронов и дырок, что затрудняло перенос заряда от Bi 2 Se 3 / TiO 2 нанокомпозиты до 304сс.
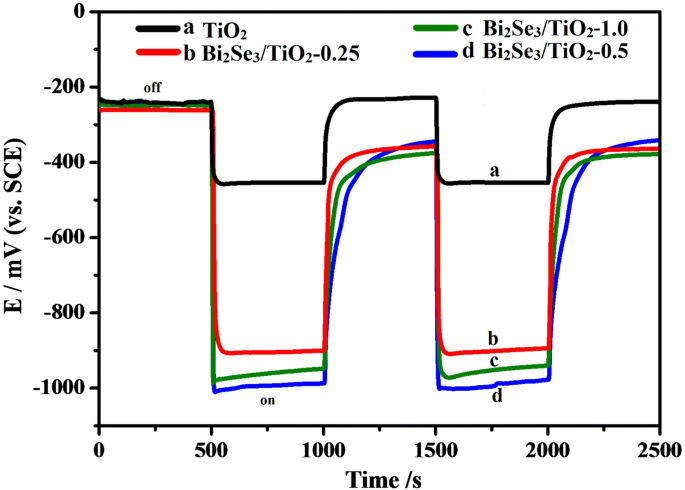
OCP для 304ss в сочетании с чистым TiO 2 и Bi 2 Se 3 / TiO 2 нанокомпозиты в 0,5 моль растворе NaCl
Как показано на рис. 6, зависимости плотности фототока от времени для TiO 2 и Bi 2 Se 3 / TiO 2 Нанокомпозиты показали быстрый и воспроизводимый фотоотклик при прерывистом освещении видимым светом, что отражало характеристики фотоэлектрического преобразования материалов. Фотогенерируемый ток был относительно небольшим в видимом свете из-за слабого поглощения видимого света (кривая а). Однако фотогенерируемый ток заметно увеличивается при освещении видимым светом после сенсибилизации TiO 2 автор Би 2 Se 3 наноцветок (кривые от b до d). Данные подразумевали, что Bi 2 Se 3 / TiO 2 нанокомпозиты способны использовать видимый свет, и что гетеропереход между TiO 2 и Bi 2 Se 3 способствовал разделению фотогенерированных электронов и дырок [58]. Кроме того, фотоэлектроны, образующиеся в зоне проводимости Bi 2 Se 3 наноцветок может быть легко перенесен в более положительную зону проводимости TiO 2 нанотрубки при освещении видимым светом. После трех интервалов облучения фототок поддерживал относительно стабильное значение, и деградации фототока не было обнаружено, что свидетельствует о хорошей фотохимической стабильности Bi 2 Se 3 / TiO 2 нанокомпозитные пленки. Для разных концентраций Bi 3+ , Би 2 Se 3 / TiO 2 нанокомпозиты показали различную интенсивность фототокового отклика. В частности, переходная плотность фототока для Bi 2 Se 3 / TiO 2 -0,5 (415 мкА / см 2 ) был выше, чем для Bi 2 Se 3 / TiO 2 -0,25 (85 мкА / см 2 ) и Bi 2 Se 3 / TiO 2 -1,0 (160 мкА / см 2 ), указывая на то, что Bi 2 Se 3 / TiO 2 -0,5 обладает идеальной эффективностью разделения фотогенерированных электронно-дырочных пар. Активные центры и сбор света были уменьшены из-за дефицита Bi 2 Se 3 наноцветки на Bi 2 Se 3 / TiO 2 нанокомпозитных пленок, в то время как сайты рекомбинации для электронов и дырок увеличиваются в присутствии избыточного количества Bi 2 Se 3 наноцветки. При освещении видимым светом самая большая фотоиндуцированная плотность тока Bi 2 Se 3 / TiO 2 -0,5 фотоанод соответствовал самым большим фотоиндуцированным падениям потенциала, показанным на рис. 5, что дополнительно подтверждает оптимальные характеристики фотокатодной защиты Bi 2 Se 3 / TiO 2 -0,5 для 304сс.
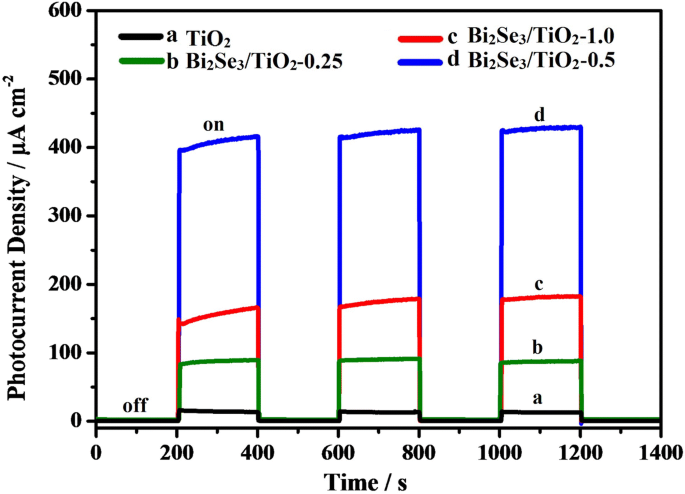
Кривые зависимости плотности фототока от времени для чистого TiO 2 и Bi 2 Se 3 / TiO 2 нанокомпозиты в 0,1 моль / л Na 2 Смешанный раствор S и 0,2 моль / л NaOH
На рисунке 7 показаны процессы фотоэлектрического преобразования и транспортировки Bi 2 . Se 3 / TiO 2 нанокомпозиты. В видимом свете Bi 2 Se 3 наноцветки могут легко поглощать фотоны, поскольку они содержат адсорбированный кислород (O A ) и имеют узкую ширину запрещенной зоны (0,35 эВ). Когда фотоны поглощаются Bi 2 Se 3 наноцветки, фотовозбужденные электроны будут генерироваться возбуждением из валентной зоны (VB) Bi 2 Se 3 в зону проводимости (ЗП) Bi 2 Se 3 . Фотовозбужденные электроны в КП Bi 2 Se 3 сдвинуты в CB TiO 2 , в то время как фотогенерированные дыры в VB TiO 2 переносятся в VB Bi 2 Se 3 , а затем захватываются S 2− в электролите превратиться в S на поверхности фотоанодной пленки. Когда фотовозбужденные электроны покидают фотоанод и переходят на 304ss, они вступают в реакцию с кислородом и водой с преобразованием OH - . Кроме того, Na + транспортируется от электролитической ячейки к фотолизной ячейке через протонообменную мембрану, так что соединительная система в целом электрически нейтральна. Как следствие, фотогенерированные заряды эффективно разделяются, и вероятность рекомбинации фотогенерированных электронно-дырочных пар снижается. Как только 304ss получает фотовозбужденные электроны от Bi 2 Se 3 / TiO 2 нанокомпозита через проволоку потенциал 304ss смещается в отрицательную сторону. При освещении видимым светом Bi 2 Se 3 / TiO 2 нанокомпозиты могут снизить скорость коррозии 304ss. Следовательно, эффективное разделение фотовозбужденных электронно-дырочных пар в Bi 2 Se 3 / TiO 2 нанокомпозиты ускоряют окислительно-восстановительную реакцию и создают эффективную фотокатодную защиту для 304ss.
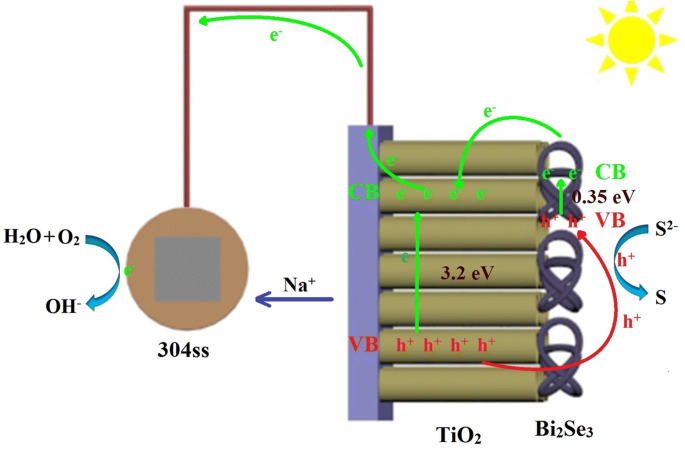
Схематическое изображение процессов переноса электрона в Bi 2 Se 3 / TiO 2
Выводы
В этой статье TiO 2 Массивы нанотрубок были приготовлены методом анодирования и Bi 2 Se 3 наноцветки выращивали на TiO 2 нанотрубки путем химического осаждения из ванны. Би 2 Se 3 / TiO 2 нанокомпозиты показали однородное распределение и упорядоченные характеристики. Электрохимические испытания нанокомпозитов и чистого TiO 2 в сочетании с 304ss показали, что характеристики фотогенерируемой катодной защиты Bi 2 Se 3 / TiO 2 нанокомпозиты были лучше, чем для чистого TiO 2 . Значение OCP для 304ss в сочетании с Bi 2 Se 3 / TiO 2 -0,5 показал отрицательный сдвиг до -996 мВ при освещении видимым светом из-за активных участков и сбора света TiO 2 сенсибилизирован Би 2 Se 3 . Путем сравнения результатов электрохимических испытаний для трех Bi 2 Se 3 / TiO 2 нанокомпозиты, нанокомпозит, приготовленный с использованием 0,5 ммоль / л Bi 3+ в электролите демонстрирует оптимальные характеристики.
Сокращения
- 304ss:
-
Нержавеющая сталь 304
- CB:
-
Полоса проводимости
- CE:
-
Противоэлектрод
- EDS:
-
Энергодисперсионная рентгеновская спектроскопия
- H 3 NTA:
-
Нитрилотриуксусная кислота
- OA:
-
Адсорбированный кислород
- OCP:
-
Потенциал холостого хода
- OL:
-
Решеточный кислород
- RE:
-
Электрод сравнения
- SCE:
-
Насыщенный каломельный электрод
- SEM:
-
Сканирующая электронная микроскопия
- УФ-видимый:
-
УФ-видимые спектры диффузного отражения
- VB:
-
Группа валентности
- МЫ:
-
Рабочий электрод
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Выбор нержавеющей стали для высокотемпературных применений
- Дифференциация нержавеющей стали 304 и 316
- Фотокаталитическая активность, усиленная Au-плазмонными наночастицами на фотоэлектроде нанотрубки TiO2, покры…
- Структурные и оптические свойства в видимой и ближней инфракрасной области спектра TiO2, легированного хромом…
- Простой метод загрузки наночастиц CeO2 на массивы анодных нанотрубок TiO2
- Хорошо выровненные массивы нанотрубок TiO2 с наночастицами Ag для высокоэффективного обнаружения ионов Fe3 +
- Модификация Cu2-xSe на Monoclinic BiVO4 для повышения фотокаталитической активности в видимом свете
- Пассивация деталей и корпусов из нержавеющей стали
- Наиболее распространенные области применения нержавеющей стали
- Прецизионные металлы для производителей



