Цельнометаллический биосенсор терагерцового метаматериала для обнаружения белков
Аннотация
В данной статье теоретически исследуется и экспериментально проверяется терагерцовый (ТГц) биосенсор на основе цельнометаллического метаматериала. В этом биосенсоре из метаматериалов ТГц диапазона используются материалы из нержавеющей стали, которые производятся с помощью технологии лазерного сверления. Результаты моделирования показывают, что максимальная чувствительность по показателю преломления и добротность этого датчика из метаматериала составляют 294,95 ГГц / RIU и 4,03 соответственно. Затем в качестве детектирующего вещества для оценки эффективности этого биосенсора был выбран бычий сывороточный альбумин. Результаты эксперимента показывают, что чувствительность обнаружения составляет 72,81 ГГц / (нг / мм 2 ) с пределом обнаружения 0,035 мг / мл. Этот биосенсор из метаматериала ТГц диапазона прост, рентабелен, прост в изготовлении и имеет большой потенциал в различных приложениях биосенсора.
Введение
В настоящее время врачи обычно собирают сыворотку у пациентов в больнице для различных обследований. Такие как обнаружение опухолей [1,2,3] и обнаружение вирусов [4,5,6] и т. Д. Предварительным методом обнаружения опухолей является обнаружение белков, потому что белки являются компонентами многих онкомаркеров, и эти биомолекулы с большим количеством информация существует в сыворотке. Альбумины сыворотки являются наиболее распространенными (52–62%) общими белками водорастворимой фракции в плазме крови [7, 8]. Кроме того, пищевые и физиологические функции сывороточных альбуминов делают их важными биомакромолекулами. Как один из самых популярных сывороточных альбуминов, бычий сывороточный альбумин (БСА) используется во многих областях исследований. Поэтому исследования по обнаружению BSA очень важны. Существует множество методов обнаружения и определения концентрации BSA, включая спектроскопию электрохимического импеданса [9], капиллярный электрофорез [10] и методы светорассеяния [11]. Но все они имеют некоторые недостатки, такие как сложные процедуры, плохая воспроизводимость или трудоемкость. Поэтому разработка новых биосенсоров имеет большое значение и пользуется большим спросом.
Волна ТГц находится между микроволновой и инфракрасной оптической волной и в переходной области от электроники к фотонике. По сравнению со световыми волнами энергия фотонов в этой полосе очень мала. Это означает, что терагерцовые волны не вызывают радиационного ионизационного повреждения биологических молекул. Многие биологические макромолекулы также имеют уникальные отпечатки пальцев в терагерцовом диапазоне [12,13,14,15]. Таким образом, терагерцовым волнам уделяется большое внимание в области биосенсоров [16, 17].
Метаматериалы - это искусственные электромагнитные материалы, состоящие из субволновых структур. Их уникальный электромагнитный резонанс имеет множество характеристик, таких как отрицательный RI [18, 19], электромагнитно-индуцированная прозрачность [20, 21] и чрезвычайная чувствительность к окружающей среде [22, 23]. Метаматериалы, чувствительные к окружающей среде, особенно те, которые состоят из субволновых металлических структур [24,25,26], широко используются для обнаружения различных биомолекул. Комбинация терагерцовых волн и метаматериалов обеспечивает новый метод обнаружения биомедицинских молекул, который не только обеспечивает обнаружение без меток, но и обновляет предел разрешения существующих датчиков. Кроме того, обнаружение может быть выполнено просто и быстро с использованием небольшого количества анализируемого вещества без химических реагентов.
На частотах ТГц производство метаматериалов обычно основывается на методах обработки на микронном уровне. Фотолитография [27] или электронно-лучевая литография [28] в основном используется для переноса микронано-рисунков с фоторезистора на поверхность функциональных материалов, а затем требуется влажное [29, 30] или сухое травление [31, 32] для завершить окончательную обработку метаматериалов. Посредством вышеуказанных шагов может быть достигнуто построение точной графики, но, к сожалению, для большинства этих методов требуется дорогостоящее оборудование для обработки, высокие стандарты операционной среды и громоздкие процедуры обработки. Лазерное сверление [33, 34] - это первая практическая технология лазерной обработки, а также одна из основных областей применения лазерной обработки. Лазерный луч сильно сконцентрирован в пространстве и времени. За счет фокусировки линзой диаметр пятна можно уменьшить до микронного уровня, а плотность мощности лазера - до 10 5 . –10 15 Вт / см 2 может быть получен. Благодаря такой высокой плотности мощности лазерное сверление можно производить практически в любом материале. Насколько нам известно, это первый случай применения технологии лазерного сверления при изготовлении биосенсоров из метаматериалов, которые могут значительно снизить стоимость обработки биосенсоров из метаматериалов и способствовать их практическому применению.
В этом исследовании был предложен, теоретически смоделирован и экспериментально продемонстрирован высокочувствительный терагерцовый биосенсор для обнаружения белков на основе цельнометаллического метаматериала. Устройство было простым в изготовлении, рентабельным и достаточно стабильным. Он был изготовлен из нержавеющей стали с использованием технологии лазерного сверления. Сначала этот датчик из метаматериала был смоделирован и проанализирован с использованием метода конечных интегралов, а также рассчитана чувствительность показателя преломления. Затем был изготовлен и измерен этот ТГц метаматериальный биосенсор. Эксперименты подтвердили высокую чувствительность этого сеньора к внешней среде. BSA был выбран в качестве детектирующего вещества для оценки эффективности биосенсора. Формула Хилла использовалась для соответствия экспериментальным данным. Чувствительность обнаружения 72,81 ГГц / (нг / мм 2 ) и предел обнаружения (LOD) 0,035 мг / мл. Измерения были повторены трижды для проверки надежности биосенсора.
Дизайн
На рис. 1а представлена структура предлагаемого терагерцового биосенсора из цельнометаллического метаматериала. Полый узор гантели с периодическим расположением вдоль направлений x и y был сформирован на пластине из нержавеющей стали толщиной 50 мкм (проводимость 1,4 × 10 6 См / м). Размеры периода P x и P y единичной структуры составляют 500 мкм и 300 мкм соответственно. Длина полой гантели L и пробел H составляют 294 мкм и 60 мкм соответственно. Радиус R кругов на обоих концах полой гантели составляет 60 мкм. Биосенсор имел цельнометаллическую конструкцию и не имел традиционной диэлектрической подложки. Терагерцовая волна падает перпендикулярно поверхности биосенсора из метаматериала.
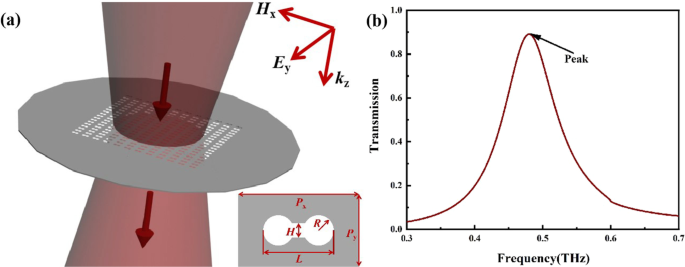
а Трехмерная диаграмма массива и диаграмма структуры ячеек биосенсора. Структурные параметры: P x =500 мкм, P y =300 мкм, L =294 мкм, H =60 мкм, R =60 мкм. б Имитация передачи биосенсора
Методы и моделирование
Затем трехмерное моделирование полноволнового электромагнитного поля с помощью метода конечных интегралов (коммерческое программное обеспечение CST) было использовано для следующих расчетов. Периодические граничные условия применялись в x и y направлениях, и идеально согласованный слой использовался в направлении распространения волны z . Как показано в правом верхнем углу рис. 1а, волновой вектор падающего электромагнитного поля k z была плоская волна, распространяющаяся в z -оси, электрическое и магнитное поля поляризованы вдоль оси y -axis и x -оси соответственно. Как показано на рис. 1b, был пик передачи на 0,48 ТГц.
Для изучения физического механизма генерации этого резонансного пика были смоделированы поверхностный ток биосенсора и магнитное поле на частоте резонансного пика. Как показано в левой части рис. 2, падающие электромагнитные волны были поляризованы вдоль y ось, вызывая колебания заряда на обоих концах отверстия, в результате чего возникает электрический диполь. Колебания заряда сопровождались колебаниями тока в противоположных направлениях вдоль кромок двух круглых отверстий, составляющих отверстия. Это привело к паре встречно ориентированных и не лежащих в плоскости магнитных диполей. Как показано на правой стороне рис. 2, в z была пара явно противоположных магнитных диполей. ось соединена встык, образуя тороидальный диполь. Следовательно, в реакции метаматериала преобладала комбинация электрических и тороидальных диполей.
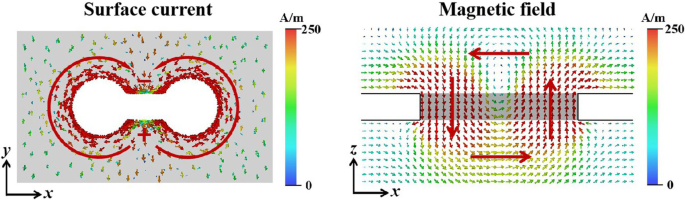
Смоделированная диаграмма распределения поверхностного тока и диаграмма распределения магнитного поля (y =0 мкм) на частоте 0,48 ТГц
Поскольку характеристики датчика зависят от параметров конструкции, необходимо оптимизировать структурные параметры во время процедуры проектирования. На рис. 3 показано влияние изменения структурных размеров на спектры пропускания. Как показано на рис. 3а, когда длина полой гантели увеличилась с 290 до 298 мкм, пиковая частота спектров пропускания сместилась в красную область с 0,48 ТГц. Как показано на рис. 3b, когда зазор полой гантели увеличился с 56 до 64 мкм, пиковая частота спектров пропускания сместилась в синий цвет с 0,48 ТГц. Как L и H увеличился, пик резонанса начал двигаться в сторону низкой и высокой частоты соответственно. При изменении радиуса круга от 56 до 64 мкм и толщины нержавеющей стали от 40 до 60 мкм положение резонансного пика несколько изменилось. Следовательно, легче настроить резонансную частоту биосенсора из метаматериала, отрегулировав длину полой гантели L и разрыв полой гантели H.
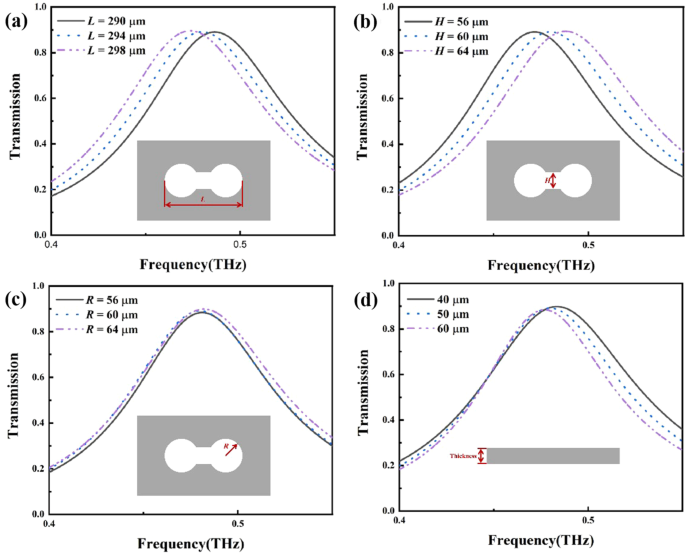
Спектры пропускания a разная длина L , b разрыв H , c радиус R , и d толщина листа нержавеющей стали
Также очень важно изучить влияние угла падения и угла поляризации на спектры пропускания. Электромагнитная волна падала вертикально, а затем менялись угол падения и поляризации. Определение этих углов показано на рис. 4а. Угол падения означает θ я в плоскости y – z, а поляризация равна θ p в плоскости x – y. Как показано на рис. 4b, когда угол падения изменился с 0 ° на 15 °, разница в частоте резонансного пика составила всего 9 ГГц. Как показано на рис. 4c, когда угол поляризации увеличился с 0 ° до 15 °, разница в частоте пика резонанса составила почти 0 ГГц, но амплитуда пика резонанса уменьшилась примерно на 0,1. Это показало, что биосенсор практически нечувствителен к изменениям угла падения и поляризации, что полезно для практических приложений биосенсора.
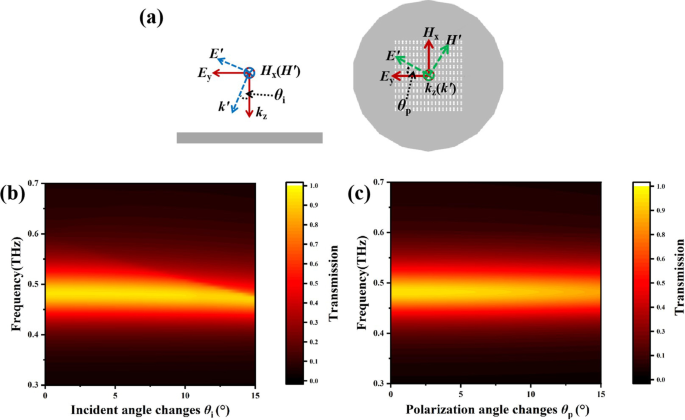
а Принципиальная схема изменения угла падения θ я и угол поляризации θ p . Спектры пропускания в зависимости от b угол падения и c угол поляризации
Чтобы исследовать сенсорную способность биосенсора, к этому биосенсору из метаматериала был добавлен тонкий слой анализируемого вещества толщиной 120 мкм, как показано на рис. 5а, затем были смоделированы различные спектры пропускания этого биосенсора из метаматериала, когда показатель преломления анализируемого вещества изменился, как показано на рис. . 5b. Чувствительность RI S был определен как отношение вариаций положения пика передачи к блоку RI ( S =Δ f / Δ п ). По мере увеличения RI аналита частота резонансного пика сдвигалась в красную область. Затем собирали сдвиг частоты резонансного пика, соответствующий каждому RI. Наблюдалась хорошая линейность. Результат подгонки на рис. 5c показывает, что чувствительность к RI составила 294,95 ГГц / RIU.
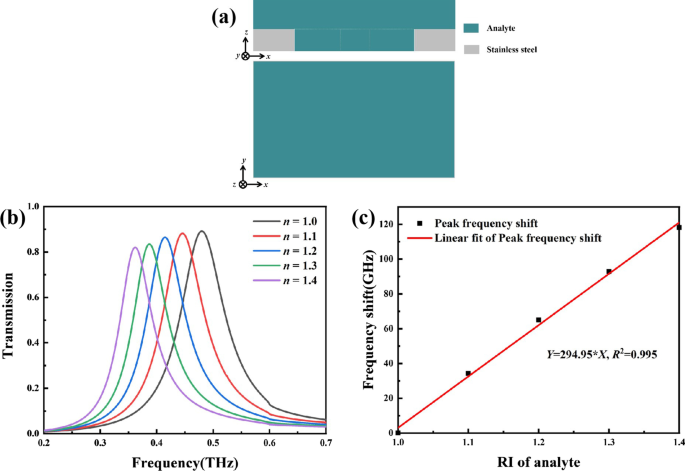
а Поперечное сечение и вид сверху схемы модели биосенсора из метаматериала с тонким слоем анализируемого вещества 120 мкм. б Влияние изменений RI аналита на спектры пропускания биосенсора. c Соответствующая линейная аппроксимация частотного сдвига пика с соответствующим RI
Эффективность зондирования также оценивалась количественно с использованием показателя качества (FOM), который был определен как:
$$ {\ text {FOM}} =\ frac {S} {{{\ text {FWHM}}}} $$ (1)где S - чувствительность, а FHWM - полная ширина на половине максимума резонансного пика. FOM этого биосенсора составлял 4,03.
Для большинства структур из метаматериалов в качестве подложек обычно используются диэлектрические материалы. Однако этот биосенсор из метаматериала, предложенный в этой статье, был основан на цельнометаллическом метаматериале, полностью сделанном из нержавеющей стали, а в качестве субстрата использовался воздух. По сравнению с традиционными диэлектрическими материалами, такими как полиэтилентерефталат (ПЭТ), кварц и кремний, воздух имеет самый низкий RI. Чтобы оценить роль субстрата, эти биосенсоры из метаматериалов были снова смоделированы с использованием различных субстратов, а затем были рассчитаны чувствительность показателя преломления и значения FOM. Как показано на рис. 6, по мере увеличения RI подложки чувствительность RI датчика и FOM начали уменьшаться. Этот результат показал, что биосенсор с более низким RI субстрата имел лучшую чувствительность.
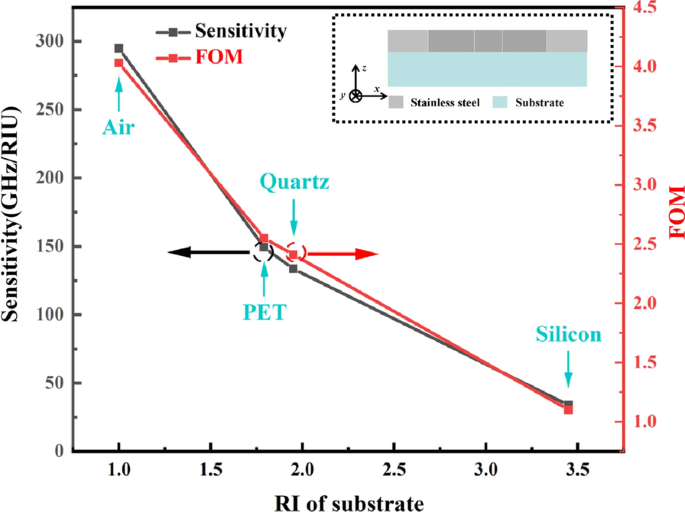
Чувствительность и FOM при использовании разных субстратов
Для дальнейшего исследования принципа восприятия биосенсора были смоделированы диаграммы распределения электрического поля, как показано на рис. 7. Вид сверху и сбоку моделированного распределения электрического поля продемонстрировал, что энергия электрического поля была в основном сконцентрирована в части нержавеющей стали. дыры. Поэтому очень важно убедиться, что аналит был добавлен в отверстия.
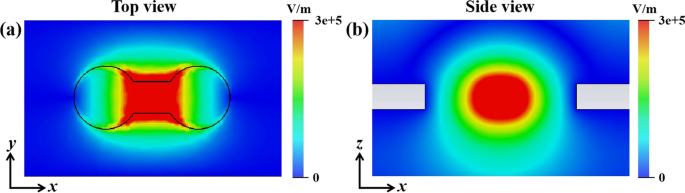
Моделирование распределения электрического поля. а Вид сверху, b вид сбоку ( y =0 мкм)
В таблице 1 обобщены чувствительность RI и FOM предложенного датчика, и они сравниваются с другими опубликованными исследованиями [35,36,37]. Все остальные ТГц сенсоры основаны на традиционных процессах фотолитографии. Видно, что разработанный нами биосенсор из метаматериала из нержавеющей стали имел отличные характеристики обнаружения с использованием дешевой технологии лазерного сверления.
Эксперимент
Материалы и подготовка образцов
Затем, чтобы продемонстрировать биосенсорную способность предложенного ТГц-метаматериального сенсора, в эксперименте было проведено детектирование белка. И BSA, и буфер PBS были приобретены у Sigma-Aldrich. Раствор BSA был приготовлен в буфере PBS (pH =7,4).
Микроскопическое изображение изготовленного биосенсора из метаматериала показано на рис. 8. Общий размер биосенсора из метаматериала составлял 12 мм × 12 мм.

Микрофотография изготовленного образца биосенсора
Концентрации приготовленного раствора BSA составляли 0,2 мг / мл, 0,5 мг / мл, 2,0 мг / мл и 4,0 мг / мл. Анализируемое вещество добавляли на поверхность биосенсора методом жидкого осаждения. Каждый раз 150 мкл раствора BSA переносили на поверхность биосенсора с помощью пистолета для пипеток, и биосенсор сушили на нагревательном столе при 40 ° C. Когда биосенсор нагревали до 40 ℃, белковая пленка формировалась быстрее и равномернее. Каждый раз перед изменением различных концентраций раствора BSA лист из нержавеющей стали помещался в деионизированную воду и подвергался вибрации в ультразвуковом вибраторе, чтобы убедиться, что белковая пленка от предыдущего процесса очищена и поверхность этого биосенсора из метаматериала чиста. На рис. 9 показаны изображения и изображения, полученные под микроскопом, процесса добавления и сушки белка. Как показано на рис. 9a, лист из нержавеющей стали был чистым, а затем, как показано на рис. 9b, раствор BSA одной концентрации был добавлен на поверхность листа из нержавеющей стали, и раствор оставался на поверхности этого биосенсора и не действовал. проходят через отверстия за счет действия поверхностного натяжения воды. После нагревания и сушки образовался тонкий слой пленки BSA, как показано на рис. 9c.

Фотографии нержавеющей стали на разных этапах тестирования:биосенсор из метаматериала после a ультразвуковая очистка и сушка, б добавление 150 мкл раствора BSA (0,2 мг / мл) и c сушка; Фотографии под микроскопом d листа из нержавеющей стали боковина и е поверхность перед добавлением BSA; Фотографии под микроскопом f листа из нержавеющей стали боковина и g поверхность после добавления и сушки раствора BSA (0,2 мг / мл)
Чтобы наблюдать за ситуацией внутри отверстий из нержавеющей стали, одна сторона нержавеющей стали была отрезана, так что одна сторона отверстий была обнаружена и наблюдалась под микроскопом. Как показано на рис. 9d – g, когда раствор BSA был закапан и высушен, тонкий слой BSA был добавлен в отверстия из нержавеющей стали, что в основном связано с тем, что диаметр отверстий намного больше, чем размер отверстия Белки БСА. Это доказывает, что определяемый аналит может попасть в чувствительную к обнаружению область нашего биосенсора, что может значительно повысить чувствительность этого биосенсора из метаматериалов.
Спектральные измерения
Все спектральные измерения проводились с использованием системы непрерывной ТГц спектроскопии (TeraScan 1550, Toptica Photonics AG). Система состояла из интеллектуальной электроники с двойным лазерным управлением (DLC), двух лазеров с распределенной обратной связью (DFB), двух фотомиксеров InGaAs с волоконной связью и четырех внеосевых параболических зеркал 90 °, как показано на рис. 10. ТГц волны были коллимированы и фокусировалась на образце через внеосевые параболические зеркала 90 °. Все спектры пропускания были получены путем сканирования в диапазоне от 50 до 1220 ГГц с шагом 40 МГц со временем интегрирования 10 мс в режиме быстрого сканирования для сокращения времени сканирования. Поляризация терагерцовой волны происходила вдоль направления раскрытия кольца гантели.
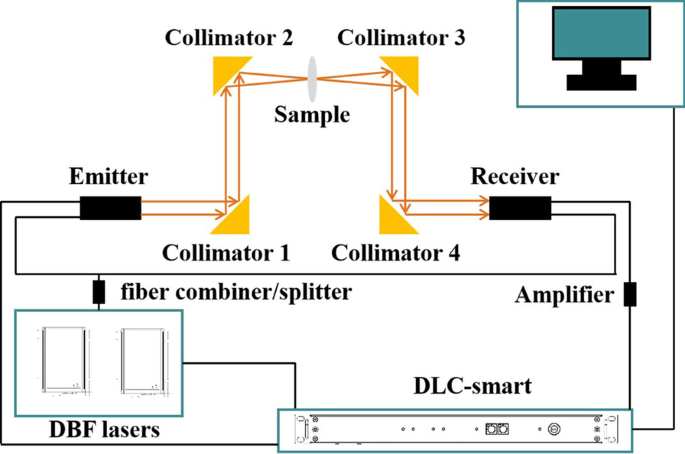
Принципиальная схема ТГц спектрометра непрерывного излучения, использованного в наших экспериментах
Результаты эксперимента и обсуждение
Эксперименты по обнаружению белка биосенсором из метаматериалов проводились с четырьмя концентрациями растворов BSA. На протяжении экспериментов каждую группу растворов BSA добавляли в порядке от низкого к высокому. Все измерения были повторены трижды.
Как показано на фиг. 11а, по мере увеличения концентрации растворов БСА частота резонансного пика сдвигалась в красную область. Эта тенденция согласуется с результатами моделирования. Уменьшение интенсивности резонанса связано с поглощением терагерцовой волны белком БСА.
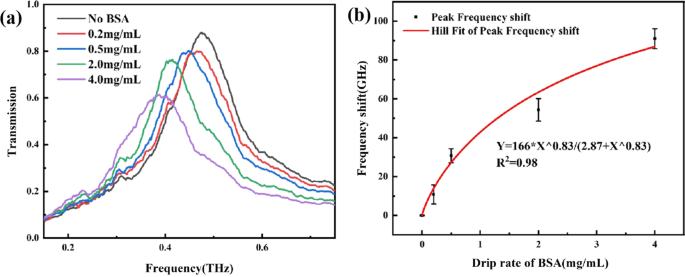
а Измерены спектры с разными концентрациями БСА. б Подгонка по холму эксперимента BSA
Связь между сдвигом частоты и концентрацией растворов БСА не линейна, что является обычным явлением в биологических экспериментах [38, 39]. Модель Хилла может характеризовать связывающую способность между нашим биосенсором из метаматериала и биомолекулами. Поэтому модель Хилла [40] была использована для соответствия экспериментальным данным, как показано на рис. 11b. Уравнение Хилла описывается следующим образом:
$$ \ Delta f =\ Delta f _ {{\ max}} \ cdot \ frac {{[{\ text {BSA}}] ^ {n}}} {{\ left \ {{K _ {{\ text {D) }}} + [{\ text {BSA}}] ^ {n}} \ right \}}} $$ (2)где максимальный сдвиг пиковой частоты Δ f макс - значение насыщения, [BSA] - концентрация раствора BSA, n - коэффициент Хилла, а K D - константа диссоциации.
Используя аппроксимирующую кривую, показанную на рис. 11b, коэффициент Хилла n было рассчитано 0,83, а константа диссоциации K D было рассчитано 2,87 мг / мл. Кроме того, Δ f макс составляла приблизительно 166 ГГц, что указывало на максимальный сдвиг частоты пика при концентрации насыщения. Результаты аппроксимации пика резонансной частоты по Хиллу подтвердили надежность и точность эксперимента.
Чувствительность биосенсора S рассчитывалась следующим образом [41]:
$$ S =\ frac {{\ Delta f _ {{\ max}}}} {{\ delta _ {{\ max}}}} $$ (3)где Δ f макс составляет 166 ГГц и δ макс - поверхностная плотность BSA. δ макс было определено [41]:
$$ \ delta _ {{\ max}} =\ frac {{M _ {{\ text {BSA}}}}}} {{N _ {{\ text {A}}} \ times P _ {{{\ text {BSA}}}} ^ {2}}} $$ (4)где M BSA =66 430 г / моль - расчетная молекулярная масса БСА [42], N A =6,02 × 10 23 моль −1 - число Авогадро, а P BSA =6,96 нм [43] - средняя длина одной молекулы БСА. δ макс было 2,28 нг / мм 2 а чувствительность биосенсора к обнаружению BSA составляла 72,81 ГГц / (нг / мм 2 ).
К D полученные с использованием модели Хилла показали, что константа диссоциации сильно зависит от BSA, а предел обнаружения (LOD) C lim BSA рассчитывали с использованием следующего уравнения [44]:
$$ C _ {{\ lim}} =K _ {{\ text {D}}} \ times \ frac {{S _ {{\ text {f}}}}} {{\ Delta f _ {{\ max}} - S _ {{\ text {f}}}}} $$ (5)где S f - спектральное разрешение 2 ГГц. Уравнение (5) показывает, что меньшая константа диссоциации приводит к более низкому пределу обнаружения. Таким образом, C lim было рассчитано 0,035 мг / мл.
В таблице 2 показаны показатели чувствительности нашего биосенсора к BSA по сравнению с данными опубликованных исследований. В эксперименте самая низкая концентрация раствора BSA составляла 0,2 мг / мл, и было получено изменение частоты 10,8 ГГц. По сравнению с Refs. [45,46,47], относительно более высокая частота изменения была достигнута при той же концентрации BSA. Формула Хилла была применена для анализа данных биосенсора метаматериала. Рассчитанный LOD 0,035 мг / мл был значительно лучше, чем в работе. [45]. Все это предсказывает, что предлагаемый нами цельнометаллический ТГц метаматериальный биосенсор будет иметь отличные характеристики во многих биологических и химических приложениях.
Благодаря превосходным чувствительным характеристикам биосенсора из нержавеющей стали, биосенсор из нержавеющей стали может быть модифицирован специфическими антителами для достижения специфического обнаружения антигена в будущем. А толщина биосенсора из нержавеющей стали составляет всего 50 мкм. С развитием микрофлюидической технологии и терагерцовой спектроскопии есть надежда на применение измерений в реальном времени in vivo в будущем.
Заключение
В заключение, биосенсор терагерцового диапазона на основе цельнометаллического метаматериала был использован для измерения концентрации белка. Биосенсор был изготовлен из нержавеющей стали и изготовлен с помощью технологии лазерного сверления. Максимальная чувствительность RI и FOM, рассчитанные с использованием программного обеспечения электромагнитного моделирования CST, составляют 294,95 ГГц / RIU и 4,03 соответственно. Образец охарактеризовали с помощью непрерывного ТГц спектрометра. Результаты экспериментов показали, что для раствора аналита БСА чувствительность и предел обнаружения составляют 72,81 ГГц / (нг / мм 2 ) и 0,035 мг / мл соответственно. Этот биосенсор обладает такими преимуществами, как малая форма, высокая чувствительность обнаружения, низкие пределы обнаружения, возможность многократного использования, простота изготовления и рентабельность. Эти результаты исследований имеют большое значение для будущих применений в области биомолекулярного обнаружения и диагностики заболеваний.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- THz:
-
Терагерц
- RI:
-
Показатель преломления
- FOM:
-
Достоинства
- BSA:
-
Бычий сывороточный альбумин
- ПЭТ:
-
Полиэтилентерефталат
- DLC:
-
Двойное лазерное управление
- DFB:
-
Распределенная обратная связь
- LOD:
-
Предел обнаружения
Наноматериалы
- Демонстрация гибкого биосенсора на основе графена для чувствительного и быстрого обнаружения клеток рака яи…
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Сверхчувствительный биосенсор для обнаружения ДНК холерного вибриона с помощью композитных наносфер полист…
- Повышенная стабильность магнитных наночастиц золота с помощью сополимера поли (4-стиролсульфоновой кислоты …
- Наночастицы кремнезема для доставки внутриклеточного белка:новый подход к синтезу с использованием зеленог…
- Система обнаружения химических веществ для низких уровней концентрации
- Система обнаружения дефектов на месте в композитах во время отверждения
- Абсорбционная спектроскопия с усилением полости (CEAS) для обнаружения озона
- Биосенсор обеспечивает мониторинг кислорода в реальном времени для органов-на-чипе
- 3 причины для технического обслуживания устройств обнаружения газа



