Сравнительные исследования двумерных (2D) прямоугольных и гексагональных нанолистов из диоксида молибдена различной толщины
Аннотация
Диоксид молибдена (MoO 2 ) своего рода полуметаллический материал демонстрирует множество уникальных свойств, таких как высокая температура плавления, хорошая термическая стабильность, большое отношение площади поверхности к объему, высокая плотность поверхностных ненасыщенных атомов и отличная проводимость. Существует тесная связь между структурным типом и оптоэлектронными свойствами 2D-нанолиста. Здесь прямоугольные и шестиугольные типы тонкого и толстого MoO 2 2D нанолисты были успешно изготовлены из МоО 3 порошка с использованием двухзонного химического осаждения из газовой фазы (CVD) с изменением экспериментальных параметров, и эти изготовленные нанолисты отображали разные цвета под светлопольным микроскопом, обладали полями и гладкой поверхностью. Толщина синего шестиугольника и прямоугольника MoO 2 нанолисты составляют ~ 25 нм и ~ 30 нм, соответственно, в то время как типичная толщина нанолиста оранжевого цвета составляет около ~ 100 нм. Проведены сравнительный анализ и исследования, выявлены смешанные кристаллические фазы в толстом MoO 2 . в качестве основной матрицы посредством рамановской спектроскопии. Впервые полосы излучения, полученные в толстом MoO 2 нанолисты с помощью системы катодолюминесценции (КЛ), демонстрирующие особые свойства полуметаллических и полупроводниковых материалов; однако в случае тонких нанолистов свечение КЛ не обнаружено. Электрические свойства тонкого MoO 2 сравнивались нанолисты с различной морфологией, и оба они демонстрировали различные металлические свойства. Сопротивление тонкого прямоугольного нанолиста составляло ~ 25 Ом при ± 0,05 В, в то время как 64 Ом при ± 0,05 В сообщалось для гексагонального нанолиста, и наблюдалось меньшее сопротивление у прямоугольного нанолиста, чем у гексагонального нанолиста.
Введение
На сегодняшний день синтезированы различные 2D-материалы, такие как графен, дихалькогениды переходных металлов, сурьма, черный фосфор, Mo 2 C и h-BN [1,2,3,4,5,6]; иллюстрируют невероятный потенциал для нового типа оптоэлектронных устройств благодаря их уникальным свойствам и богатой возможности для создания технологий 2D материалов [7]. Конечно, некоторые из конкретных 2D-материалов имеют недостатки, такие как нулевая запрещенная зона, низкая эффективность поглощения и нестабильность в открытой атмосфере, что является проблемами при изготовлении идеальных наноразмерных устройств. Чтобы преодолеть эти проблемы, оксиды переходных металлов (TMO) были признаны эффективными 2D-материалами с точки зрения высокой проводимости, пьезоэлектричества, колоссального магнитосопротивления, лучшей стабильности в открытой среде и сверхпроводимости и т. Д. [8,9,10]. Диоксид молибдена представляет собой типичный материал TMO, имеющий три кристаллические полиморфные формы; гексагональная фаза (P6 3 / ммс ) [11], тетрагональная фаза (P4 2 / мин. ) [12] и моноклинный (P2 1 / c) [13], а также имеет частично рутильную конфигурацию [14], содержащую MoO 6 , октаэдрически связанный Mo через атомы кислорода на краях элементарной ячейки включает четыре MoO 2 единиц напротив двух элементарных ячеек [15, 16]. Хорошо известно, что свойства оксидов молибдена сильно зависят от их кристаллической структуры; в частности, рутиловая структура МоО 2 представляет интерес благодаря превосходной металлической электропроводности [12], низкому электрическому сопротивлению, высокой температуре плавления [17, 18], легкому переносу ионов [19] и превосходной химической стабильности [20]. Это было связано с различными межатомными связями и сравнительно с верхней плотностью состояний на уровне Ферми. Наличие свободных электронов генерирует Mo 4+ в МоО 2 в отличие от поколения Mo 6+ из МоО 3 ; следовательно, все валентные электроны в металлическом молибдене ковалентно связаны с ближайшими атомами кислорода [21, 22]. Небольшое изменение валентности Mo может вызвать значительные колебания физических свойств оксидов молибдена. Например, можно получать соединения других оксидов с различными физическими свойствами [23, 24].
Следовательно, кристалличность, форма и размер продукта могут быть плавно достигнуты путем изменения различных параметров при желаемых методах синтеза; например, Spevack et al. получена моноклинная структура MoO 2 (P2 1 / c) из ɑ-MoO 3 методом термического восстановления [25]. Alves et al. сообщил об электронных и структурных переходах при различных температурах, что привело к увеличению теплового расширения, теплоемкости и электросопротивления монокристалла MoO 2 [26]. Jacob et al. описал деформацию в МоО 2 при высокой температуре и признал фазовый переход, происходящий при определенной температуре с преобразованием искаженной структуры рутила ( P 2 1 / c ) в гексагональную структуру рутила ( P 4 2 / мин. ) [27]. Кроме того, электронная структура и свойства материалов из оксида молибдена меняются в зависимости от толщины [16], и MoO 2 наноструктуры широко используются в электрохимических суперконденсаторах [28], катализе [18], зондировании [29], накоплении энергии [30], электрохромных дисплеях [31] и режимах преобразования энергии [32] из-за их превосходных свойств переноса заряда. [24]. Кроме того, различные методы были использованы для синтеза различных морфологий MoO 2 для достижения исключительных свойств. МоО 2 не имеет кристаллических свойств Ван-дер-Ваальса и, следовательно, не может расслаиваться на слои из объема. В основном, MoO 2 был синтезирован из их предшественников различными методами, такими как гидротермальный и сольвотермический способы [11], термическое разложение молибдатов [33], реакция твердого восстановления [34] и электроспиннинг [35], имеющий различную морфологию, например наночастицы [36], нанопроволоки [31], наностержни [28], нанозвезды [28], нанолисты [37], полые [38] и мезопористые частицы [39]. Однако эти методы оказались неэффективными для контроля морфологии поверхности и размера частиц [22].
Двумерный MoO 2 нанолисты с тонкой и хорошо однородной морфологией поверхности считаются подходящими для обеспечения высокой металлической проводимости, идеальной химической стабильности и позволяют использовать 2D MoO 2 нанолисты как многообещающие для интеграции 2D-материалов в различные электронные структуры и устройства нанометрового масштаба [40]. Здесь мы представили сравнительное исследование и синтез двумерных (2D) прямоугольных и гексагональных нанолистов из оксида молибдена, нанесенных на SiO 2 / Si без обработки после отжига методом CVD:два типа ультратонкого MoO 2 Нанолисты различной толщины были успешно приготовлены и охарактеризованы методами комбинационного рассеяния света, AFM и CL, а также ВАХ. Электрическое поведение оксидов молибдена варьируется от полуметаллического до полупроводникового с широкой запрещенной зоной, поскольку оно зависит от толщины и состояния оксидов. Регулировка времени контролирует осаждение, толщину и определяет субоксидные состояния [41]. Понимание фазовой стабильности оксидов, диапазонов и смесей не только важно для понимания нанолистов оксида молибдена, но также важно для других TMO в оптоэлектронных приложениях [42].
Методы / экспериментальный раздел
Синтез гексагонального МоО 2 Нанолистовые материалы
Синтез гексагональных диоксидов молибдена (MoO 2 ) нанолистов из прекурсора ~ 20 мг MoO 3 порошок (99,95%, Alfa Aesar) помещают на один конец кварцевой трубки в фарфоровую лодочку и нагревают в двухзонной печи в атмосфере азота (N 2 ) атмосферы, как показано на рис. 1а. Родительский SiO 2 Подложки / Si последовательно очищают деионизированной водой, ацетоном, этанолом и изопропанолом с помощью обработки ультразвуком и размещают чистые подложки на расстоянии 3 см от порошков прекурсора. На конце кварцевой трубки помещались два термоблока; перед нагреванием кварцевую трубку продували N 2 (99,999%) при постоянном расходе газа 200 sccm в течение 20 минут для удаления O 2 и других загрязняющих веществ, а затем снизили скорость потока до 20 куб.см в качестве газа-носителя. В левой зоне нагрева была установлена температура 480 ° C со скоростью 10 ° C мин -1 . повышение температуры, в то время как правая зона была настроена на 780 ° C с той же скоростью повышения температуры и выдерживалась в течение 20 минут в присутствии N 2 окружающая обстановка. После завершения реакции печь оставляли для естественного охлаждения до комнатной температуры и, наконец, получали гексагональный МоО 2 нанолисты, нанесенные на SiO 2 / Si подложки.
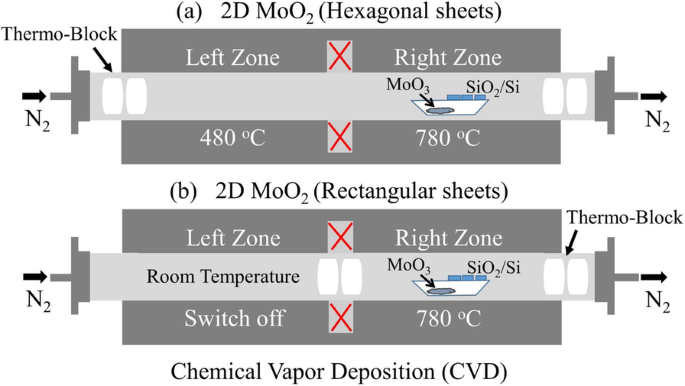
Схематическая конфигурация CVD-системы (красным крестом обозначены изолирующие области). а Гексагональные оксиды молибдена. б Прямоугольные оксиды молибдена
Синтез прямоугольного MoO 2 Нанолистовые материалы
Подобным образом, упомянутым выше, прямоугольный диоксид молибдена (MoO 2 ) нанолисты выращивались в двухзонной трубчатой печи при N 2 атмосферы, как показано на рис. 1b. В этой установке термоблоки были размещены близко к середине трубки:левая зона была установлена на комнатную температуру, а остальные параметры остались такими же, как были установлены для синтеза гексагонального MoO 2. нанолисты для выращивания прямоугольных MoO 2 нанолисты на SiO 2 / Si подложки.
Изготовление устройств
Электронно-лучевая литография использовалась для изготовления электродов с Ti (10 нм) / Au (90 нм) для гексагонального и прямоугольного MoO 2 нанолисты как контактные.
Характеристики
АСМ-изображения получали с использованием атомно-силового микроскопа Dimension Edge PSS (Bruker, Inc., Карлсруэ, Германия) в бесконтактном режиме. СЭМ-изображения были записаны под микроскопом Hitachi S-4800, работающим при 10,0 кВ. Оптические фотографии записывали с помощью оптического микроскопа (Olympus BX51M). Рамановские спектры регистрировались конфокальной рамановской установкой (на основе спектрометра Princeton Acton SP2500). Спектры катодолюминесценции (КЛ) регистрировали с помощью установки для измерения КЛ (Horiba Is-100-em-type2). ВАХ устройств были измерены с помощью системы микрозондовых станций (Keithley 4200-SCS).
Результаты и обсуждения
Для синтеза прямоугольных и гексагональных нанолистов TMO были установлены разные условия, и изменение параметров привело к получению нанолистов разной формы, как показано на рис. 1. В литературе предлагается некоторый возможный механизм реакции для нанолистов, выращенных методом CVD; некоторые молекулы газообразного азота превращаются в молекулы ионизированного азота при определенной температуре под действием теплового излучения в трубчатой печи, и такие молекулы ионизированного азота отмечены символом \ ({\ mathrm {N}} _ 2 ^ {\ ast} \) [43] . При желаемой температуре молекулы MoO 3 сталкиваются с ионизированными молекулами \ ({\ mathrm {N}} _ 2 ^ {\ ast} \), которые производят серию возможных реакций в присутствии инертной газообразной среды азота [44,45,46].
$$ \ mathrm {e} + {\ mathrm {N}} _ 2 \ to {\ mathrm {N}} _ 2 ^ {\ ast} + \ mathrm {e} $$ (1) $$ {\ mathrm {M} } _ {\ mathrm {o}} {\ mathrm {O}} _ 3+ \ left (\ frac {x} {2} \ right) {\ mathrm {N}} _ 2 ^ {\ ast} \ to {\ mathrm { M}} _ {\ mathrm {o}} {\ mathrm {O}} _ {3- \ mathrm {x}} + \ mathrm {xNO} $$ (2) $$ {\ mathrm {M}} _ { \ mathrm {o}} {\ mathrm {O}} _ {3- \ mathrm {x}} + \ left (\ frac {1-x} {2} \ right) {\ mathrm {N}} _ 2 ^ { \ ast} \ to {\ mathrm {M}} _ {\ mathrm {o}} {\ mathrm {O}} _ 2+ \ left (1- \ mathrm {x} \ right) \ \ mathrm {NO} $$ ( 3) $$ {\ mathrm {M}} _ {\ mathrm {o}} {\ mathrm {O}} _ 2 + 3 {\ mathrm {M}} _ {\ mathrm {o}} {\ mathrm {O} } _3 \ kern0.5em \ to {\ mathrm {M}} _ {\ mathrm {o} 4} {\ mathrm {O}} _ {11} $$ (4)Структура испаренного MoO 3 молекулы могут изменяться на нанолисты различной морфологии, увеличивая или уменьшая N 2 расход газа и время выдержки при заданных температурах [45]. Во время диффузии молекул к субстратам они начинают агрегацию с образованием различных видов правильных прямоугольных и гексагональных MoO 2 листов.
На рис. 2а показан гексагональный МоО 2 , изготовленный методом химического осаждения из паровой фазы. нанолисты намного лучше, чем синтез гексагонального MoO 2 на основе раствора нанолисты [47, 48]. Кроме того, различные фазовые структуры прямоугольного MoO 2 может быть получен методом CVD с определенными параметрами контроля; температура зон нагрева, расположение термоблоков и положение подложек, как показано на рис. 2d. Установка температуры левой зоны нагрева на 480 ° C был чрезвычайно важен для синтеза гексагонального MoO 2 нанолисты. Основной механизм гексагонального MoO 2 нанолисты - это температурный градиент. Xu, X., et al. сообщают о высокой зависимости морфологических изменений от термодинамики и влияния кинетики на процесс роста кристаллов, которые основаны на различии в термодинамической стабильности и деформации решетки между фазами [49]. И низкотемпературные, и высокотемпературные зоны играют решающую роль в создании гексагональных нанолистов; однако изменение температуры высокотемпературной зоны очень эффективно для роста прямоугольного MoO 2 нанолист. Кроме того, Wang, S., et al. сообщили об эволюции двумерных нанолистов, которые сильно зависят от пространственного расположения подложек [50]. Янг, X., et al. также сообщил о зависящем от температуры росте регулярной морфологии нанолистов и дополнительно объяснил механизм химического пара с помощью первопринципного метода KMC [51]. Есть несколько гексагональных и прямоугольных нанолистов синего и оранжевого цвета разной толщины; Нанолисты синего цвета тоньше нанолистов оранжевого цвета и хорошо согласуются с характеристиками других 2D-материалов [52]. Смешанные цвета означают, что многослойный нанолист сформирован различной толщины, как показано на рис. S1 и рис. S2 в дополнительной информации. Толщина нанолистов монотонно уменьшалась последовательно:оранжевый цвет, желтый цвет и синий цвет, что зависит от вариации синтетических параметров. На рис. 2b, e показано усиленное SEM-изображение типичного гексагонального и прямоугольного нанолиста, демонстрирующее гладкую поверхность, четкие поля, правильную форму высокого качества и длину 10 мкм. С помощью АСМ были измерены синие гексагональные и прямоугольные нанолисты толщиной ~ 25 нм и ~ 30 нм соответственно, как показано на рис. 2c, f.

а Фотография нанолистов гексагонального оксида молибдена под микроскопом. б СЭМ-изображение нанолиста гексагонального оксида молибдена, масштаб 2 мкм. c Результат АСМ гексагонального нанолиста оксида молибдена синего цвета. г Фотография прямоугольных нанолистов оксида молибдена под микроскопом. е СЭМ-изображение прямоугольного нанолиста оксида молибдена на шкале 2 мкм. е Результат АСМ прямоугольного нанолиста оксида молибдена синего цвета
Рамановские спектры были получены для исследования качества и однородности выращенного MoO 2 нанолисты. Здесь мы представляем спектры комбинационного рассеяния прямоугольного и гексагонального MoO 2 нанолисты разного цвета при облучении лазером с длиной волны 532 нм. На рис. 3а пики комбинационного рассеяния, полученные из тонкого гексагонального нанолиста (синий цвет), расположены на 143,1, 184,6, 204,6, 229,6, 292,0, 311,0, 364,3, 383,3, 495,7, 570,5 и 737,6 см -1 , соответственно. По сравнению с тонким прямоугольным нанолистом пики синего цвета соответствуют небольшому сдвигу пиков при 143,1, 185,1, 204,6, 229,2, 292,7, 311,1, 361,7, 380,2, 495,9, 569,8 и 735,1 см -1 , соответственно. Оба типа тонких нанолистов синего цвета имеют одинаковое количество пиков комбинационного рассеяния; однако дополнительный сильный пик кремния был получен при 526 см −1 в гексагональном нанолисте синего цвета. Фактически, смещение пика происходит из-за разницы в толщине нанолистов; гексагональные нанолисты тоньше прямоугольных, как показано на рис. 2c, f. Дополнительное расположение пика для кремния произошло из-за проникновения лазера, попадания на поверхность кремния, служившего подложкой, и связано с толщиной гексагональных и прямоугольных нанолистов синего цвета по сравнению с гексагональными и прямоугольными нанолистами оранжевого цвета, как показано на рис. 3a. Для толстых гексагональных нанолистов было получено 13 пиков с положением пика при 142,3, 183,5, 204,6, 229,2, 292,3, 311,0, 347,7, 361,6, 380,2, 457,8, 495,1, 570,2 и 739,7 см −1 , соответственно. 13 пиков, отмеченных для толстого прямоугольного нанолиста в положениях 143,3, 183,9, 204,6, 229,2, 292,2, 311,0, 346,1, 359,3, 380,2, 455,5, 495,1, 568,3 и 736,8 см −1 имеют небольшое изменение положения по сравнению с гексагональными нанолистами. Толщина вызывала несколько дополнительных пиков с разными волновыми числами по сравнению с более тонкими нанолистами синего цвета [53]. Детали идентификации пиков комбинационного рассеяния для тонких / толстых гексагональных и прямоугольных нанолистов приведены на рис. S3 в дополнительном файле; результаты хорошо согласуются с опубликованными результатами моноклинного МоО 2 тонкая пленка, полученная различными способами синтеза CVD [54, 55]:толщина и смещение пиков зависят от условий выращивания [56, 57]. В данной работе мы впервые сообщаем о 13 вибрационных пиках для оранжевого цвета, а 11 пиков для синего цвета правильного шестиугольного и прямоугольного MoO 2 нанолисты, подтверждающие наличие смешанных структур в MoO 2 нанолисты. Острые и сильные пики подтвердили лучшую кристалличность по сравнению с другими опубликованными результатами [15, 54, 55].
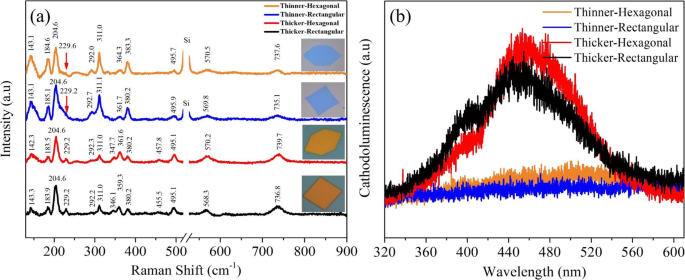
а Рамановские спектры тонких гексагональных и прямоугольных нанолистов оксида молибдена синего цвета и толстых гексагональных и прямоугольных нанолистов оксида молибдена оранжевого цвета. б Спектры катодолюминесценции (КЛ) (оранжевые спектры для тонкого гексагонального нанолиста, синие спектры представляют собой тонкий прямоугольный нанолист, красные спектры представляют собой толстый гексагональный нанолист, а черные спектры представляют собой толстый прямоугольный нанолист)
Из этих четырех типичных нанолистов можно сделать вывод, что все они содержат сложные и смешанные структуры, такие как чистый MoO 3 , МоО 3 − x , моноклинный МоО 2 , ромбический МоО 3 (α-МоО 3 ) и ромбический Mo 4 О 11 . Рамановский пик при 289 см −1 назначен чистому МоО 3 , 142 см −1 в MoO 3 − x [58] и пик на 287 см −1 связан с ромбическим α-MoO 3 [59]. Дитерле М. сообщил о пиках комбинационного рассеяния для различных оксидов молибдена; орторомбический МоО 3 , моноклинный МоО 2 , и ромбический Mo 4 О 11 ; полосы 290–292 см −1 считаются произведенными из орторомбического МоО 3 (α-МоО 3 ), а пик комбинационного рассеяния составляет 183, 306 см −1 вырос из орторомбического Mo 4 О 11 [60]. Пики на 380 см −1 были назначены в МП 2 [61] и 460 см −1 в α-MoO 3 [62]. Результаты спектров комбинационного рассеяния света синтезированных нами нанолистов представлены на рис. 3а. Результаты спектров комбинационного рассеяния отдельных нанолистов доступны на дополнительном рисунке S3. Следовательно, пики комбинационного рассеяния в наших результатах связаны с различными структурными фазами различных оксидов молибдена:142,3 ~ 143,3 см −1 (МоО 3 − x ), 183,5 ~ 185,1 см −1 (Мо 4 О 11 ) и 204,6 см −1 (МоВ 2 ). Более того, пики составляют 229,2 ~ 229,6 см −1 (МоВ 2 ), присутствующие в нанолистах оранжевого цвета, резче и шире по сравнению с нанолистами синего цвета, что подтверждает наличие множественных деформаций в толстых нанолистах. Пики при 292,0 ~ 292,7 см -1 (α-МоО 3 ) в нанолистах синего цвета резче и шире, чем нанолисты оранжевого цвета. Пики при 311,0 ~ 311,1 см −1 (Мо 4 О 11 ) существуют во всех четырех типах нанолистов; более интенсивный пик наблюдается в тонких нанолистах синего цвета по сравнению с нанолистами оранжевого цвета. Однако пики на 346,1 ~ 347,7 см −1 (МоВ 2 ) существуют только в нанолистах оранжевого цвета. В основном все эти пики присутствуют во всех типах нанолистов с небольшими вариациями; пики при 359,3 ~ 364,3 см −1 для (MoO 2 ) и достигает пиков при 380,2 ~ 383,3 см −1 (МоВ 2 ) присутствовали во всех нанолистах; однако пики на 455,5 ~ 457,8 см -1 (α-МоО 3 ) присутствуют только в нанолистах оранжевого цвета. Основные пики хорошо совпадают с диоксидами молибдена и повышены во всех нанолистах, например, пики при 495,1 ~ 495,9 см -1 (МоВ 2 ), 568,3 ~ 570,5 см −1 (МоВ 2 ) и 735,1 ~ 739,7 см −1 (МоВ 2 ). Субоксиды образовались из-за межвалентных переходов; в субоксидах расстояние между атомами Мо связано с атомами кислорода, в которых латерально тетраэдрический c ось увеличивалась с увеличением деформации связи от ненарушенного участка к плоскости сдвига. Это влияет на полностью поляризованные моды параллельно c ось:поляризованные моды перпендикулярны c оси зависят от расстояний связи M =O. Уход атомов кислорода из чистого MoO 3 после обработки при высокой температуре подтверждены кристаллографические структуры сдвига через длительные сдвиговые дефекты, завершающие трансляционную симметрию [58]. Для гексагональных и прямоугольных нанолистов оранжевого цвета, отличных от обычных пиков диоксидов молибдена, отмечается большее количество дополнительных пиков; пики при 142,3 ~ 143,3 см -1 для МоО 3 − x пики при 292,2 ~ 292,3 и 455,5 ~ 457,8 см −1 для α-MoO 3 и достигает пиков при 183,5 ~ 183,9 и ~ 311,0 см −1 для Mo 4 О 11 .
Для дальнейшей проверки проводят катодолюминесценцию (КЛ), чтобы проверить влияние структурной фазы сложных структурных фаз оксида молибдена на металлические свойства как толстых гексагональных, так и прямоугольных нанолистов. Теоретически полуметаллический MoO 2 частично превратится в полупроводник за счет участия МоО 3 . Однако измерить спектр ФЛ чистого MoO 2 очень сложно. наноструктуры из-за металлических характеристик:MoO 3 представляет собой широкозонный полупроводник со слабой интенсивностью люминесценции до превращения и исчезновения MoO 3 в MoO 3 − x , и дальнейшее преобразование в MoO 2 нанолисты [63]. Следовательно, для гексагональных и прямоугольных нанолистов из оксида молибдена не сообщается о спектре люминесценции.
Свойства катодолюминесценции (КЛ) толстых нанолистов молибдена выявили электронный переход между зоной проводимости и валентной зоной из-за присутствия субоксидов. Как показано на рис. 3b, спектры ХЛ, полученные для толстых гексагональных и прямоугольных нанолистов оксида молибдена, показывают небольшие пики ХЛ при 410 нм (3,02 эВ), в то время как более сильные и широкие пики при 454 нм (2,73 эВ) генерируются нанолистами. Более слабые пики при 410 нм в обоих спектрах ХЛ аналогичны МоО 3 спектры, а слабое излучение может быть связано с рекомбинацией состояния ловушки:полоса 454 нм, относящаяся к связанным с дефектами состояниям ловушки, происходящим из кислородных вакансий [64]. Энергия испускаемых фотонов для чистого MoO 3 расположенное при 3,02 эВ вместо 3,2 эВ для запрещенной зоны указывает на преобразование MoO 3 порошок в МоО 3 − x и был проверен по результатам спектров комбинационного рассеяния света. Широкополосные спектры КЛ, которые варьируются от 3,02 до 2,73 эВ, подтвердили смешанные наноструктуры в толстых нанолистах, обладающих градиентным поведением металл-полупроводник. Эти оксиды молибдена связаны с развитием концентраций носителей, концентраций кислородных вакансий в восстановленном MoO 3 , и концентрация свободных электронов в MoO 2 . Эти исследования расширили знания о структурных и оптических свойствах нанолистов субстехиометрического оксида молибдена, что способствовало разработке передовых оптических устройств. Аналогичные спектры ХЛ представлены для оксидов других переходных металлов, таких как WO 3 и α-Fe 2 О 3 [65]. Проблема обнаружения спектров КЛ в тонких нанолистах описана и опубликована в литературе. Интенсивность ХЛ чешуек уменьшалась с уменьшением толщины слоя; тонкослойные чешуйки прозрачны для электронного луча; созданные электронные дырки прямо пропорциональны их толщине [66]. Bourrellier, R., et al. подтвержденное обнаружение широкополосной люминесценции в кристаллах низкого качества, которая связана не с внешними дефектами, а, очевидно, с собственными дефектами, которые могут возникнуть при электронном облучении [67]. Недавно Zhou, N., et al. сообщили о сильной ориентации интенсивности ХЛ из-за увеличения концентрации дефектов и увеличения толщины чешуек, но интенсивность излучения ХЛ снижалась с уменьшением толщины чешуек [68]. Несмотря на этот эффект, толстые чешуйки демонстрируют значительную люминесценцию по сравнению с тонкими чешуйками. По этой причине спектры КЛ чистого тонкого MoO 2 невозможно обнаружить в тонких нанолистах; Спектры КЛ как тонкого гексагонального (спектры оранжевого цвета), так и прямоугольного нанолиста (спектры синего цвета) представлены на рис. 3b.
Тонкие гексагональные и прямоугольные нанолисты обладают металлическими характеристиками, подтвержденными измерениями ВАХ, как показано на рис. 4 и вспомогательной информацией (SI) на рис. S4. Мы изготовили два терминала, содержащие шесть устройств, на тонких нанолистах синего цвета и измерили ВАХ с такими же параметрами; три из них были прямоугольными нанолистами, а остальные три были гексагональными нанолистами, как показано на вставке к рис. 4a, b, соответственно. Контакты были изготовлены с использованием Ti / Au в качестве электродов. Принципиальная схема одиночных прямоугольных и гексагональных нанолистов из оксида молибдена представлена на рис. 4а, б. На рис. 4c, d ВАХ обоих типов нанолистов измерены путем изменения напряжения смещения от отрицательного (-0,05 В) до положительного (+ 0,05 В) несколько раз без каких-либо изменений в устройствах и отображаются линейно. поведение при омическом контакте между нанолистами и электродами устройств. Для измерения сопротивления использовалось омическое уравнение R = V / Я , где R представляет сопротивление, V напряжение и I Текущий; Сопротивление прямоугольных и гексагональных нанолистов было измерено на ~ 25 Ом при ± 0,05 В и 64 Ом при ± 0,05 В, соответственно, что дополнительно подтвердило, что прямоугольный нанолист имеет меньшее сопротивление, чем гексагональный нанолист.
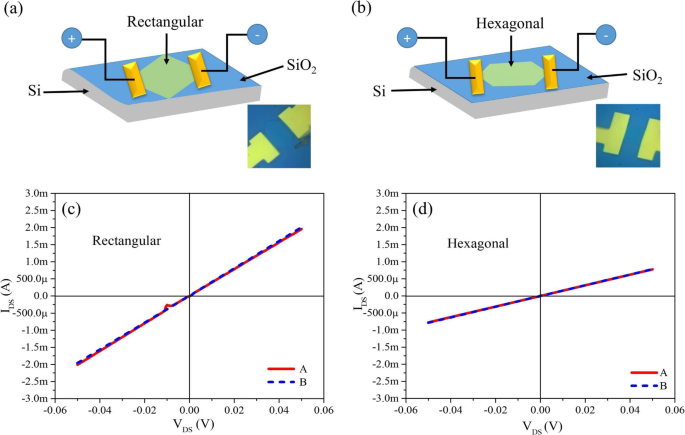
а Принципиальная схема устройства одиночного прямоугольного нанолиста оксида молибдена. Врезка:реальное изображение устройства. б Принципиальная схема устройства одинарного гексагонального нанолиста оксида молибдена. Врезка:реальное изображение устройства. c ВАХ индивидуального одиночного прямоугольного нанолиста оксида молибдена. г ВАХ индивидуального устройства одиночного гексагонального нанолиста оксида молибдена
Кроме того, сопротивление ( R ) тонких прямоугольных нанолистов синего цвета составляют ~ 30 Ом при ± 0,05 В и ~ 43 Ом при ± 0,05 В, как показано на рис. S4a, b в вспомогательной информации (SI); однако сопротивление ( R ) тонких гексагональных нанолистов синего цвета составляют ~ 61 Ом при ± 0,05 В и ~ 61 Ом при ± 0,05 В, как показано на рис. S4c, d. Это подтверждает, что тонкие прямоугольные нанолисты синего цвета имеют меньшее сопротивление при тех же параметрах, чем тонкие шестиугольные нанолисты синего цвета.
Выводы
В этой работе мы сообщаем о контрольном синтезе прямоугольных и гексагональных нанолистов оксида молибдена из порошка одного прекурсора MoO 3 без постотжиговой обработки методами ССЗ. Сравнительный анализ и исследования проводились с использованием различных спектроскопических методов:спектров комбинационного рассеяния света, оптической фотографии, сканирующей электронной микроскопии, атомно-силовой микроскопии и катодолюминесценции (КЛ). Оптический контраст зависит от толщины нанолистов. Результаты СЭМ подтвердили хорошую симметрию и гладкую морфологию контролируемых нанолистов. АСМ-анализ измерял толщину тонких прямоугольных нанолистов ~ 30 нм и гексагональные нанолисты ~ 25 нм. Результаты спектров комбинационного рассеяния света показывают наличие смешанных структур в MoO 2 нанолисты из-за сложной кристаллической структуры. Сильный спектральный отклик и смещение пиков зависит от толщины нанолистов. Сравнительно меньше пиков комбинационного рассеяния наблюдалось для тонких, чем более толстых нанолистов, и они хорошо согласовывались с колебаниями кристалла MoO 2 и другие смешанные кристаллы; однако некоторые пики исчезли в тонких 2D-нанолистах. Толстые нанолисты оранжевого цвета содержат больше пиков из-за сложных структурных фаз оксида молибдена; особенно, дополнительный МоО 3 и МоО 3 − x встречается в полуметаллическом MoO 2 , и, таким образом, толстые нанолисты демонстрируют поведение полупроводников с широкой запрещенной зоной и были дополнительно подтверждены спектрами катодолюминесценции (КЛ). Впервые комбинированные свойства металлических и широкозонных полупроводников наблюдались в смешанном оксиде молибдена, толстых гексагональных и прямоугольных нанолистах. Эти пики в нанолистах оранжевого цвета могут быть полезными фотонными материалами для практических применений в наноразмерных устройствах; однако для тонких нанолистов свечение ХЛ не обнаружено. ВАХ всех устройств, изготовленных из тонких прямоугольных или гексагональных нанолистов, демонстрирует линейное металлическое поведение из-за хорошо установленного омического контакта между нанолистами и электродами. Тонкий гексагональный нанолист показал более высокое сопротивление, чем прямоугольный нанолист. Это исследование обеспечивает глубокое понимание специальных двумерных нанолистов из оксида молибдена, обеспечивая способ модуляции свойств различных типов нанолистов.
Доступность данных и материалов
Все данные полностью доступны без ограничений.
Сокращения
- 2D:
-
Двумерный
- MoO 2 :
-
Диоксид молибдена
- MoO 3 :
-
Триоксид молибдена
- CL:
-
Катодолюминесценция
- R:
-
Resistance
- Ω:
-
Ohm
- V:
-
Voltage
- I – V:
-
Current–Voltage
- CVD:
-
Химическое осаждение из паровой фазы
- Mo2 C:
-
Molybdenum carbide
- h-BN:
-
hexagonal-Boron nitride
- TMOs:
-
Оксиды переходных металлов
- P:
-
Space group
- N 2 :
-
Азот
- \( {\mathrm{N}}_2^{\ast } \) :
-
Ionized nitrogen
- sccm:
-
Standard cubic centimeters per minute
- SiO 2 /Si:
-
Silicon dioxide/silicon
- Ti:
-
Титан
- Au:
-
Золото
- AFM:
-
Атомно-силовой микроскоп
- SEM:
-
Сканирующий электронный микроскоп
Наноматериалы
- Экспериментальные исследования стабильности и естественной конвекции наножидкости TiO2-вода в корпусах с раз…
- Широкополосный идеальный абсорбер с однослойным MoS2 и массивом нанодисков из гексагонального нитрида титана
- Простой синтез серебряных нанопроволок с разным соотношением сторон и используемых в качестве высокоэффект…
- Влияние толщины бислоя на морфологические, оптические и электрические свойства наноламинатов Al2O3 / ZnO
- Изготовление, характеристика и биологическая активность систем нано-доставки авермектина с различными разм…
- Морфология, структура и оптические свойства полупроводниковых пленок с наноостровками GeSiSn и напряженными сл…
- Сравнительное исследование электрохимических, биомедицинских и тепловых свойств природных и синтетических…
- Свойства контролируемого синтеза и селективной адсорбции нанолистов Pr2CuO4:обсуждение механизма
- 20 различных типов металлов и их свойства
- Различные свойства и марки инструментальной стали



