Гетероструктура ядро-оболочка CNT @ Li2FeSiO4 @ C как высокостабильный катодный материал для литий-ионных батарей
Аннотация
Разумный дизайн наноструктуры является ключом к устранению внутренних дефектов и достижению высоких характеристик Li 2 FeSiO 4 катодные материалы. В данной работе представлена новая гетероструктура CNT @ Li 2 FeSiO 4 @C был разработан, синтезирован и использован в качестве катодного материала для литий-ионных аккумуляторов. Выявлено, что продукт имеет однородную структуру ядро-оболочка, а толщина Li 2 FeSiO 4 слой и внешний углеродный слой составляет около 19 нм и 2 нм соответственно. Рациональная конструкция эффективно ускоряет диффузию ионов лития, улучшает электропроводность и уменьшает изменение объема во время процесса зарядки / разрядки. Обладая преимуществами своей специфической структуры, CNT @ Li 2 FeSiO 4 @C успешно преодолел недостатки, присущие Li 2 FeSiO 4 и показал хорошую обратимую емкость и циклические свойства.
Введение
Литий-ионные батареи (LIB) широко используются в портативных электронных устройствах и электромобилях из-за преимуществ высокоэффективного преобразования энергии, длительного срока службы, высокой плотности энергии и низкого саморазряда [1,2,3]. Тем не менее, LIB нового поколения с более высокой плотностью энергии, более высокими скоростными характеристиками и более высокими характеристиками езды на велосипеде срочно необходимы для удовлетворения развития электромобилей [4,5,6]. Было признано, что использование новых катодных материалов имеет большое значение для разработки LIB нового поколения, поскольку характеристики LIB тесно связаны со свойствами катодных материалов. В последние несколько лет Ли 2 FeSiO 4 Катодный материал привлек большое внимание из-за его недорогой, хорошей химической стабильности и безвредности для окружающей среды. В частности, есть возможность вставить / извлечь два иона лития для каждой молекулярной единицы, имеющей емкость 332 мАч г -1 . теоретически [7, 8]. Однако реализовать два накопителя Li на практике сложно из-за низкой проводимости (~ 6 × 10 - 14 См см −1 ) и коэффициент диффузии ионов лития (~ 10 - 14 см 2 s −1 ) Ли 2 FeSiO 4 [9,10,11,12]. Следовательно, очень важно улучшить электронную проводимость и литий-ионную транспортную способность Li 2 FeSiO 4 катод для оптимизации работы LIB. Было приложено много усилий для решения этих проблем, таких как синтез Li 2 в нанометровом масштабе. FeSiO 4 [13,14,15] и покрытие поверхности углеродным материалом [16,17,18]. Однако в процессе синтеза часто возникают две проблемы. Одна из проблем заключается в том, что трудно синтезировать чистую фазу Li 2 FeSiO 4 продукт и некоторые сопутствующие примеси, такие как Fe 3 О 4 или Ли 2 SiO 3 часто неизбежны, что отрицательно сказывается на возможностях практики [19, 20]. Другая проблема заключается в том, что наноструктура Li 2 FeSiO 4 часто повреждаются во время отжига.
В данном исследовании гетероструктура ядро-оболочка CNT @ Li 2 FeSiO 4 Синтезирован катодный материал @C. По сравнению с опубликованной работой о Ли 2 FeSiO 4 катодный материал, УНТ @ Li 2 FeSiO 4 Материал @C демонстрирует преимущество отсутствия примесной фазы и структурной целостности за счет регулирования дозировки химического реагента и условий реакции. Кроме того, внутренний слой УНТ может увеличивать проводимость. Толщина Li 2 FeSiO 4 в среднем слое составляет всего 20–25 нм, что дает преимущество Li + диффузия. А внешний аморфный углеродный слой может улучшить проводимость и защитить внутреннюю структуру каркаса. Следовательно, гетероструктура ядро-оболочка CNT @ Li 2 FeSiO 4 @C демонстрирует значительное улучшение удельной емкости, стабильности цикла и производительности.
Методы
Материалы и синтез
CNT @ Li 2 FeSiO 4 @C был изготовлен путем пошаговой подготовки. Во-первых, CNT @ SiO 2 Коаксиальная структура была получена методом золь-гель покрытия [21, 22]. Обычно 8 мг УНТ диспергировали в смеси 80 мл этанола и 30 мл деионизированной воды, а затем смесь обрабатывали ультразвуком в течение 30 минут для образования гомогенного раствора. Затем 2 мл NH 3 · H 2 О (25–28 мас.%) И 0,16 г бромида цетилтриметиламмония (ЦТАБ) добавляли в указанный выше раствор при обработке ультразвуком и выдерживали в течение 20 мин. Смешанный раствор, содержащий 0,45 мл тетраэтоксисилана (TEOS) и 40 мл этанола, по каплям добавляли в указанный выше раствор при перемешивании магнитной мешалкой в течение более 40 минут, после чего следовало перемешивание в течение 10 часов. УНТ @ SiO 2 продукт был получен центрифугированием и очисткой деионизированной водой и этанолом. Затем CNT @ Li 2 FeSiO 4 получается твердофазным спеканием. Водный раствор 0,334 г LiAc · 2H 2 O и 0,734 г Fe (NO 3 ) 3 · 9H 2 О последовательно растворяли в 30 мл этанола при перемешивании в течение 20 мин. Полученные УНТ @ SiO 2 добавляли к раствору и обрабатывали ультразвуком в течение 40 минут и перемешивали магнитной мешалкой в течение 20 минут. Затем его перенесли в вакуумную сушилку при 80 ° C на 12 часов. Полученный сухой порошок сначала прокаливали при 400 ° C в течение 2 часов, а затем нагревали при 650 ° C в течение 10 часов в атмосфере аргона; в результате CNT @ Li 2 FeSiO 4 был подготовлен. CNT @ Li 2 FeSiO 4 @C был получен с использованием глюкозы в качестве источника углерода. 0,2 г CNT @ Li 2 FeSiO 4 диспергировали ультразвуком в течение 40 мин в 40 мл этанола. Затем к раствору добавляли раствор, содержащий 0,1 г глюкозы. Полученный раствор помещали в вакуумную сушилку при 80 ° C на 6 часов. Затем продукт прокаливали при 400 ° C в течение 4 часов в атмосфере аргона, чтобы получить CNT @ Li 2 FeSiO 4 @C катодный материал.
Характеристики материалов
Кристаллическая структура УНТ @ Li 2 FeSiO 4 @C и CNT @ Li 2 FeSiO 4 был охарактеризован дифракцией рентгеновских лучей (XRD, D2 PHASER Bruker) в диапазоне 2θ от 10 ° до 80 ° с использованием излучения Cu-Kα ( λ =1,5418 Å) излучения при 30 кВ и 10 мА. Химические элементы материалов подтверждены системой рентгеновской фотоэлектронной спектроскопии (XPS, K-ALPHA 0.5EV). Сканирующая электронная микроскопия (FESEM, S-4800) и просвечивающая электронная микроскопия (ТЕМ, Tecnai G2 F 20) использовались для наблюдения за структурой и морфологией материалов. Распределение элементов в композите выявлено методом энергодисперсионной рентгеновской спектроскопии (EDX). Содержание углерода в композите исследовали с помощью кривой термогравиметрического анализатора (TGA) (STD Q600 TA) при скорости 10 ° C мин -1 от КТ до 800 ° С.
Электрохимические измерения
Катод был сделан из 10 мас.% Поливинилиденфторида (ПВДФ), 20 мас.% Ацетиленовой сажи и 70 мас.% Активного материала, диспергированного в N -метил-2-пирролидон (NMP) с образованием однородной суспензии. Затем суспензию наносили на алюминиевую фольгу и сушили в вакууме при 80 ° C в течение более 12 часов. Массовая загрузка активного материала для CNT @ Li 2 FeSiO 4 @C и CNT @ Li 2 FeSiO 4 электрод составлял около 1,5 мг / см 2 . Наконец, полуэлементы были собраны в перчаточном ящике, заполненном аргоном. Батарею тестировали на заряд и разрядку с использованием аккумуляторной системы Neware в диапазоне напряжений 1,5 ~ 4,8 В. Циклические вольтамперометрические (CV) измерения выполняли на многоканальной электрохимической рабочей станции VMP3 (Франция, Bio-logic) при различных скоростях сканирования.
Результаты и обсуждение
Принципиальная схема процесса приготовления CNT @ Li 2 FeSiO 4 Материал @C показан на рис. 1. Во-первых, CNT @ SiO 2 был приготовлен простым золь-гель методом. Контролируя дозировку УНТ и ТЭОС, цель точного контроля толщины Li 2 FeSiO 4 слой был достигнут. Во-вторых, CNT @ Li 2 FeSiO 4 с хорошей кристалличностью был получен отжигом при 650 ° C в течение 10 ч в атмосфере аргона. Наконец, CNT @ Li 2 FeSiO 4 был покрыт аморфным углеродом только при 400 ° C для получения гетероструктуры ядро-оболочка CNT @ Li 2 FeSiO 4 @C.
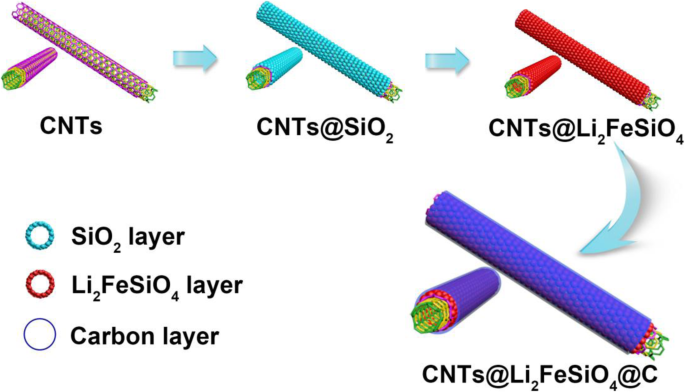
Принципиальная схема синтеза гетероструктуры ядро-оболочка CNT @ Li 2 FeSiO 4 @C
На рисунке 2а показаны дифрактограммы CNT @ Li 2 . FeSiO 4 и CNT @ Li 2 FeSiO 4 @C . Дифракционные пики Li 2 FeSiO 4 согласуются с моноклинной структурой с p2 1 / n космическая группа. Кроме того, нет пика дифракции XRD примесей (таких как Fe 3 О 4 и Ли 2 SiO 3 ), что подтверждает чистоту полученного продукта. Основной элемент и состояние поверхностной валентности CNT @ Li 2 FeSiO 4 @C изучаются методом РФЭС (рис. 2б – г). На рис. 2б показан полный спектр Li 2 . FeSiO 4 , включая Li 1s, Si 2p, Si 2s, C 1s, O 1s и Fe 2p. На рисунке 2c показан спектр Fe2p, а два пика при 710,3 эВ и 723,8 эВ относятся к Fe 2p 3/2 . и Fe 2p 1/2 Fe 2+ , соответственно. Пик сателлитной энергии связи при 710,4 эВ на 4,6 эВ ниже, чем сателлитный пик энергии связи при 715,0 эВ, что дополнительно указывает на то, что только Fe 2+ существует в Ли 2 FeSiO 4 нанокристаллы [23]. На рисунке 2d показано, что пик на Si 2p при 101,8 эВ в основном согласуется с пиком на Si 4+ . в полисилоксане, что свидетельствует об образовании ортогональной силикатной структуры [SiO 4 ] [24, 25].
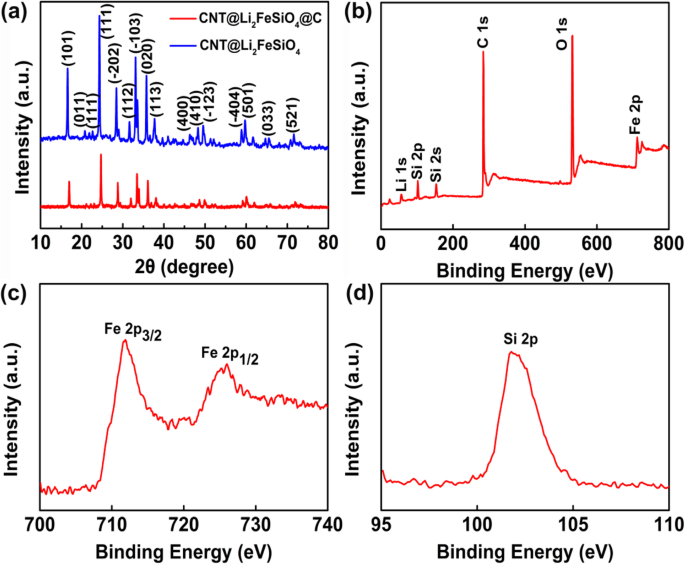
а XRD CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 , b Полные XPS-спектры CNT @ Li 2 FeSiO 4 @C, и спектры высокого разрешения c Fe 2p и d Si 2p
Сканирующая электронная микроскопия (SEM) выявляет морфологию и структуру CNT (дополнительный файл 1:Рисунок S1A), CNT @ SiO 2 (Дополнительный файл 1:Рисунок S1B), CNT @ Li 2 FeSiO 4 (Рис. 3а, б), а CNT @ Li 2 FeSiO 4 @C (рис. 3в, г). Стоит отметить, что одномерная наноструктура как CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 @C сохраняется и нет бесплатного Li 2 FeSiO 4 наблюдаются частицы. Результат ТГ подтверждает, что содержание углерода в CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 @C составлял 16,93% и 22,69% соответственно (дополнительный файл 1:рисунок S2).

а , b СЭМ изображения CNT @ Li 2 FeSiO 4 , c и d СЭМ изображения CNT @ Li 2 FeSiO 4 @C. е и е ПЭМ изображения CNT @ Li 2 FeSiO 4 , ч и я ПЭМ изображения CNT @ Li 2 FeSiO 4 @C; j и k HRTEM CNT @ Li 2 FeSiO 4 @C и CNT @ Li 2 FeSiO 4 @C соответственно; l - o Отображение элементарных элементов EDX для Fe, Si и O
Структура CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 @C дополнительно подтверждается просвечивающей электронной микроскопией (ПЭМ). Структура ядро-оболочка CNT @ Li 2 FeSiO 4 можно визуально различить из рис. 3e и f. Полный диаметр CNT @ Li 2 FeSiO 4 составляет около 70 нм, а толщина внешнего слоя Li 2 FeSiO 4 составляет 20 нм. Гетероструктура ядро-оболочка УНТ @ Li 2 FeSiO 4 @C можно ясно подтвердить на рис. 3h и i. Кроме того, на рис. 3i показана одномерная наноструктура УНТ @ Li 2 . FeSiO 4 @C диаметром около 85 нм. Внутренний слой УНТ имеет диаметр около 40 нм, а средний слой Li 2 FeSiO 4 имеет толщину около 16–22 нм. А толщина внешнего углеродного слоя составляет около 2 нм. На рис. 3j и k показана ВР-ПЭМ CNT @ Li 2 . FeSiO 4 и CNT @ Li2FeSiO4 @ C соответственно. Полоса решетки на расстоянии 0,27 нм совпадает с шагом решетки (- 103) ромбического Li 2 FeSiO 4 . Рисунок 3k также показывает, что толщина внешнего аморфного углерода составляет около 1,5 нм. На рис. 3l – o представлен анализ элементарного отображения CNT @ Li 2 . FeSiO 4 , который демонстрирует сосуществование и равномерное распределение элементов Fe, Si и O.
Производительность CNT @ Li 2 при езде на велосипеде FeSiO 4 и CNT @ Li 2 FeSiO 4 @C был протестирован на системе тестирования батарей Neware с диапазоном напряжения 1,5–4,8 В при плотности тока 0,2 C. Как показано на рис. 4a, удельная емкость CNT @ Li 2 FeSiO 4 составляет 100,8 мАч г −1 и сохранение емкости после 2, 10, 50 и 150 циклов составило 95,2%, 92,8%, 91% и 78,2% соответственно. Напротив, CNT @ Li 2 FeSiO 4 @C имеет зарядную емкость 207 мАч g −1 и разрядная емкость 178 мАч g −1 в начальном цикле (рис. 4б). После 2, 10, 50 и 150 циклов сохранение разрядной емкости CNT @ Li 2 FeSiO 4 Электрод @C остается на уровне 95,5%, 93,3%, 92,4% и 89,3% соответственно. Очевидно, CNT @ Li 2 FeSiO 4 @C имеет гораздо большую емкость и лучшую производительность при циклировании по сравнению с CNT @ Li 2 FeSiO 4 , что должно быть связано с его гораздо более высокой проводимостью [26, 27]. Насколько нам известно, циклические характеристики CNT @ Li 2 FeSiO 4 @C в этой работе демонстрирует намного лучшие характеристики езды на велосипеде по сравнению с предыдущими отчетами. Например, пористый Li 2 FeSiO 4 / C нанокомпозит, полученный золь-гель методом с винной кислотой, имел начальную разрядную емкость 176,8 мАч г -1 при 0,5 C и обратимой емкости 132,1 мАч г −1 при 1 С после 50 циклов [28]. Восстановленный оксид графена, модифицированный Li 2 FeSiO 4 Композит / C был синтезирован золь-гель методом на основе лимонной кислоты, который может обеспечить обратимую емкость 178 мАч г -1 при 0,1 ° C и сохранении емкости 94,5% после 40 циклов [29]. Причину лучших электрохимических свойств можно резюмировать в следующих трех частях. Во-первых, комбинация CNT и Li 2 FeSiO 4 может улучшить электропроводность материала. Во-вторых, Ли 2 FeSiO 4 при толщине всего 20–25 нм способствует диффузии иона лития. Наконец, углеродный слой, нанесенный на внешнюю сторону Li 2 FeSiO 4 может защитить внутреннюю структуру и дополнительно улучшить проводимость. Кроме того, графики производительности при езде на велосипеде CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 @C на рис. 4c дополнительно подтверждает вышеприведенное утверждение. Видно, что CNT @ Li 2 FeSiO 4 @C имеет более высокую производительность и емкость цикла, чем CNT @ Li 2 FeSiO 4 при плотности тока 0,2 С. Скоростные характеристики CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 @C показан на рис. 4d. Можно заметить, что разрядная емкость CNT @ Li 2 FeSiO 4 составляет 98,8 мАч г −1 , 81,3 мАч г −1 , 78,6 мАч г −1 и 62,4 мАч g −1 при 0,2, 0,5, 1 и 2 ° C соответственно. Пока CNT @ Li 2 FeSiO 4 Катод @C показывает намного лучшие характеристики, разрядная емкость 167,7 мАч г −1 , 125,8 мАч г −1 , 94,6 мАч г −1 и 70,6 мАч g −1 достигается при 0,2, 0,5, 1 и 2 ° C соответственно. Эти характеристики лучше, чем описанные в других аналогичных отчетах [30,31,32].
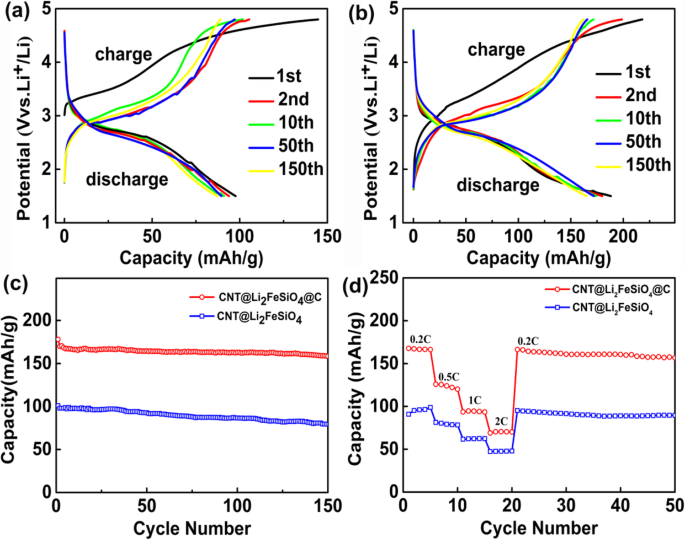
а Кривые заряда / разряда CNT @ Li 2 FeSiO 4 электрод из расчета 0,2 С, б кривые заряда / разряда CNT @ Li 2 FeSiO 4 Электрод @C из расчета 0,2 ° C, c производительность велосипеда CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 Электрод @C и d скорость работы CNT @ Li 2 FeSiO 4 и CNT @ Li 2 FeSiO 4 Электрод @C
Кривые CV в дальнейшем применяются для анализа кинетических характеристик CNT @ Li 2 FeSiO 4 @C катодный материал. На рис. 5а показан CV-профиль CNT @ Li 2 . FeSiO 4 @C при разных скоростях сканирования от 0,1 до 1,0 мВ с −1 .
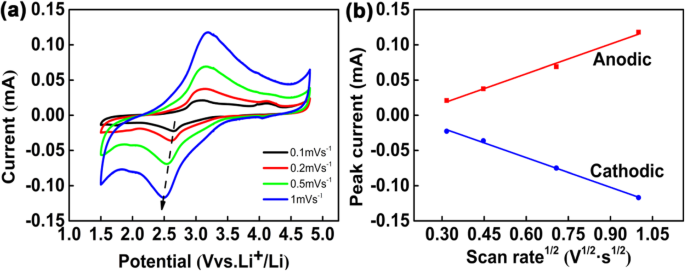
Кинетический анализ CNT @ Li 2 FeSiO 4 @C с использованием CV. а Профили CV с различной скоростью сканирования. б пиковый ток как функция квадратного корня из скоростей сканирования
Основные потенциалы окислительно-восстановительной пары, вызванные Fe 2+ / Fe 3+ реакции составляют 3,1 В (анодный) и 2,7 В (катодный), соответственно, что соответствует кривой гальваностатической платформы. Стоит отметить, что только один основной потенциал окислительно-восстановительной пары при 3,1 В (анодный) и 2,7 В (катодный), соответствующий Fe 2+ / Fe 3+ реакции наблюдаются, и Fe 3+ / Fe 4+ Подтверждено отсутствие окислительно-восстановительной пары. И результат CV соответствует данным зависимости dQ / dV от напряжения (дополнительный файл 1:Рисунок S3). Таким образом, можно сделать вывод, что только один Li + на формульную единицу вставляется и извлекается в процессе заряда / разряда.
Кроме того, положение пика окислительно-восстановительного пика немного изменяется с увеличением скорости сканирования, что указывает на небольшую реакцию поляризации CNT @ Li 2 FeSiO 4 @C катодный материал [28]. Коэффициент диффузии ионов лития в CNT @ Li 2 FeSiO 4 @C можно рассчитать по линейной зависимости между пиковым током Ip (A) и квадратным корнем из скорости сканирования v 1/2 ( v 1/2 s −1/2 ) из резюме (рис. 5б). Используя уравнение ниже [33, 34],
$$ \ mathrm {Ip} =2,69 \ times {10} ^ 5 {n} ^ {3/2} {\ mathrm {AD}} _ {\ mathrm {Li}} ^ {1/2} {\ mathrm { C}} _ {\ mathrm {Li}} ^ {\ ast} {v} ^ {1/2} $$Здесь n - количество электронов, участвующих в реакции, A относится к площади электрода, а C ∗ Ли обозначает объемную концентрацию Li + в электроде. На рисунке 5b показана хорошая линейная зависимость между Ip и v . 1/2 . Во время анодной и катодной реакций коэффициенты диффузии ионов лития составляют 7,32 × 10 −11 и 0,64 × 10 −12 см 2 s −1 , и эти коэффициенты превосходят предыдущие экспериментальные результаты [35, 36]. Это преимущество можно объяснить превосходной электропроводностью и эффективностью переноса ионов CNT @ Li 2 FeSiO 4 @C во время зарядки и разрядки. Электрохимическая импедансная спектроскопия (EIS) была использована для исследования электрохимических характеристик CNT @ Li 2 FeSiO 4 @C и CNT @ Li 2 FeSiO 4 . Дополнительный файл 1. На рисунке S4 показаны графики Найквиста CNT @ Li 2 . FeSiO 4 @C и CNT @ Li 2 FeSiO 4 электрод. Графики Найквиста состоят из высокочастотного полукруга, связанного с сопротивлением миграции литий-ионов ( R SEI ) через границу раздела твердого электролита (SEI), полукруг промежуточной частоты, вызванный сопротивлением переноса заряда на границе раздела катод-электролит ( R ct ), и линия наклона низкочастотной области, соответствующей диффузии литий-иона в катоде (область Варбурга) [36]. Сопротивление переноса заряда (76,5 Ом) CNT @ Li 2 FeSiO 4 @C значительно ниже, чем у CNT @ Li 2 FeSiO 4 (193,4 Ом), что указывает на то, что скорость переноса электронов CNT @ Li 2 FeSiO 4 @C выше.
Выводы
Таким образом, мы подготовили CNT @ Li 2 FeSiO 4 @C с помощью очень эффективной стратегии послойного стекирования. Гетероструктура ядро-оболочка CNT @ Li 2 FeSiO 4 @C улучшает проводимость, обеспечивает быстрое извлечение / введение ионов лития и уменьшает структурные повреждения. В результате он демонстрирует высокую производительность, цикличность и скорость. Следовательно, CNT @ Li 2 FeSiO 4 Катодный материал @C имеет многообещающую перспективу для использования в литий-ионных аккумуляторах.
Доступность данных и материалов
Все данные и материалы доступны в полном объеме без ограничений.
Сокращения
- CNT:
-
Углеродная нанотрубка
- CTAB:
-
Бромид цетилтриметиламмония
- Резюме:
-
Циклический вольтамперометрический
- EDX:
-
Энергодисперсионная рентгеновская спектроскопия
- EIS:
-
Электрохимическая импедансная спектроскопия
- HR-TEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- LIB:
-
Литий-ионные батареи
- NMP:
-
N -метил-2-пирролидон
- PVDF:
-
Поливинилиденфторид
- SEI:
-
Интерфейс твердого электролита
- SEM:
-
Сканирующая электронная микроскопия
- ТЕМ:
-
Просвечивающая электронная микроскопия
- TEOS:
-
Тетраэтоксисилан
- TGA:
-
Термогравиметрический анализатор
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Скальмаллой:новейший высокопроизводительный материал для 3D-печати на металле
- Образец высоко реактивной треугольной молекулы IBM и Warwick впервые
- Инструментальная сталь H13 для принтера Metal X
- Возобновляемые марки PVDF для литий-ионных батарей
- СИНТЕЗ И ЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА КАТОДНЫХ МАТЕРИАЛОВ LiNi0.5Mn1.5O4 с легированием композитов Cr3 + и F− для литий-…
- Многослойный композит MoS2 / ацетиленовый черный как эффективный анодный материал для литий-ионных батарей
- Иерархическая гетероструктура полых сфер ZnO @ TiO2 для высокоэффективного фотокаталитического выделения водор…
- Материал для следующего поколения интеллектуальных датчиков
- Вопросы и ответы:Оптимизация литий-ионных аккумуляторов для сверхбыстрой зарядки
- Какой материал сцепления лучше всего подходит для трения?



