Определение перекиси водорода на основе модификации внутренней поверхности твердотельных нанопор
Аннотация
Есть много методов обнаружения молекул. Но обнаружение молекул через твердотельные нанопоры в растворе - одна из многообещающих, высокопроизводительных и недорогих технологий, используемых в наши дни. В настоящем исследовании твердотельная платформа с нанопорами была изготовлена для обнаружения пероксида водорода (H 2 О 2 ), который не только не содержит этикеток, но и является важным участником окислительно-восстановительной реакции. Нами успешно изготовлен нитрид кремния (Si 3 N 4 ) нанопор диаметром ~ 50 нм с помощью сфокусированного пучка ионов Ga внутренняя поверхность нанопоры была модифицирована пероксидазой хрена (HRP) с помощью химии карбодиимидного сочетания. Иммобилизованные ферменты HRP обладают способностью вызывать окислительно-восстановительные реакции в одном канале нанопоры. Более того, единый агрегированный ABTS в реальном времени • + события молекулярной транслокации отслеживались и исследовались. Разработанный твердотельный биосенсор с нанопорами является обратимым и может применяться для обнаружения H 2 О 2 несколько раз.
Фон
Технология обнаружения нанопор основана на счетчике Коултера [1] и ионном канале клетки [2]. Nanopore обнаруживает заряженные молекулы, присутствующие в проходящем через нее растворе. Появление молекул в нанопоре, по-видимому, может изменить проводимость поры и, следовательно, изменить сигнал тока. Изменение тока дает информацию о размерах и концентрации молекул внутри поры, чтобы выявить динамический процесс поведения молекул при перемещении [3]. Некоторые наноразмерные объекты могут быть обнаружены с помощью нанопоры, например наночастицы [4,5,6], вирусы [7,8,9], белковые молекулы [10,11,12,13] и последовательности ДНК [14,15,16 , 17]. Нанопоры бывают двух типов. Биология нанопоры и твердотельные нанопоры. Биологические нанопоры имеют более низкое отношение сигнал / шум (SNR) и более высокое разрешение. Маленькие и развернутые белки могут быть обнаружены с помощью биологических нанопор [18,19,20,21,22,23]. Твердотельные нанопоры регулируются по размеру и обладают более высокой стабильностью. Твердотельные нанопоры обычно высверливаются на пленке, эта пленка делит жидкую ячейку на две части [24]. Напряжение смещения прикладывается к тонкой мембране, содержащей нанопору, в результате чего возникает ионный ток от одной клетки к другой [25]. Белковые молекулы, включая свернутые и развернутые структуры, обнаруживаются и анализируются с помощью твердотельных нанопор [26,27,28,29]. Взаимодействие белков также можно обнаружить с помощью твердотельных нанопор [30, 31]. Кроме того, он способен определять кинетику белков [32, 33]. Чтобы преодолеть ограничения диапазона обнаружения, широко применялись химически модифицированные твердотельные нанопоры [34,35,36,37,38,39], химически модифицированные твердотельные нанопоры применялись для обнаружения одноцепочечной ДНК. [40] и белки [41].
Для обнаружения H 2 уже применено множество количественных методов. О 2 , большинство из них основаны на спектрометрии [42,43,44,45], хемолюминесценции [46,47,48,49], амперометрии [50,51,52,53] и электрохимии [54,55,56,57] . Обычные спектрометрические и хемолюминесцентные методы обычно трудоемки и дороги. Твердотельный датчик с нанопорами отличается низким энергопотреблением и простой структурой, и его можно использовать для обнаружения небольших молекул.
Здесь мы представляем твердотельные нанопоры, модифицированные пероксидазой хрена (HRP). HRP были иммобилизованы на внутренней поверхности твердотельной нанопоры, иммобилизованные HRP оставались активными в окислительно-восстановительной реакции, которая происходила внутри одного канала нанопоры в присутствии H 2 О 2 [58]. ABTS • + образуется в окислительно-восстановительной реакции, будет агрегироваться, тогда агрегированный ABTS • + прошел через нанопоры. События транслокации могут быть обнаружены. Для обнаружения перекиси водорода твердотельная структура проста, и она может обнаруживать агрегированные ABTS • + за счет низкого расхода реагентов. Эта твердотельная нанопора, модифицирующая ферменты пероксидазы хрена (HRP), может образовывать перекись водорода (H 2 О 2 ) зондирование косвенно, через агрегированный ABTS • + обнаружение. Это имеет поучительное значение для обнаружения одиночных молекул и сборки молекул во внутренней твердотельной нанопоре.
Методы
Химические вещества и материалы
Молекула пероксидазы хрена (HRP) (1 мг / мл -1 , Enzyme Commission №1.11.1.7, 44 кДа) был приобретен у Xiya Reagent (Chengdu, China). Образец (HRP) растворяли в 0,02 мкм фильтрованном 0,1 M PBS, хранили при 4 ° C и использовали в течение двух дней после приготовления. Хлорид калия (KCl), N- (3-диметиламинопропил) -N'-этилкарбодиимид (EDC), N-гидроксисукцинимид (NHS) и 2,2'-азино-бис (3-этилбензотиазолин-6-сульфоновая кислота) ((ABTS ), 98%) были приобретены у DiBo chemical technology co., LTD (Шанхай, Китай). Перекись водорода (H 2 О 2 , 30%) был приобретен у Sinopharm Chemical Reagent Co., Ltd. (3-Аминопропил) триэтоксисилан (3-APTES) был приобретен у Sigma-Aldrich (Сент-Луис, Миссури, США). Эксперименты проводились с использованием чистой воды из системы очистки воды Milli-Q (удельное сопротивление 18,2 МОм / см, 25 ° C, Millipore Corporation, Биллерика, Массачусетс, США) и фильтровали через 0,02 мкм в системе FEI Strata 201 FIB (FEI Co., Hillsboro, OR, США), Zetasizer (Malvern Zetasizer Nano ZS) и Axopatch 700B (Molecular Devices, Inc., Саннивейл, Калифорния, США). Фотографии использованных нами инструментов были добавлены к дополнительному материалу (см. Дополнительный файл 1:Рисунок S1).
Изготовление твердотельных нанопор и электрические измерения
Во-первых, тонкая мембрана из Si 3 N 4 (Толщиной 100 нм) был нанесен на подложку Si толщиной 300 мкм. Затем проводится фотолитография (размер открытого окна 500 × 500 мкм 2 ). Затем поверхность мембраны бомбардировали ионами Ga + с использованием системы FEI Strata 201 FIB (FEI Co., Hillsboro, OR, USA) при ускоряющем потенциале 30 кВ, при этом измеренный ток составлял 1 пА. Время измельчения в точечном режиме составляло 1,5 с. Наконец, были получены твердотельные чипы с нанопорами и очищены в свежеприготовленном растворе пираньи при 80 ° C в течение 30 минут с последующей промывкой ультрачистой водой. После очистки чип был собран в специально изготовленной тефлоновой ячейке с двумя уплотнительными кольцами из витона для разделения двух сторон чипа и формированием двух резервуаров, обеспечивающих единственный путь для ионного тока через нанопору. Фотографии использованного нами оборудования были добавлены к дополнительному материалу (см. Дополнительный файл 1:Рисунок S2). Электроды (Ag / AgCl) были подключены к жидкостной ячейке и усилителю патч-зажима (Axopatch 700B, Molecular Devices, Inc., Саннивейл, Калифорния, США), который позволял измерять ионный ток при постоянных напряжениях с частотой дискретизации сигналов 100 кГц. . Внутренний восьмиполюсный фильтр Бесселя нижних частот усилителя был установлен на 10 кГц [3]. Весь инструмент был помещен в двойную клетку Фарадея.
Результаты и обсуждение
Иммобилизация нанопор с помощью HRP
Выбранную нанопору диаметром ~ 50 нм погружали в раствор пираньи при 80 ° C на 30 мин. После обработки раствором пираньи внутренняя поверхность нанопоры могла захватывать гидроксильные группы кремния. Затем всю тонкую пленку активировали (3-аминопропил) триэтоксисиланом (3-APTES). В результате обработки 3-АПТЕСами амино (-NH 2 ) группы были сформированы на поверхности пленки.
После активации (3-аминопропил) триэтоксисиланом (3-APTES) чип с нанопорами помещали в 0,1 М раствор PBS N- (3-диметиламинопропил) -N'-этилкарбодиимида (EDC) (10 мМ) и N-гидроксисукцинимида ( NHS) (20 мМ). После этого нанопористый чип вводили в пероксидазу хрена (HRP) (10 нг / мл). Согласно результатам предыдущих исследований нашей группы [3], при различной концентрации соли от 0,1 до 2 М KCl, pH 7,0, HRP не агрегировался. За счет pI значение пероксидазы хрена, равное 4,3 ± 0,2, мы также доказали, что HRP не агрегировалась в 0,1 М KCl, pH 6,0 и pH 7,0. Реагент EDC активировал карбоксильные (-COOH) группы HRP с образованием высокореактивного промежуточного соединения о-ацилизомочевины. Кроме того, промежуточное соединение в дальнейшем превращалось в более стабильный сукцинимидиламин-реактивный эфир в присутствии NHS [58]. В результате происходит ковалентное связывание промежуточного соединения с (-NH 2 ) на внутренних поверхностях нанопор с образованием стабильных амидных связей (рис. 1).
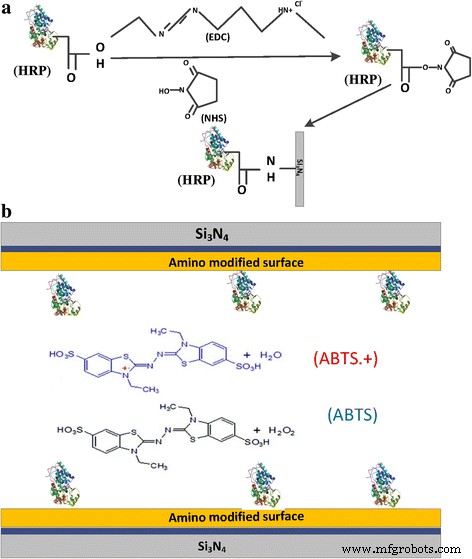
Выполнение процесса модификации в одиночном канале с твердотельными нанопорами. а Схематическое изображение ковалентного присоединения пероксидазы хрена (HRP) к одному каналу нанопоры посредством химии карбодиимидного связывания. Карбоксильные (-COOH) группы HRP были активированы раствором EDC, что позволило HRP реагировать с (-NH 2 ), генерируемые на поверхности чипа с нанопорами. б Схема сенсора пероксида водорода на иммобилизованной HRP, внутренняя поверхность сенсора модифицирована HRP. Когда H 2 О 2 и ABTS произошли, ABTS • + произведен. Кристаллическая структура HRP была использована с разрешения автора [3]
Эти процессы приводят нас к иммобилизации HRP на внутренней поверхности одиночной нанопоры. Реализация процесса функционализации была подтверждена измерением вольт-амперной характеристики ( I-V ) одной нанопоры до и после модификации (рис. 2).
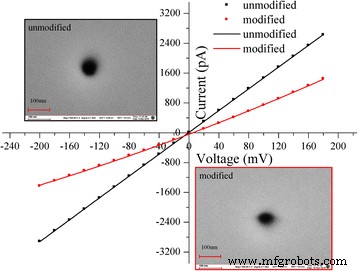
Выполнение типичного тока-напряжения ( I-V ) кривые немодифицированной (исходной) и модифицированной нанопоры в 0,1 M KCl, забуференной при pH 7,0 0,1 M PBS. черная линия это I-V кривые немодифицированной нанопоры и красная линия это I-V кривые модифицированной нанопоры с HRP. вставки сканирующая электронная микроскопия (SEM) одиночной нанопоры (диаметр ~ 50 нм цис) и датчик нанопоры. 100 нм - масштаб
Характеристика модифицированных твердотельных нанопор HRP
Здесь форма одиночного Si 3 N 4 канал нанопор имеет цилиндрическую форму. На рисунке 2 показан типичный ток-напряжение ( I-V ) кривые немодифицированной (исходной) и модифицированной нанопоры в 0,1 M KCl, забуференной при pH 7,0 0,1 M PBS. После модификации внутренней поверхности нанопор ферментами HRP размер пор стал меньше.
Согласно Вануну и др., Принимая во внимание проводимость внешней части нанопоры, диаметр твердотельной нанопоры можно рассчитать по следующему уравнению:
$$ d =\ left (1+ \ sqrt {1+ \ frac {16 \ sigma l} {\ pi G}} \ right) G / 2 \ sigma $$ (1)Где, d и l диаметр и длина поры, G - проводимость открытой поры нанопоры, σ - проводимость ионного раствора.
Учитывая геометрические эффекты, после модификации твердотельной нанопоры ферментами HRP можно рассчитать эффективный размер. Диаметр отдельной нанопоры можно рассчитать на основе уравнения (1). Где значение проводимости ( G без изменений ) составляет ~ 15 нСм, может быть получено из I-V кривые немодифицированной твердотельной нанопоры. Электропроводность ( σ ) раствора ионов 0,1 M KCl (25 ° C), забуференного при pH 7,0 0,1 M PBS, составляет ~ 1,28 См / м. Следовательно, диаметр немодифицированной нанопоры составляет ~ 51 нм, он аналогичен измеренному диаметру. Используя тот же метод, полученное значение проводимости ( G изменено ) составляет ~ 7,5 нСм, и можно рассчитать диаметр (~ 34 нм) модифицированной нанопоры. Уменьшение диаметра возможно по следующим двум причинам:первая - это обработка внутренней поверхности нанопоры (3-аминопропил) триэтоксисиланом (3-APTES), что позволяет поверхности нанопоры принимать (-NH 2 ) аминогруппы. Вторая причина заключается в том, что гидродинамический диаметр ( D h ) фермента HRP составляет ~ 8 нм [3], иммобилизованные HRP могут уменьшить диаметр поры. Здесь твердотельная нанопора, модифицированная HRP, диаметром ~ 34 нм используется в качестве канала обнаружения пероксида водорода.
Принцип окислительно-восстановительной реакции
Окислительно-восстановительная реакция проводилась внутри одной модифицированной нанопоры, и представленный ниже процесс реакции хорошо согласуется с предложенной окислительно-восстановительной реакцией [58]. При наличии H 2 О 2 (0,5 мМ) ферменты HRP, иммобилизованные на внутренней поверхности нанопоры, немедленно превращались в соединение 1. Затем соединение 1 приняло один электрон от восстанавливающей молекулы субстрата ABTS (1,5 мМ) для образования соединения 2. Затем соединение 2 было восстановлено обратно до покоящегося фермента посредством переноса одного электрона от другой молекулы субстрата ABTS.
Катионные продукты (ABTS • + ) окислительно-восстановительных реакций накапливались в одной нанопоре. Перемещение накопленных молекул из канала нанопор приведет к изменению проводимости ( G ), и, следовательно, изменение тока ( ΔI б ) можно найти.
$$ \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {3 +} \ right) \ mathrm {Porp} + {\ mathrm {H}} _ 2 { \ mathrm {O}} _ 2 \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) {\ mathrm {Porp}} ^ {\ cdotp +} \ left (\ mathrm {Compound} \ 1 \ right) + {\ mathrm {H}} _ 2 \ mathrm {O} $$ $$ \ mathrm {H} \ mathrm { R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) {\ mathrm {Porp}} ^ {\ cdotp +} + \ mathrm {ABTS} \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) \ mathrm {Porp} \ left (\ mathrm {Compound} \ 2 \ right) + {\ mathrm {ABTS}} ^ {\ cdotp +} $$ $$ \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe }} ^ {4 +} =\ mathrm {O} \ right) \ mathrm {Porp} + \ mathrm {ABTS} \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {3 +} \ right) \ mathrm {Porp} + {\ mathrm {ABTS}} ^ {\ cdotp +} + {\ mathrm {H}} _ 2 \ mathrm {O} $$Обнаружение событий перемещения
Эксперименты проводились с использованием модифицированных пероксидазой хрена (HRP) нанопор с измененным диаметром пор (~ 34 нм) в 0,1 М KCl, забуференных при pH 7,0 0,1 М PBS. 2, 2'-Азинобис- (3-этилбензтиазолин-6-сульфонат (ABTS) (1,5 мМ) и пероксид водорода (H 2 ) О 2 ) (0,5 мМ) добавляли в транс-компартмент нанопоры. После добавления ABTS и H 2 О 2 были выполнены эксперименты с использованием напряжений смещения от -100 до -800 мВ, и они были дискретизированы с частотой 100 кГц. Событий транслокации не было, пока напряжение не увеличилось до -400 мВ. На рисунке 3 показаны характерные следы ионного тока события транслокации при различных напряжениях от -400 до -800 мВ в 0,1 М KCl, 0,1 М PBS, pH 7,0. К дополнительному материалу были добавлены данные экспериментов по длительным транслокационным событиям при различных напряжениях (см. Дополнительный файл 1:Рисунок S3).
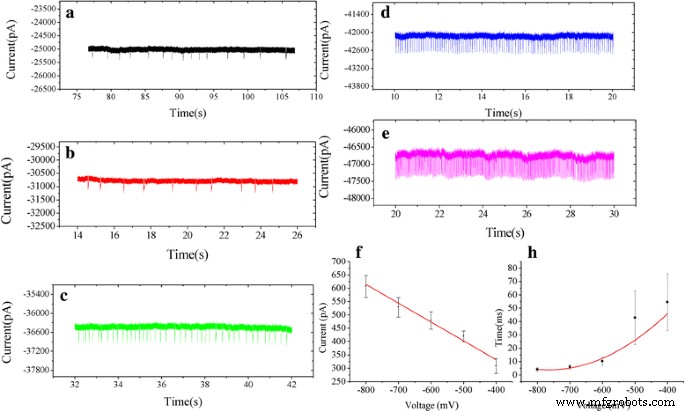
а - е Схематическое изображение событий транслокации при различных напряжениях от -400 до -800 мВ. Частота событий транслокации увеличивалась при увеличении приложенного напряжения с -400 мВ до -800 мВ. е Амплитуда тока линейно увеличивается с увеличением напряжения. ч Экспоненциально убывающая функция ( t d ~ e -v / v0 ) использовался для подбора времени выдержки в зависимости от приложенного напряжения
Наблюдали события миллисекундной блокады тока, проводимые в 0,1 М KCl, 0,1 М PBS, pH 7,0. Добавляя реагент H 2 О 2 и ABTS в транскомпартмент, ферменты HRP иммобилизовались на внутренней поверхности одиночного канала нанопоры, и произошла окислительно-восстановительная реакция. Обилие ABTS • + были произведены молекулы, одна молекула меньшего размера ABTS • + не могут быть обнаружены с помощью нашей твердотельной нанопоры из-за разрешающей способности системы [3]. Однако после образования эти молекулы будут агрегироваться. Следовательно, можно обнаружить ABTS • + молекулы. Здесь отрицательные напряжения удерживались и суммировались ABTS • + молекулы прошли через нанопоры. При приложении отрицательного напряжения наблюдался электрофоретический и электроосмотический поток. HRP был заряжен отрицательно в 0,1 M KCl, 0,1 M PBS, pH 7,0 [3], в результате образовался бы двойной электрический слой, и электроосмос был бы направлен в сторону отрицательного электрода. По этой причине электрофорез и электроосмос были в одном направлении. Агрегированные ABTS • + в канале с одной нанопорой будет переноситься через твердотельную нанопору в направлении отрицательного электрода.
Статистический анализ событий перемещения
Поскольку напряжение смещения играет ключевую роль в перемещении агрегированных ABTS • + , влияние текущих блокад агрегированных АБТС • + прохождение через модифицированные нанопоры HRP в зависимости от приложенного напряжения. Частота возникновения событий транслокации значительно улучшилась с увеличением напряжения (рис. 3f). По мере увеличения напряжения увеличивается и амплитуда тока. Однако события транслокации постепенно исчезали, когда напряжение смещения поддерживалось ниже -300 мВ, что предполагало, что агрегированные ABTS • + через модифицированные нанопоры HRP требовалось пороговое напряжение -300 мВ. На рисунке 4 показаны гистограммы средней текущей амплитуды событий транслокации, измеренные для агрегированных ABTS • + при разном напряжении. На основе аппроксимирующих кривых пиковые значения текущей блокировки ( ΔI б ) составляют 308,4 ± 27,795 пА, 419,1 ± 20,354 пА, 478,8 ± 32,857 пА, 528,1 ± 36,98 пА, 606,9 ± 40,916 пА при -400, -500, -600, -700 и -800 мВ соответственно, вероятно, что уменьшение тока вызвано агрегированным ABTS • + молекула, проходящая через нанопору при разных напряжениях. Значения амплитуды тока были подогнаны с помощью полиномиальной функции первого порядка, которая дает наклон -0,706 и точку пересечения 49,262. Однако на основе аппроксимирующих кривых значения времени выдержки составляют 54,5 ± 21,374 мс, 42,8 ± 20,181 мс, 10,3 ± 3,05 мс, 6,0 ± 1,744 мс, 4,0 ± 1,441 мс, при -400, -500, -600, - 700 и −800 мВ. На рисунке 3h показана экспоненциально убывающая функция ( t d ~ e -v / v0 ) использовался для подбора времени выдержки в зависимости от приложенного напряжения. Гистограммы времени пребывания событий транслокации были добавлены к дополнительному материалу (см. Дополнительный файл 1:Рисунок S4).
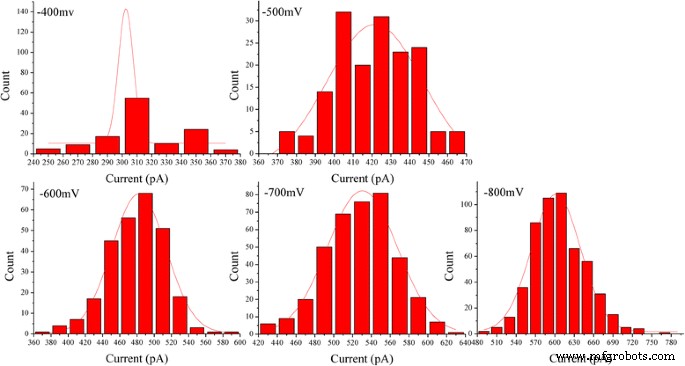
Гистограммы средней текущей амплитуды событий транслокации, измеренные для агрегированных ABTS • + при разных напряжениях (-400, -500, -600, -700, -800 мВ) в 0,1 М KCl, 0,1 М PBS, pH 7,0. Все гистограммы были подогнаны к распределению Гаусса
Текущая блокада в сравнении с временем задержки событий для каждой агрегированной ABTS • + при различных напряжениях были подобраны на двумерных диаграммах рассеяния (рис. 5). Все агрегированные ABTS • + показать кластер событий от -400 до -800 мВ, основные кластеры событий связаны с агрегированными ABTS • + проходя через модифицированные твердотельные нанопоры HRP.
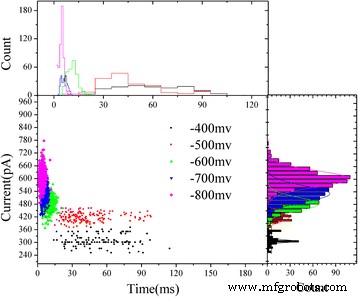
Двумерные графики разброса текущей блокировки в зависимости от времени ожидания события для каждого агрегированного ABTS • + при разном напряжении. Справа и вверху нанесены соответствующие ему гистограммы. Все гистограммы были подогнаны к распределению Гаусса
Кроме того, было проанализировано единичное событие транслокации при каждом напряжении, и текущая блокада была вызвана тем же размером и заряженным веществом. Таким образом, считается, что каждое событие транслокации было вызвано одним агрегированным ABTS • + . Для анализа времени транслокации агрегированных ABTS • + в наших экспериментах. Текущая продолжительность блокады t d рассматривается как время ожидания одного агрегированного ABTS • + от места, где он образовался, до выхода нанопоры. Здесь было рассмотрено другое условие:некоторые ферменты HRP могут быть иммобилизованы на входе нанопоры, и это может катализировать окислительно-восстановительную реакцию. Поэтому были проведены другие эксперименты, чтобы убедиться, что окислительно-восстановительная реакция происходит на внутренней поверхности одиночной нанопоры, а не на входе. Для проверки были применены и проанализированы немодифицированные HRP. Эти нанопоры были активированы 3-APTES. И такая же концентрация HRP (10 нг / мл), ABTS (1,5 мМ) и H 2 О 2 (0,5 мМ) добавляли в транс-отсек нанопоры, отрицательное смещенное напряжение прикладывали в 0,1 M KCl, 0,1 M PBS, pH 7,0, из-за силы электрофореза HRP не могли проходить через нанопору. Вследствие окислительно-восстановительной реакции агрегированный ABTS • + продуцируются, но событий транслокации обнаружено не было. Возможно, что агрегированный ABTS • + вызывают электростатический эффект с HRP и предотвращают агрегирование ABTS • + проходя через нанопоры.
На рисунке 6 показаны двумерные диаграммы разброса изменения проводимости ( ΔG ) по сравнению со временем ожидания события для каждого агрегированного ABTS • + при разном напряжении. Можно обнаружить, что изменение проводимости ( ΔG ) в основном сконцентрировано в 0,8 нСм. Форма событий транслокации почти такая же. Среднее значение ΔG составляет ~ 0,8 нСм при разных напряжениях. Можно предположить, что исключение объема каждого агрегированного ABTS • + молекула почти такая же. Возможно, что электростатические и стерические эффекты агрегированных ABTS • + молекулы могут изменять ионный ток. После анализа две типичные формы текущих следов с положительно заряженными агрегированными ABTS • + транслокации не наблюдались (рис. 7). События транслокации при -700 мВ в качестве представителя. Процент событий двух типов был проанализирован, и можно заметить, что процент событий типа 1 увеличивался с увеличением напряжения, с другой стороны, процент событий типа 2 уменьшался. Считалось, что более высокое напряжение ускоряет перемещение, чем более низкое напряжение.
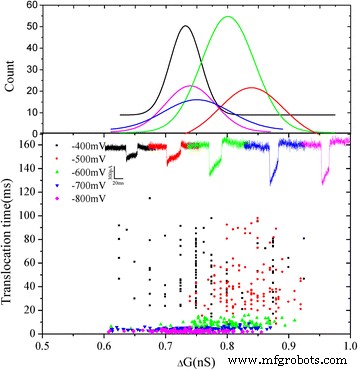
Схематическое изображение двумерных диаграмм рассеяния ΔG по сравнению с временем ожидания событий для каждой агрегированной ABTS • + при разном напряжении. Соответствующие кривые подгонки были расположены выше. вставка - это события перемещения различных напряжений (от -400 до -800 мВ)
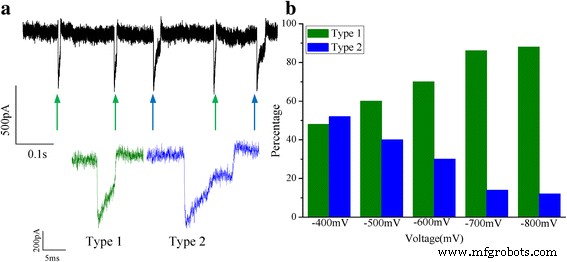
а Схема двух типов транслокационных событий при напряжении -700 мВ. б Процент событий двух типов при разных напряжениях (−400, −500, −600, −700, −800 мВ)
Текущие сигналы блокады показали размер, структуру и взаимодействие агрегированных ABTS • + проходя через единственный канал нанопоры. Что касается изменения текущей формы, предполагался процесс изменений. Для события 1 сигналы тока имеют типичную флуктуационную часть с большой интенсивностью и коротким временем пребывания. Возможно, что агрегированный ABTS • + проходит через нанопору с места, где она образовалась. Когда агрегированный ABTS • + проходя через нанопору, ионный ток нанопоры восстанавливается до исходного уровня (базовый уровень) ( I 0 ). Для события 2 сигналы тока имеют флуктуационную часть с большой интенсивностью, а затем имеют горизонтальную стадию. Такая форма сигналов может быть объяснена электростатическим взаимодействием агрегированных ABTS • + с HRP на выходе из нанопоры, и ток медленно восстанавливался до базового уровня. Чтобы лучше понять текущее изменение, нам нужно начать с изменения проводимости открытых пор ( G поры ) при концентрации соли (0,1 М KCl). Как обсуждалось в предыдущих исследованиях, уравнение проводимости открытой поры отрицательно заряженной нанопоры диаметром d и длиной l при низкой концентрации соли можно описать как
$$ {G} _ {p ore} =\ frac {\ pi {d ^ 2} _ {p ore}} {4 {l} _ {p ore}} \ left [\ left ({\ mu} _ { K ^ {+}} + {\ mu} _ {C {l} ^ {-}} \ right) {n} _ {K Cl} \ cdot e + {\ mu} _K \ frac {4 {\ sigma} _p } {d_ {p ore}} \ right] $$ (2)где μ К и μ Cl - электрофоретическая подвижность K + и Cl - , n KCl это плотность числа K + и Cl - , элементарный заряд равен e, σ p - поверхностная плотность заряда поверхности нанопор. В этом эксперименте твердотельная нанопора была химически модифицирована, и диаметр нанопоры был изменен. Плотность поверхностного заряда поверхности нанопор ( σ p ) не может быть получен точно. Следовательно, проводимость открытых пор ( G поры ) рассчитывалась по уравнению (1). С учетом уравнения (1) проводимость открытой поры ( G поры ) составляет ~ 7,5 нСм. Предполагается, что изменение проводимости можно объяснить двумя причинами [15]. Первая причина заключается в том, что объемное исключение ионов в нанопоре было занято агрегированными ABTS • + молекулы. В результате проводимость твердотельной нанопоры уменьшилась ( ΔG - ). Вторая причина заключается в том, что некоторые ионы были перенесены из нанопоры агрегированным ABTS • + молекулы, которые увеличивают проводимость твердотельной нанопоры. В этих экспериментах ABTS • + производился внутри нанопоры, и никакие ионы не приносились. Следовательно, изменение проводимости твердотельной нанопоры ( ΔG ) был вызван только исключением объема. Итак, полное изменение проводимости можно описать как
$$ \ varDelta G =\ varDelta {G} ^ {-} $$ (3)Уменьшение проводимости твердотельной нанопоры вызвано исключением объема, и его можно рассчитать по следующему уравнению
$$ \ varDelta {G} ^ {-} =\ sigma \ frac {\ gamma \ varLambda} {{\ left (l + 0.8 d \ right)} ^ 2} $$ (4)где γ - коэффициент формы частицы, который представляет собой отношение площадей поверхности одного и того же сферического объема и частицы. В этой работе агрегированный ABTS • + молекула была упрощена до глобального объекта, поэтому значение γ равно 1 и Λ исключение тома. Электропроводность объемного раствора σ составляет 1,28 См / м, 0,1 М KCl (25 ° C).
Для исключения объема ( Λ ), мы можем сделать выводы из событий перемещения некоторых других молекул. Для подключения изменения проводимости ( ΔG ) к физическим свойствам молекул, закон Ома может быть применен к изменению объема раствора электролита на основе твердотельной нанопоры [59]. Когда происходит перемещение молекулы в цилиндрическую твердотельную нанопору, ток мгновенно уменьшается. Когда сопротивление твердотельной нанопоры равно сопротивлению всей цепи, изменение проводимости ( ΔG ) можно описать следующим уравнением
$$ \ varDelta G (t) =- {G} _ {p ore} \ frac {\ varLambda (t)} {H_ {eff} {A} _p} \ left [1+ f \ left ({d} _m / {D} _p, {l} _m / {H} _ {eff} \ right) \ right] $$ (5)В этом уравнении A p H эфф =V p - объем твердотельной нанопоры, f ( г м / D p , лм / выс. эфф ) является поправочным коэффициентом (он не учитывает эффект поверхностного заряда), в наших экспериментах мы упростили агрегированный ABTS • + молекула к глобальному объекту; следовательно, поправочный коэффициент равен 1. d м / D p - отношение диаметра молекулы к диаметру нанопор, лм / H эфф - отношение эффективной длины молекулы к эффективной длине наопоры. Выражение (5) можно упростить как
$$ \ varDelta G / {G} _ {p ore} \ приблизительно \ varLambda / {V} _p $$ (6)Среднее значение проводимости ( G поры ) был проанализирован транслокационные события. Из уравнения (5) среднее значение исключения объема ( Λ ) при разных напряжениях (-400, -500, -600, -700, -800 мВ). Между тем известен размер используемой нанопоры, объем нанопоры ( V p ) составляет ~ 90746 нм 3 . С учетом уравнения (4) значение изменения проводимости ( ΔG - ) можно рассчитать как ~ 0,6 нСм. Среднее значение изменения проводимости, полученное в экспериментах по транслокации при различных напряжениях (-400, -500, -600, -700, -800 мВ), составляет ~ 0,784 нСм. Можно обнаружить, что расчетное значение близко к экспериментальному значению.
В некоторых предыдущих исследованиях было достигнуто обнаружение молекул перекиси водорода с помощью различных технологий. Но обнаружить перекись водорода по наноканалу редко. Tan et al. [3] дифференцировали разные сигналы событий, когда HRP проникали в нанопоры, были ABTS и H 2 О 2 в растворе KCl. Сигналы разного типа с транслокацией HRP были расценены как ABTS • + проходя через нанопоры. Проанализировано шесть типичных событий транслокации продукта субстратов ферментативного катализа. Они размышляли о возможных процессах каждого типа. Однако для дачи показаний недостаточно доказательств. Мубарак Али и др. удалось обнаружить продукты окислительно-восстановительной реакции внутри единичных конических наноканалов [58]. Они обнаружили, что катионный радикал ABTS • + reduced the ion current in the HRP-nanochannel in a voltage-dependent fashion, consistent with voltage-dependent concentrations of ions in conical nanochannels. The magnitude of the current blockage was correlated with the H2 О 2 concentration in the solution.
Выводы
In conclusion, we fabricated a Si3 N4 nanopore employing a FIB successfully, a single naonopore system whose surface was modified with covalently linked HRP enzymes. The effect of the immobilized HRPs enzymes in a single solid-state nanopore as a hydrogen peroxide (H2 О 2 ) sensor was affirmed by investigating products (ABTS •+ ) of the redox reactions occurring in presence of the substrates H2 О 2 and ABTS. The aggregated cationic radical ABTS •+ produced inside the solid-state nanopore and reduced the ionic current in the HRPs modified solid-state nanopore, are consistent with voltage-dependence. The current blockade trends showed linear dependence for applied biased voltages. The relationship between the dwell time versus applied biased voltage was the exponentially decaying (t d ~ e −v/v0 ). Meanwhile, the aggregated ABTS •+ passed through the HRPs modified nanopores needed a −300 mV threshold voltage. The change of conductance (ΔG) has been calculated analytically and compared to the measured experimental values. The translocation events were produced by the certain size aggregated cationic radical ABTS •+ . We expect that using solid-state nanopores will allow lowering the detection limit and improve the system sensitivity. For our solid-state nanopore system, the structure is simple; it is not susceptible to fouling and can be used multiple times.
Сокращения
- 3-APTES:
-
(3-Aminopropyl)triethoxysilane
- ABTS:
-
3-ethylbenzothiazoline-6-sulfonic acid
- EDC:
-
N-(3-dimethylaminopropyl)-N’-ethylcarbodiimide
- FIB:
-
Focused ion beam
- HRP:
-
Horseradish peroxidase
- KCl:
-
Potassium chloride
- NHS:
-
N-гидроксисукцинимид
- SEM:
-
Сканирующая электронная микроскопия
- SNR:
-
Signal to noise ratio
Наноматериалы
- Твердотельный LiDAR предлагает более простое решение для автомобильных датчиков.
- Нанокремний для производства водорода
- Полупроводниковые нанокристаллы помогают производить водородное топливо
- Нанографема, гибкая прозрачная память на основе кремния
- Углеродные наноточки как двухрежимные нанодатчики для селективного обнаружения перекиси водорода
- Определение перекиси водорода на основе модификации внутренней поверхности твердотельных нанопор
- Плазмонный датчик на основе диэлектрических нанопризм
- Оценка накопления энергии суперконденсатором на основе дробно-дифференциальных уравнений
- Твердотельные нанопоры
- Ambarella, Lumentum и ON Semiconductor совместно работают над трехмерным зондированием на основе искусственного интеллекта д…



