Виртуальный скрининг на основе фармакофоров для перепрофилирования лекарств
Переназначение лекарств - это давно устоявшаяся стратегия выявления новых применений одобренных или исследуемых терапевтических средств, выходящих за рамки первоначального медицинского показания. 1 С тех пор, как по счастливой случайности препарат, предназначенный для лечения гипертонии и стенокардии, превратился в печально известную «маленькую синюю таблетку» Pfizer, обычно называемую виагрой, не было такой видимости в общественном мнении. Глобальная актуальность терапевтических средств для лечения COVID-19 снова привлекла внимание общественности к этой лекарственной стратегии.
Трехмерное моделирование белков включает в себя несколько методов молекулярного моделирования и моделирования для перепрофилирования лекарств. В предыдущей публикации этой серии молекулярный докинг исследовался как метод выявления возможных ингибиторов, связывающихся с основной протеазой SARS-CoV-2. Можно ли альтернативу in silico такие методы, как моделирование фармакофора, позволяют получить сопоставимые результаты и предоставить дополнительные доказательства, подтверждающие выбор одного кандидата по сравнению с другим?
Выбор альтернативного маршрута
Моделирование фармакофоров обеспечивает абстракцию молекулярных характеристик, которые необходимы для распознавания лиганда белковой мишенью. Его представление о молекулярных взаимодействиях и связывании обеспечивает противоположную перспективу по сравнению с классическими методами моделирования.
Мы получили исходный набор данных о нескольких основных белковых структурах протеазы SARS-CoV-2 от Diamond Light Source. 2 Мы выровняли эти структуры, а затем использовали протокол «Генерация фармакофоров взаимодействия», доступный в BIOVIA Discovery Studio, для создания фармакофоров, представляющих несвязанные взаимодействия каждого комплекса рецептор-лиганд. Общее количество характеристик в фармакофорах варьировалось от двух для кристаллических структур 5R80 и 5R7Y до модели с девятью характеристиками для 6LU7. Мы объединили фармакофоры из отдельных комплексов в единую модель и отредактировали тесно сгруппированные характеристики. Окончательная модель включала 14 функций, которые представляют межмолекулярные контакты между протеазой и возможными связующими небольшими молекулами.
Впоследствии мы выполнили in silico мутагенез со сканированием аланином остатков активного сайта всех комплексов для определения того, какие остатки снижают аффинность связывания (горячую точку) этого комплекса белок-лиганд при мутации. Из всех комплексов мы идентифицировали восемь остатков (HIS41, MET49, ASN142, HIS163, MET165, PRO168, GLN189 и GLN192) в качестве горячих точек по крайней мере в одном комплексе и три остатка, которые были горячими точками по крайней мере в четырех комплексах. В модели фармакофоров с 14 признаками шесть признаков соответствовали взаимодействиям с одним из восьми горячих остатков. Второй набор данных нековалентного M PRO лигандные комплексы, выпущенные Diamond Light Source 2 выявили ряд различных способов связывания, что привело нас к разделению шести ключевых характеристик фармакофоров на две группы для использования на следующем этапе виртуального скрининга.
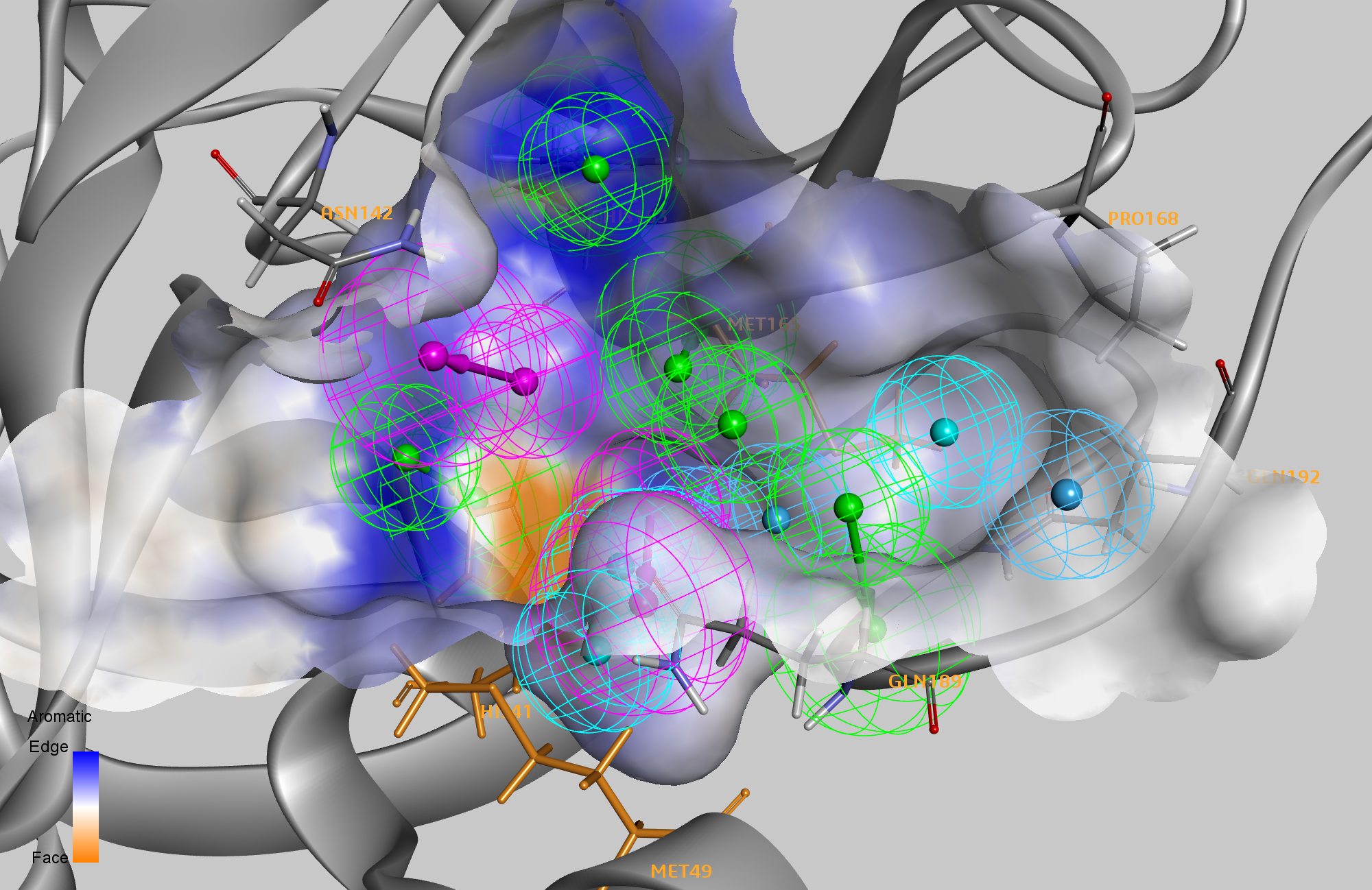
Теперь мы использовали эту фармакофорную модель для выполнения виртуального скрининга выбранной библиотеки, содержащей 2650 одобренных FDA лекарств, которые имеют несколько подтверждений лиганда, предварительно сгенерированных для быстрого поиска. Мы проверили эти лиганды по отношению к фармакофорам с 14 признаками с требованием, чтобы по крайней мере один признак из каждой из двух требуемых групп должен был совпадать, а также по крайней мере два признака из оставшихся восьми признаков, чтобы идентифицировать попадание. Это сделано для того, чтобы позволить разнообразное исследование различных способов связывания лигандов, а также гарантировать, что сохраняются только позы, которые могут образовывать по крайней мере два взаимодействия со значительными остатками, идентифицированными в мутагенезе со сканированием аланина. Алгоритм по существу исследует более 12 000 возможных комбинаций фармакофоров. Затем мы минимизировали наиболее подходящие совпадения для каждой комбинации фармакофора в белке. Наконец, мы определили энергии связывания оптимизированных поз, полученных из фармакофора, используя CHARMm с обобщенной моделью Борна с использованием модели неявного растворителя молекулярного объема (GBMV). Этот метод фактически представляет собой расчет молекулярной стыковки (как в нашем предыдущем блоге), но здесь мы использовали нашу оптимизированную модель фармакофоров, чтобы ограничить и отфильтровать стыкованные результаты.
Мы рассчитали несвязанные взаимодействия каждой позы и отфильтровали, чтобы сосредоточиться только на тех позах, которые взаимодействуют с четырьмя ключевыми остатками - HIS41, MET49, CYS145 и MET165. HIS41, MET49 и MET165 были тремя остатками, общими по крайней мере для четырех комплексов, идентифицированных ранее, а CYS145 является вторым остатком в значительной каталитической диаде HIS41 / CYS145, обнаруженной в каждой субъединице основного гомодимера протеазы. Мы отсортировали совпадения с рассчитанной свободной энергией связи, чтобы определить десять наиболее вероятных кандидатов для дальнейшего исследования. Ритонавир был единственным распространенным лигандом, идентифицированным здесь и в предыдущем блоге. Ритонавир имел седьмое место по величине свободной энергии связывания, а также ранее занимал седьмое место в исследовании стыковки. Ритонавир в настоящее время проходит ряд клинических испытаний на COVID-19. 3
Видео 1 :Лучшая поза для ритонавира, взаимодействующего с HIS41, MET49, SER144, CYS145, MET165, GLU166 и GLN189.
Лучшим лигандом для оценки в представленном здесь методе был монтелукаст, антагонист цистеинилового лейкотриенового рецептора. В недавно опубликованной статье была выдвинута гипотеза о его использовании для ограничения прогрессирования заболевания при заражении COVID-19. 4
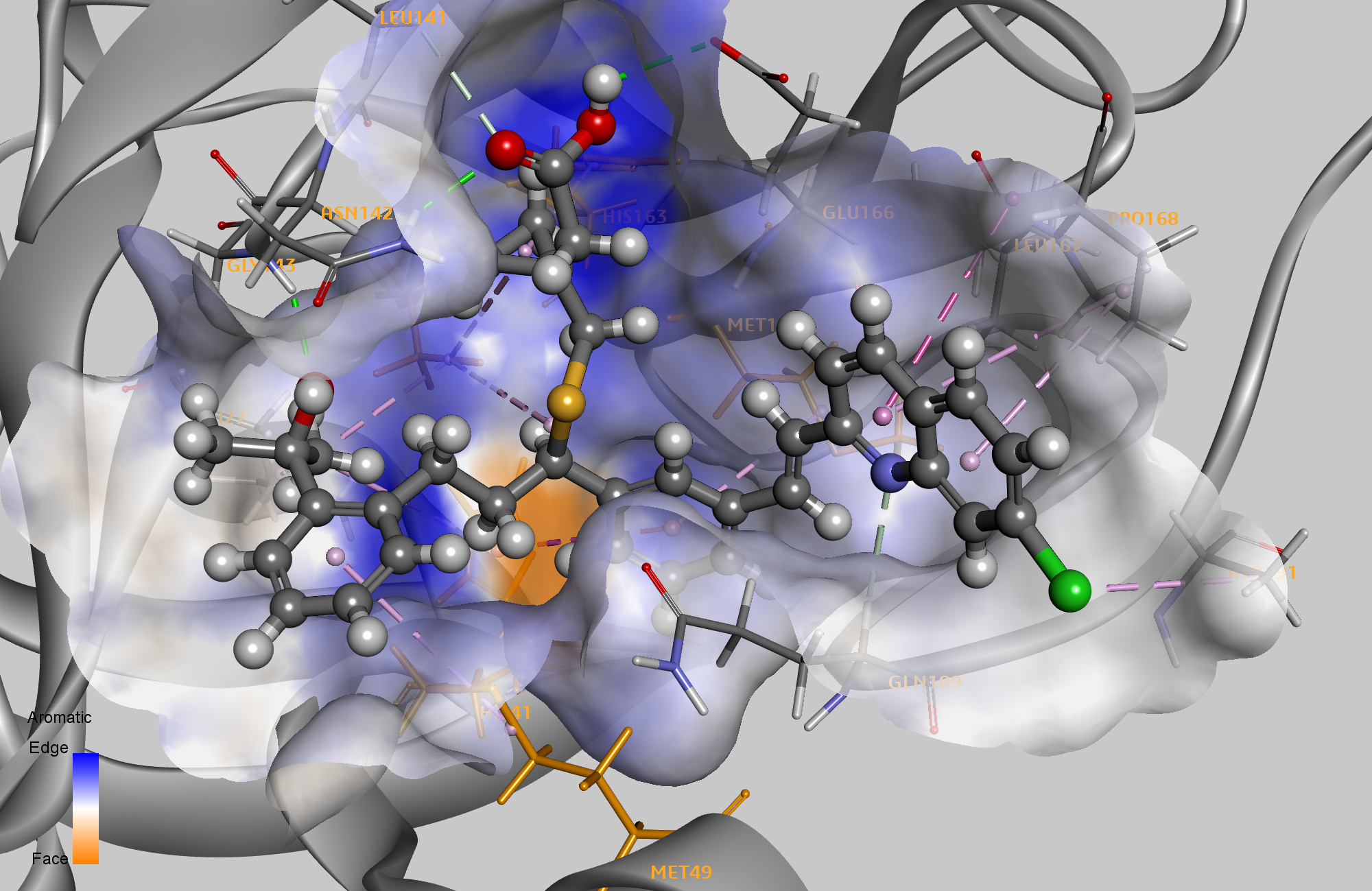
Три дополнительных соединения, получивших наибольшее количество баллов, включали препараты телмисартан, моэксиприл и гидроксиклорхин. Потенциал всех этих соединений в качестве повторно используемых лекарств от COVID-19 недавно стал предметом пристального изучения, 5 с гидроксихлорохином вызывает наибольшие споры. Еще одно различие между десятью лучшими списками этих двух методов заключается в разнообразии включенных мишеней для лекарств. В первую десятку результатов стыковки вошли семь ингибиторов протеазы ВГС или ВИЧ. В хит-лист с приоритетом фармакофоров входят лекарства с семью различными целевыми классами.
В результате нашего виртуального скрининга на основе фармакофоров был составлен приоритетный список, включающий несколько новых потенциальных лекарств от COVID-19, которые не были идентифицированы в нашей предыдущей стыковочной работе. С помощью этого подхода мы демонстрируем использование in silico мутагенез со сканированием аланина как полезный метод уточнения модели фармакофоров. Мы также ввели требование о наличии определенных функций для подгонки во время процесса отбора. Результаты этих двух исследований нельзя напрямую сравнивать - не столько из-за различий в основных алгоритмах, сколько из-за реализации различных поддерживающих стратегий.
Краткое сравнение результатов двух методов показало небольшое совпадение в выводах, на которых следует сосредоточить внимание. Можно сказать, что общность ритонавира, выявленная обоими методами, дает доказательства, подтверждающие выбор этого кандидата для дальнейшего изучения. Предыдущие исследования показали, что использование консенсуса функций стыковки белков и лигандов улучшает идентификацию предполагаемых лекарств-кандидатов. 6 По этой причине исследователи могут использовать уникальные соединения с лучшими показателями из каждого метода для определения приоритетных соединений для экспериментального тестирования.
В заключение, виртуальный скрининг на основе фармакофоров обеспечивает дополнительный и дополнительный метод стыковки, способствуя достижению консенсуса и большей уверенности в выборе кандидатов для экспериментальной проверки. Помимо срочности предоставления лекарственного препарата-кандидата для перепрофилирования, этот метод, основанный на фармакофорах, может также определять лиганды, которые более разнообразны, для последующей оптимизации потенциальных клиентов.
Биопрепараты
- Никотиновый пластырь
- Виртуальный инвентарь и 3D-печать:необходимость безопасности
- С# для цикла
- C для цикла
- Нановолокна и нити для улучшенной доставки лекарств
- Дизайн генеративной терапии
- Переделка наркотиков
- Universal Robots запускает крупнейшую в мире виртуальную конференцию для роботов для совместной работы
- Производство печатных плат для 5G
- Микророботы, напечатанные на 3D-принтере, обещают доставку лекарств



