Дефосфорация сталей
Дефосфорация стали
Влияние фосфора (P) на свойства сталей обобщено в таблице 1. Видно, что фосфор оказывает как положительное, так и отрицательное влияние на свойства стали.
| Таблица 1 Влияние фосфора на свойства сталей | ||
| <тд 197"> <тд 268"> | ||
| Серийный № | Свойство | Влияние фосфора |
| <тд 197"> <тд 268"> | ||
| 1 | Сила | Сильный положительный (укрепляет феррит) |
| 2 | Прокаливаемость | Положительно |
| 3 | Пластичность | Сильный минус |
| 4 | Гальванический отжиг | Может повысить стойкость к порошкообразию |
| 5 | Фосфатируемость | Положительно |
| 6 | Эмаль | <тд 268">|
| а. Чистка рыбы | Отрицательный | |
| б. Травление | Положительно | |
| 7 | Свариваемость | Безвреден при содержании менее 0,1 % |
| 8 | Потери сердечника в пластинах двигателя | Сильный минус |
| 9 | Вязкость на излом | Сильный минус |
Стали с низким содержанием фосфора необходимы для применений, требующих высокой пластичности, таких как тонкие листы, сталь глубокой вытяжки, трубопроводы и т. д. Раньше контроль содержания фосфора не считался большой проблемой при производстве стали, поскольку железные руды с низким Содержание фосфора было легко и дешево доступно. Однако в недавнем прошлом из-за высоких цен на железную руду использовались более дешевые железные руды из источников, которые обычно имеют более высокое содержание фосфора, и это сделало контроль фосфора важным видом деятельности при производстве стали.
В дополнение к фосфору из железных руд, фосфор также поступает в жидкую сталь из-за рециркуляции шлака кислородно-конвертерного конвертера. Переработка конвертерного шлака осуществляется через аглофабрику или непосредственно в доменную печь, чтобы извлечь из шлака железо и известь и свести к минимуму проблемы, связанные с утилизацией шлака. Агломерат или конвертерный шлак, подаваемые в доменную печь, неизбежно увеличивают содержание фосфора в чугуне и, следовательно, нагрузку фосфора на процесс производства стали.
На интегрированных сталеплавильных заводах удаление фосфора обычно происходит во время основного процесса производства стали, обычно в кислородном конвертере. Чтобы удовлетворить новые требования к контролю фосфора, необходимо улучшить понимание термодинамики и кинетики реакции распределения фосфора между шлаком и расплавами металла в процессе производства стали.
Дефосфорация сталей стала очень важным металлургическим методом в процессе производства стали для производства высококачественных сталей. Поскольку содержание фосфора контролируется реакциями в кислородном конвертере, метод двойного шлака обычно применяется для получения раскисленных сталей с низким содержанием фосфора. Однако этот прием сопровождается увеличением наработки и снижением выхода стали. Помимо проблем с производительностью при использовании этого метода, во время работы конвертерного конвертера также образуется огромное количество шлака конвертера.
Фосфор также можно удалить в процессе рафинирования стали. Фактически более 90 % фосфора, вводимого в расплав, может быть удалено в кислородном конвертере. Очищающая способность шлака зависит от многих переменных, таких как состав шлака и металла, температура, время и интенсивность перемешивания шлака/металла.
Содержание P в жидкой стали при выпуске, раскислении, продувке инертным газом и разливке может увеличиваться постепенно за счет введения его с раскислителями и восстановления из шлака. Эту возможность необходимо учитывать для поддержания условий дефосфорации в жидкой стали. В результате реакций между сталью, шлаком и раскислителями равновесие фосфора смещается в сторону увеличения содержания фосфора в стали, несмотря на значительное снижение температуры. В этом случае дефосфорация существенно зависит от соотношения массы стали и шлака. Роль этих факторов можно вывести из следующего уравнения баланса фосфора.
(Содержание P в ковшовом шлаке) + (Содержание P в ковшовой стали) =(Содержание P в выпускаемом металле) + (Содержание P в шлаке, захваченном сталью в ковше) + (P из раскислителей).
Реакция фосфора и термодинамическое равновесие
Первые комплексные исследования дефосфорации были проведены в 1940-х годах. Эти исследования показали, что FeO и CaO являются необходимыми составляющими шлака для дефосфорации стали. Эти исследования также показали, что реакция дефосфорации является экзотермической и что способность шлака к дефосфорации снижается с температурой. Исследования также показали, что дефосфорация усиливается за счет снижения температуры и увеличения содержания FeO и основности шлака.
Было разработано множество корреляций для прогнозирования коэффициента распределения фосфора в зависимости от состава металла и шлака, а также от температуры. Однако все еще существуют разногласия в лабораторных данных и равновесном распределении фосфора, которое можно предсказать.
Хотя количественная оценка равновесия фосфора чрезвычайно важна, многие сталеплавильные печи не работают в равновесии, обычно из-за образования жидкого шлака, кинетики и временных ограничений. Таким образом, важно знать, насколько близко к равновесию работают сталеплавильные печи, чтобы предложить оптимальный состав шлака, способствующий дефосфорации.
В ходе ранних исследований было отмечено, что условия перемешивания и состав шлака являются двумя ключевыми переменными, обеспечивающими оптимальное удаление фосфора. Кроме того, чрезмерное насыщение шлака CaO и MgO, по-видимому, никоим образом не способствует процессу.
В ходе этих исследований было обнаружено, что динамические межфазные явления на границе металл-шлак, вероятно, играют значительную роль в кинетическом поведении системы из-за обмена поверхностно-активными элементами, такими как кислород (O2), который резко снижает межфазное натяжение и вызвать самопроизвольное эмульгирование. Было также установлено, что P не играют роли в самопроизвольном эмульгировании и быстро удаляются до наступления динамических межфазных явлений. Эмульгирование может быть вызвано раскислением металла после того, как произошло удаление Р, и металл по неизвестной причине стал перенасыщенным О2. Расчетная площадь поверхности быстро увеличивается более чем на порядок в начальный и промежуточный периоды реакции. Капля металла распадается на сотни мелких капель, эффективно эмульгируя металл в шлак. Со временем площадь поверхности уменьшается, и капли металла сливаются. Аналогичные результаты наблюдались для окисляемой капли железа (Fe).
В 1950-х годах было высказано предположение, что удовлетворительно рассматривать реакцию в ее простейшей форме, как показано ниже.
2P + 5O =P2O5 (жидкость)
Свободная энергия, связанная с реакцией, оценивалась с использованием оценки энтропии плавления P2O5, так что
Дельта G =– 740375+535,365T Дж/моль
При Т более 1382 град К дельта G? становится положительным, что приводит к разложению P2O5 на P и O. Таким образом, удаление P требует восстановления P2O5. Коэффициент активности P2O5 увеличивается за счет кремнезема (SiO2) и уменьшается за счет основных оксидов, таких как CaO и MgO.
В течение 1980-х годов были проведены дальнейшие исследования распределения фосфора в различных шлаковых системах. Эти исследования показали, что коэффициент распределения Р увеличивается с увеличением содержания СаО в шлаке и с понижением температуры. Также видно, что влияние CaF2 на дефосфорацию такое же, как и у CaO, без повышения температуры плавления шлака. Также изучалось влияние оксида бария (BaO) и оксида натрия (Na2O) на распределение P. Эти исследования пришли к выводу, что эквивалентность CaO для Na2O и BaO составляет 1,2 и 0,9 в весовых процентах соответственно.
Распределение фосфора в различных шлаковых системах изучалось много раз, и было установлено несколько корреляций. Различные выводы этих исследований приведены ниже.
- Содержание CaO, MgO, SiO2, P2O5, FeO и MnO в шлаке влияет на распределение фосфора.
- Жидкий шлак полностью ионизирован, и фосфор в шлаке существует в виде ионов фосфата.
- Log распределения P увеличивается на 2,5 log % FeO, как и предсказывает термодинамика, и увеличение основности шлака также увеличивает коэффициент разделения.
- Увеличение основности шлака (CaO/SiO2) до 2,0 оказывает сильное повышающее влияние на разделение фосфора. Однако это увеличение гораздо менее выражено при основности выше 2,5.
- Коэффициент распределения P первоначально увеличивается с увеличением содержания FeO, но затем уменьшается после достижения определенного уровня. Этот уровень зависит от основности шлака и температуры. Эти выводы справедливы и для содержания FeO в шлаке от 15 % до 25 %. Более конкретно, доля P не зависит от содержания FeO выше 19 %. Кроме того, распределение P оказывается ниже с увеличением содержания MgO при температурах 1600°C и 1650°C.
- Для шлаков, содержащих от 0,2 % до 1,0 % P2O5, логарифм коэффициента активности P2O5 является линейной функцией содержания CaO и MgO и не зависит от температуры. Для шлака, содержащего P2O5 более 1 %, логарифм коэффициента активности P2O5 также является линейной функцией CaO, но также зависит от температуры.
- Увеличение концентрации Ca2+, Fe2+ и Mg2+ приводит к снижению коэффициента активности P2O5, тогда как (SiO4)4- имеет противоположный эффект.
- Полимеризация P не происходит в широких масштабах в шлаках, которые обычно используются при производстве стали.
Также были опробованы другие подходы к разделению модели P между сталью и шлаком. В 2011 году была разработана исчерпывающая термодинамическая модель, основанная на теории сосуществования ионов и молекул (IMCT), для прогнозирования соотношения распределения фосфора между шлаками CaO-SiO2-FeO-Fe2O3-MnO-Al2O3-P2O5 и жидкой сталью. ММКИ предполагает, что шлак состоит из простых ионов, таких как Ca2+, Fe2+, Mg2+ и O2-; простые молекулы P2O5, SiO2 и Al2O3; силикаты, алюминаты и многие другие в виде сложных молекул. Все ионные частицы участвуют в реакциях образования сложных молекул из ионных пар (Me2+ и O2-) и простых молекул и находятся в термодинамическом равновесии. Принимаемые во внимание возможные молекулы фосфора:P2O5, 3FeO.P2O5, 4FeO.P2O5, 2CaO.P2O5, 3CaO.P2O5, 4CaO.P2O5, 2MgO.P2O5, 3MgO.P2O5 и 3MnO.P2O5. Было обнаружено, что вклад 3CaO.P2O5 и 4CaO.P2O5 в измеренное распределение фосфора составляет 96 % и 4 % соответственно.
До сих пор обсуждалось равновесие Р между жидкой сталью и жидким шлаком. Однако из-за многокомпонентной природы сталеплавильных шлаков нередки случаи, когда твердые фазы находятся в равновесии с жидким шлаком. Существенные исследования были проведены на конкретных твердых фазах, которые обычно встречаются в сталеплавильных шлаках. В частности, исследования были сосредоточены на шлаках, содержащих частицы 2CaO.SiO2 и CaO. Эти твердые фазы обычно присутствуют в сталеплавильных шлаках кислородного конвертера и могут играть роль в дефосфорации, поскольку в них могут растворяться фосфаты.
Очистка фосфора в кислородном конвертере
Хороший сталеплавильщик также хорошо производит шлак» — это популярное высказывание среди сталеплавильного персонала, очень актуальное в контексте конвертерного процесса. Надлежащий контроль над образованием и составом шлака обеспечивает оптимальное рафинирование и сводит к минимуму риск повторной продувки O2 или внесения дополнительных добавок в конце плавки. В начале удара пику держат высоко над поверхностью металла. В течение первых 3-4 минут Si (кремний) из металла быстро окисляется вместе с Fe, образуя шлак, богатый FeO и SiO2. В конвертер добавляется значительное количество извести и доломитовой извести. По мере продолжения продувки твердая известь непрерывно растворяется в жидком шлаке, увеличивая массу и основность шлака. По мере продолжения обезуглероживания шлак начинает пениться, а образующийся газ CO снижает содержание FeO в шлаке. Ближе к концу продувки скорость обезуглероживания снижается, и окисление Fe снова становится значительным. На протяжении всей продувки температура металла неуклонно повышается от 1350°С до 1650°С, а температура шлака обычно на 50°С выше, чем температура металла в конце продувки.
Механизм растворения извести очень важен для кислородного конвертера и удаления фосфора. Достижение быстрого растворения извести во время кислородно-конвертерного процесса дает хорошие возможности для повышения производительности, сокращения времени и стоимости процесса. Механизм растворения извести зависит от состава шлака и уровня насыщения двухкальциевого силиката (2CaO.SiO2). Исходный шлак обогащен FeO и SiO2. Когда известь добавляется впервые и начинает растворяться, вокруг твердых частиц образуется слой 2CaO.SiO2, который замедляет скорость растворения извести. Этот твердый слой может разрушиться, и шлак может проникнуть в поры частиц извести и продолжить растворение. Проникновение шлака зависит от вязкости и размера пор твердых частиц.
Поскольку в конвертерном процессе часто присутствуют твердые оксидные фазы, сосуществующие со шлаком, важно понимать, как твердые частицы могут влиять на удаление фосфора. В нескольких исследованиях рассматривалась растворимость P в различных твердых частицах, таких как CaO, 2CaO.SiO2 и 3CaO.SiO2. Ниже приведены некоторые выводы этих исследований.
- Распределение фосфора между частицами 2CaO.SiO2 и шлаком колеблется от 2 до 70 по мере увеличения содержания FetO и основности в шлаке. Температурная зависимость распределения P оказывается очень слабой, и изолированные частицы 2CaO.SiO2 демонстрируют полное равномерное превращение в 2CaO.SiO2-3CaO.P2O5 в течение 5 секунд.
- При контакте со шлаком CaO-FetO-SiO2-P2O5 частица CaO быстро инкапсулируется слоем 2CaO.SiO2-3CaO.P2O5 и шлака CaO-FetO без образования P2O5 между частицей CaO и 2CaO. .SiO2-3CaO.P2O5 твердый раствор.
- Существует два возможных пути переноса фосфора из шлака в 2CaO.SiO2. В первом случае 2CaO.SiO2-3CaO.P2O5 будет осаждаться из жидкого шлака после переноса P из металлической фазы. Во втором возможном пути частицы 2CaO.SiO2 уже присутствуют в шлаке до переноса P из металла. Затем P диффундирует в осажденную свободную от P частицу 2CaO.SiO2. Было обнаружено, что скорость переноса P путем осаждения намного выше, чем путем диффузии. Это указывает на тот факт, что наличие ранее существовавших частиц 2SiO2.SiO2 не обязательно улучшает удаление фосфора.
Во время продувки в кислородном конвертере создается очень динамичная среда. Когда струя O2 попадает на поверхность шлака, а затем и жидкого металла, она создает трехфазную эмульсию газ-шлак-металл, что значительно увеличивает общую площадь поверхности раздела, доступную для протекания нескольких химических реакций между фазами. Капли металла непрерывно выбрасываются из металлической ванны в шлакогазовую смесь, где они могут вступать в реакцию в течение заданного времени. Образование этих металлических капель очень важно для кинетики внутри кислородного конвертера.
Скорость рафинирования в конвертерном процессе зависит не только от химической кинетики, но и от времени пребывания данной капли металла в шлаке. Расчетное время пребывания капли металла, выбрасываемой из массы металла и движущейся по баллистической траектории через шлак, составляет менее 1 секунды, что слишком мало для того, чтобы данная капля могла реагировать в значительной степени. Однако при изучении поведения капель Fe-C в шлаке было замечено, что образование газового «гало» во время обезуглероживания удерживает металлическую каплю во взвешенном состоянии в шлаке от 50 до 200 секунд. Основываясь на этих наблюдениях, модель модифицируется, чтобы учесть влияние обезуглероживания на кажущуюся плотность капли металла, и она способна прогнозировать время пребывания консистенции.
В опубликованном в 2011 году отчете под названием «Имфос:улучшение рафинирования фосфора» среди прочего рассматривались профили соотношения металл/шлак, распределение капель металла по размерам в эмульсии шлак/металл, распределение фосфора на границе шлак-металл и растворение извести. В отчете определены пять профилей удаления фосфора, как показано на рис. 1. Эти профили:(i) почти постоянный профиль фосфора, (ii) профиль реверсии фосфора, (iii) профиль высокого удаления фосфора, (iv) профиль реверсии и замедления фосфора и (v) реверсия с профилем быстрого удаления фосфора. Для каждого из этих профилей исследовано количество металла и его химический состав для эмульсии шлак/металл и для объемной ванны. Было обнаружено, что содержание P в каплях металла в шлаке обычно ниже или равно содержанию в массе ванны, что указывает на тот факт, что удаление P обусловлено дефосфорацией капель металла, присутствующих в эмульсии шлак/металл, а не в объемная ванна. Одно интересное наблюдение в отчете заключается в том, что на ранних стадиях продувки удаление фосфора из эмульгированных капель происходило намного быстрее, чем обезуглероживание.
Установлено, что капли металла крайне бедны фосфором (намного меньше 100 частей на миллион), в то время как содержание углерода в ванне значительно превышает 1 %. Это потенциально связано с газовым «ореолом» и эмульгированием, которые могут увеличить время пребывания капель на ранних стадиях продувки, давая им достаточно времени для реакции с присутствующим сильно окисляющим шлаком, что приводит к быстрому удалению фосфора, если размер капель подходит. Поскольку удаление фосфора тесно связано с образованием капель металла, существует идеальная высота фурмы на каждом этапе продувки, чтобы максимизировать образование капель и создать хорошую эмульсию шлак/металл/газ. Замечено, что по мере уменьшения высоты фурмы образуется меньше капель металла.
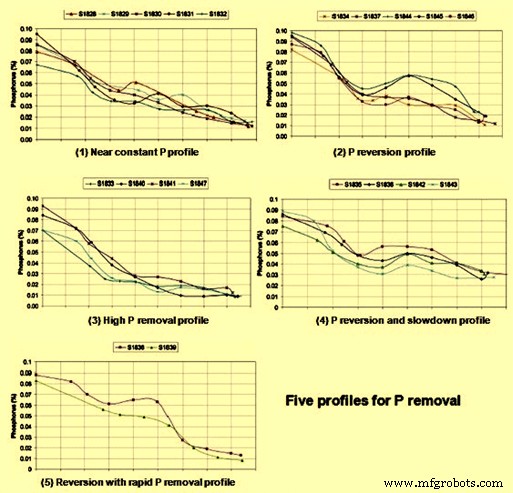
Рис. 1. Различные профили удаления P
Механизм дефосфорации в конвертерном процессе можно резюмировать следующим образом.
- В начале продувки, когда кислородная фурма держится высоко, достигается хороший выброс капель и быстрое удаление фосфора.
- По мере того, как продувка продолжается и начинается процесс обезуглероживания с образованием газообразного CO, FeO в шлаке восстанавливается, и шлак может стать недостаточно окисляемым. Это может привести к возвращению фосфора в расплав по мере того, как капли рефосфорируются и возвращаются в объем металла. Это особенно важно, если растворение извести не является оптимальным.
- Ближе к концу продувки обезуглероживание замедляется, а содержание FeO в шлаке увеличивается, снова благоприятствуя дефосфорации. Однако этого может быть недостаточно, чтобы компенсировать возможную реверсию, произошедшую ранее.
- Оптимальные результаты могут быть достигнуты путем тщательного контроля содержания FeO и CaO в шлаке. Добавление железной руды может помочь поддерживать идеальное содержание FeO для продолжения окисления фосфора параллельно с обезуглероживанием.
Кинетика удаления фосфора
Хотя равновесие фосфора широко изучено, кинетика удаления фосфора до такой степени не изучена. Однако те же принципы применимы и к другим высокотемпературным металлургическим реакциям. Когда P, растворенный в Fe, контактирует со шлаком, во время реакции дефосфорации происходит несколько стадий, которые дают основную иллюстрацию этого явления. Эти шаги заключаются в следующем.
- Массоперенос в металлической фазе [P] и [O] по направлению к границе раздела шлак-металл
- Массоперенос в шлаковой фазе (O2-) к границе раздела шлак-металл
- Химическая реакция на границе шлак-металл с образованием (PO4)3-
- Массоперенос в шлаковой фазе (PO4)3- вдали от поверхности реакции
Поскольку дефосфорация происходит при высоких температурах, разумно предположить, что химическая реакция на границе раздела протекает быстро и находится в равновесии. Таким образом, возможными этапами, ограничивающими скорость, являются массоперенос в металлической или шлаковой фазах или в обеих, если предполагается, что в шлаке нет твердых фаз, способных поглощать фосфор.
Одно из исследований кинетики дефосфорации чугуна Fe-C(sat)-P окислительными шлаками показывает, что одной из основных проблем при дефосфорации жидкого металла является правильное количественное определение движущей силы реакции из-за отсутствия -равновесный потенциал O2 на границе шлак/металл. Эта неравновесность возникает из-за обезуглероживания жидкого металла, что снижает потенциал O2 в металле. В таких случаях шлак имеет высокий потенциал O2, в то время как металл имеет низкий потенциал O2. В ходе исследования было обнаружено, что реакция дефосфорации следует кинетической скорости первого порядка по отношению к концентрации P в металле, а более высокое содержание FeO увеличивает коэффициент массопереноса шлака из-за снижения вязкости, хотя FeO также может влиять либо положительно или отрицательно движущая сила реакции. Исследование также показало, что массоперенос в шлаковой фазе является стадией, ограничивающей скорость дефосфорации металла.
Совсем недавно в другом исследовании использовался математический подход для количественной оценки массообмена фосфора между металлом и шлаком. Исследование показало, что кажущийся коэффициент массопереноса, по-видимому, является функцией межфазного натяжения, на которое влияет поток массы поверхностно-активного элемента, такого как O2, особенно в условиях быстрого массопереноса. Изменения параметра массопереноса связаны с динамическим межфазным явлением, которое усиливает массоперенос в периоды высокого потока О2 через границу раздела. Предполагается, что этот высокий поток O2 снижает межфазное натяжение во время реакции, что приводит к увеличению межфазной поверхности или коэффициента массопереноса, или того и другого.
Несколько исследований показали, что спонтанное эмульгирование может происходить в периоды интенсивного массопереноса поверхностно-активных элементов из-за очень выраженного снижения межфазного натяжения между двумя несмешивающимися жидкостями. Кроме того, для равновесного межфазного натяжения содержание O2 и S (серы) в металле играет существенную роль в наблюдаемом равновесном натяжении. Добавление CaF2 и Na2O повышает межфазное натяжение, а добавление MnO имеет тенденцию его снижать. Одно из исследований показало, что когда поток О2 становится больше примерно 0,1 г атом/кв.м·с, межфазное натяжение приближается к значению, близкому к нулю. Когда поток O2 становится ниже 0,01 г атом/кв.м·сек, межфазное натяжение быстро увеличивается до значения, близкого к равновесному натяжению.
Кинетика дефосфорации изучена гораздо меньше, чем равновесие фосфора между металлом и шлаком. Существуют разногласия по поводу того, влияет ли массоперенос в металле, шлаке или в обоих случаях на скорость реакции. Из-за характера реакции явление динамической границы раздела, по-видимому, играет значительную роль в общей скорости реакции. Самопроизвольное эмульгирование, по-видимому, происходит, когда происходит быстрый массоперенос O2 на границе раздела систем металл-шлак. Это приводит к существенному снижению межфазного натяжения, что увеличивает площадь реакции и ее общую скорость. Однако прямой расчет изменений площади реакции вследствие самопроизвольного эмульгирования остается очень сложным.
Производственный процесс
- Металлические материалы для 3D-печати
- Инконель против нержавеющей стали
- Стандартные марки инструментальной стали
- Включения, разработка включений и чистые стали
- Грануляция доменного шлака в литейном цехе
- Высокоглиноземистый шлак и доменная печь
- Азот в сталях
- Аргонная промывка сталей
- Что такое шлак?
- Понимание электрошлаковой сварки (ESW)



