Разработка общей стратегии производства углеродистых нанокомпозитов из благородных металлов с фототермическими свойствами
Аннотация
Это исследование демонстрирует простой гидротермальный метод, который может быть обобщен для управляемого синтеза благородных металлических углеродистых наноструктур (например, Au @ C, Ag @ C) в мягких условиях (180–200 ° C), что также обеспечивает уникальный подход для изготовления полых углеродистые структуры путем удаления ядер (например, серебра) с помощью процесса окислительно-восстановительного травления. Микроструктура и состав полученных наночастиц были охарактеризованы с использованием различных микроскопических и спектроскопических методов. Бромид цетилтриметиламмония (CTAB), выступающий в качестве поверхностно-активного вещества в реакционной системе, играет ключевую роль в формировании нанокабелей Ag @ C, Au @ C и соответствующих им полых углеродных нанотрубок. Подробно обсужден механизм динамического роста и формирования углеродных наноструктур. И, наконец, были исследованы фототермические свойства нанокомпозитов Au @ C, индуцированные лазерным излучением. Результаты могут быть полезны для проектирования и создания наноструктур из углеродистых металлов или оксидов металлов с потенциальным применением в областях электрохимического катализа, накопления энергии, адсорбентов и биомедицины.
Графический аннотация
Это исследование демонстрирует простой гидротермальный синтез углеродсодержащих нанокомпозитов благородных металлов (например, Au @ C) с помощью простых процедур в мягких условиях, который может быть расширен как общий метод получения различных углеродных наночастиц ядро-оболочка. Углеродистые наноструктуры Au @ C демонстрируют интересные свойства в УФ-видимом диапазоне в зависимости от толщины оболочки.
Основные моменты
-
Разработать простой гидротермальный метод создания наноструктур из благородного металла @ C ядро-оболочка
-
Образовавшиеся ядра Ag или Au хорошо кристаллизованы, но углеродистая оболочка аморфна.
-
Глюкоза играет множественную роль в качестве восстановителя ионов металлов, модификатора формы и защиты поверхности
-
Низкотемпературная (60–100 ° C) гидротермальная реакция травления ядро-оболочка Ag @ C с получением полой углеродистой оболочки
-
Стержневые нанокомпозиты Au @ C демонстрируют фототермический эффект, потенциал для биомедицинского применения
Введение
Углеродные материалы становятся все более важными в материаловедении и технологиях. В прошлом был исследован ряд углеродных частиц, таких как углеродные нанотрубки, углеродные сферы / точки [1,2,3] и оксид графена (GO) [4, 5]. Среди них углеродные наноструктуры проявляют некоторые уникальные свойства, такие как хорошая стабильность (<200 ° C), пористые стенки трубок, превосходные смазывающие свойства, легко диспергируются в воде и биосовместимость, а также легко гибридизуются с металлами (например, Au, Ag ) и / или оксидов металлов для создания гибридных функциональных наноструктур [6,7,8,9,10,11,12,13].
В частности, нанокомпозиты на основе углеродистых металлов привлекли больше внимания из-за их превосходной биосовместимости в медицинских приложениях. Для получения таких углеродистых частиц или их металлических гибридных структур был разработан ряд методов, например гидротермальный метод с использованием сахара или крахмала в качестве исходного материала [14], например одностадийный гидротермальный синтез углеродсодержащих серебряных нанокабелей и нанотрубок. после травления серебряной сердцевины s [15], шаблонный подход для изготовления коаксиальных нанокабелей Ag / Cu @ поливиниловый спирт (ПВС), наноструктур теллура (Te) @PVA [16], а также пористых мембранных шаблонов и твердых позитивных шаблонов. [17,18,19,20] для синтеза углеродных наноструктур. Однако удаление твердого шаблона (ов) может привести к проблемам при последующей обработке (химическое травление или высокотемпературное обжигание), например, разрушению или разрушению структуры [14,15,16,17,18,19,20,21 , 22]. Кроме того, мало что было описано для выяснения механизма образования / эволюции углеродистых наноструктур благородных металлов, достигаемых в указанных условиях.
Фототермическая терапия была разработана, потому что она меньше повреждает здоровые ткани за счет генерации локализованного тепла, особенно на ранних стадиях метастазирования или когда опухоль находится в начальной стадии. Золотые наночастицы (ЗНЧ) - один из отличных вариантов для этого подхода. Последние достижения в многофункциональной конструкции ЗНЧ позволяют генерировать локализованное тепло вблизи раковых тканей и дополнительно позволяют доставлять множество желаемых лекарств контролируемым и целевым образом. ЗНЧ обладают множеством преимуществ, которые делают их пригодными для фототермического лечения опухолей или рака, поскольку они могут доставляться в локальную область опухоли, сводя к минимуму неспецифическое распространение, активируясь с помощью лазерного света в ближней инфракрасной области (БИК), создавая способность проникать внутрь. глубоко в биологические ткани и модулированы для создания многогранной фототермической терапии рака [23,24,25].
Здесь мы демонстрируем простой, но эффективный метод синтеза для создания углеродистых наноструктур Au @ C или Ag @ C в мягких условиях (180–200 ° C). Интересно, что ядра из серебра, а не из золота, могут быть вытравлены или удалены из углеродистой структуры путем низкотемпературного травления (60 ° C в течение десятков часов) без необходимости какой-либо высокотемпературной обработки. Будет охарактеризована микроструктура полученных нанокомпозитов, и будут поняты возможные механизмы образования. Фототермические свойства наноструктур Au @ C в качестве примера будут изучены со ссылкой на недавние исследования [23,24,25]. Это исследование может предложить простую, но эффективную стратегию приготовления углеродистых металлических нанокомпозитов с потенциальным применением в материаловедении, катализе и биохимии.
Экспериментальный метод
Химические вещества
Следующие химические вещества были закуплены у Sigma-Aldrich и использованы без дополнительной очистки в том виде, в котором они были получены:нитрат серебра (> 99%), d -глюкоза (99%), бромид цетилтриметиламмония (CTAB,> 98%) и тригидрат хлорида золота (III) (HAuCl 4 · 3H 2 О> 99,9%). Всю стеклянную посуду промывали свежей царской водкой, тщательно промывали несколько раз дистиллированной водой и / или этанолом и сушили перед использованием.
Синтез углеродистых наноструктур Ag @ C и Au @ C
Обычно процедура синтеза включает несколько этапов. Через tep 1, 2,0 мл 0,01 М AgNO 3 и 6,0 мл 0,01 М раствора глюкозы добавляли в стеклянный стакан на 50 мл, содержащий 10 мл 0,12 М раствора ЦТАБ, затем перемешивали и перемешивали, чтобы убедиться в гомогенности. у. Через tep 2, общий объем раствора смеси фиксировали на уровне 35 мл с использованием дистиллированной воды при перемешивании в течение 10 мин для гомогенности. Цвет раствора смеси постепенно становился светло-желтым, вероятно, из-за образования осадка AgBr в присутствии ЦТАБ. И в На этапе 3 смешанный раствор переносили в автоклав из нержавеющей стали с тефлоновым вкладышем емкостью 50 мл и нагревали в печи при 180 °. C на пару часов.
Подобно процедуры приготовления наночастиц Au @ C, замена AgNO 3 Автор:HAuCl 4 · 3H 2 Решение O было проведено в данной работе. Что касается получения углеродистых наностержней Au @ C, сначала были синтезированы наностержни Au на основе нашей предыдущей работы [26,27, - 28], в котором CTAB играет ключевую роль в управлении формирование наностержней Au. Наностержни Au диспергировали в растворе глюкозы для дальнейшей гидротермальной реакции при 180 ° C в течение 6 - 24 ч.
Травление полой углеродистой структуры
Полые углеродные наноструктуры были изготовлены путем травления ядер Ag из нанокомпозитов Ag @ C, выдерживая тот же реакционный раствор при температуре 60 ° C. C в течение десятков часов, в то время как это невозможно для травления ядра Au из Au @ C. В процессе динамической реакции ядра серебра были удалены , и поэтому , образовались полые углеродистые структуры. Полученные образцы промывали дистиллированной водой три раз для дальнейшей характеристики.
Характеристика
Процессы формирования, роста и травления предварительно приготовленных углеродных наноструктур Au @ C и Ag @ C были охарактеризованы с использованием различных методов, включая просвечивающую электронную микроскопию (ПЭМ, JEOL-1400), сканирующую электронную микроскопию (СЭМ, FEI Nova NanoSEM 230). FESEM), ПЭМ высокого разрешения (HRTEM) с использованием автоэмиссионного пистолета Phillips CM200. ПЭМ, работающий при 200 кВ, УФ-видимые спектры с помощью спектрофотометра Cary 5000 UV-Vis NIR с кварцевой ячейкой 1 см, инфракрасное излучение с преобразованием Фурье (FT-IR ) спектр с помощью микроскопа Perkin Elmer Spotlight 400 FT-IR (650–4000 см −1 ), Рамановской спектроскопии (Рамановский спектрометр Renishaw RM1000, длина волны возбуждения 514 нм) и многоцелевой рентгеновской дифракционной системы Philips X’pert с использованием Cu-K α ( λ =0,15406 нм) излучения при 40 кВ и 100 мА, в диапазоне измерения 10–80 ° с шагом сканирования 0,02 ° / с.
Фототермические измерения
Термопара использовалась для измерения фототермической температуры на основе предыдущих отчетов [23,24,25, 29,30,31]. Для измерения термопары использовали Delta OHM HD2128.2 T. Источником света является лазер мощностью 0,17 Вт / см 2 . . Чтобы быть более точным и надежным, температуры были измерены ИК-камерой Cedip Titanium 560 M с разрешением изображения 640 × 512 пикселей при частоте кадров до 100 Гц. Пиксели имеют квадратную форму размером 24 × 24 мкм. Чип устройства с зарядовой связью (ПЗС) в камере чувствителен к длине волны 3,6–5,1 мкм, поэтому на изображениях можно увидеть только тепловое излучение жидкости, поскольку длина волны лазера 0,8 мкм невидима для сенсора камеры. . Диапазон температур составляет 0–60 ° C. Для фототермических измерений мы выбрали углеродистые структуры Au @ C (наностержни Au с соотношением сторон ~ 3,7) в качестве примера из-за высокой стабильности и нетоксичности Au в биосистемах.
Результаты и обсуждение
Микроструктура углеродистых наноструктур Ag @ C
Морфология и состав полученных наночастиц были охарактеризованы с использованием методов ПЭМ и СЭМ. На рис. 1а показаны ПЭМ-изображения предварительно приготовленных нанокабелей Ag @ C вместе со вставкой увеличенного изображения, на которой диаметр кабелей оценивается как 30–50 нм, а ширина сердцевины из Ag - 10–20 нм. Это также подтверждается SEM, как показано на рис. 1b, где нанокабели Ag @ C не прямые, а изогнутые. Здесь было обнаружено, что были сформированы только одномерные нанокабели Ag @ C, но углеродистые сферы, что указывает на то, что процесс самозарождения и роста за счет карбонизации глюкозы был значительно подавлен, а процесс нанесения покрытия на ядро Ag является доминирующим в наших условиях. сообщенные условия.

Наноструктуры Ag @ C: a ТЕА и б СЭМ-изображения углеродистых нанокабелей. c , d ПЭМ для углеродистых нанотрубок
Впоследствии нанокабели Ag @ C можно было травить, выдерживая тот же реакционный раствор при 60 ° C в течение 24 часов, без добавления травителей, и затем были получены полые углеродистые трубки, как показано на рис. 1c, d с разные увеличения. Очевидно, что сердцевина из серебра может быть удалена или вытравлена из нанокабелей (рис. 1а) с помощью разработанной гидротермальной реакции. Для сравнения, нанотрубки немного сжаты, но не повреждены или сломаны, что позволяет предположить, что углеродистые оболочки относительно стабильны по структуре в указанных условиях.
Чтобы лучше понять процессы образования и роста нанокомпозитов Ag @ C, для отслеживания динамической реакции было взято разное время реакции (рис. 2). При увеличении времени с 1 ч (а) до 3 ч (б), 6 ч (в), 12 ч (г) и 24 ч (д) при температуре реакции 180 ° C образовался углеродистый Ag @ C. , в котором Ag постепенно образовывался от точек (a) до коротких стержней (b – d) и, наконец, до стержней / проволок (e). Наностержни серебра в наноструктурах Ag @ C хорошо кристаллизованы, что подтверждается изображениями ПЭМВР на рис. 2f и g, а также электронной дифракционной картиной, вставленной на рис. 2g. Кристаллические плоскости Ag {111} с пространством решетки 0,238 нм четко просматривались с помощью изображения ПЭМВР (рис. 2g).

Процесс формирования структуры ядро-оболочка Ag @ C со временем: a 1 ч, б 3 ч., c 6 ч., д 12 ч. И д 24 ч; е Шаблон ED с индексированными плоскостями и g ПЭМВР стержней Ag из нанокомпозитов Ag @ C с пространством решетки 0,238 нм, отнесенных к плоскостям {111}
Согласно текущим экспериментам, для объяснения образования Ag @ C можно использовать два возможных механизма. Сначала осадок AgBr образовывался Br - ионы (из CTAB), реагирующие с Ag + ионы (из AgNO 3 ) из-за очень маленького K sp (5,0 × 10 −13 ) при комнатной температуре в водном растворе, в то время как AgBr не является термически стабильным и, таким образом, образует металлический Ag при термообработке, действуя как центр зародышеобразования для образования и роста углеродистой оболочки. CTAB также играет другую роль в модификации поверхности, способствуя формированию ориентации серебряных наностержней или нанопроволок, поскольку молекулы CTAB преимущественно адсорбируются на длинноосных кристаллических плоскостях растущих частиц Ag [32]. Во-вторых, глюкоза действовала как восстанавливающий агент, снижающий содержание свободного Ag + ионы к Ag 0 атомы при высокой температуре (> 140 ° C) [33] из-за его богатых -OH и альдегидных групп. Затем вновь образованные ядра Ag действовали как центр зародышеобразования для адсорбции молекул глюкозы и впоследствии полимеризовались в виде углеродной оболочки на основе серебра [34,35,36,37].
В качестве дополнительного подтверждения, метод XRD был использован для отслеживания образования нанокабелей Ag @ C и углеродистой оболочки. Зависимые от времени измерения XRD использовали для отслеживания изменения состава промежуточных и конечных продуктов наночастиц Ag @ C. Общий процесс состоит из двух стадий в зависимости от температуры реакции. На первом этапе глюкоза, AgNO 3 , и ЦТАБ использовались в качестве исходных материалов для получения нанокабелей Ag @ C при высокой температуре (180 ° C). На втором этапе температура реакции той же системы была снижена до 60 ° C для гидротермальной обработки. Временные интервалы для процессов роста и травления составляют 4 и 3 часа соответственно, как показано на рис. 3c.
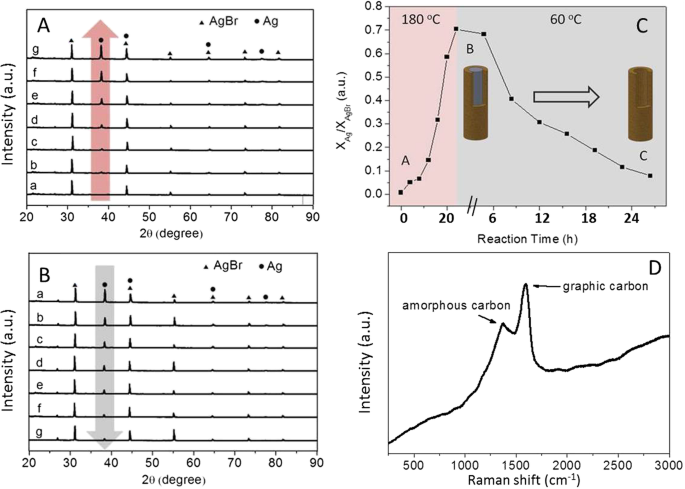
XRD, иллюстрирующий процессы образования наностержней Ag с углеродистой оболочкой ( A ) и постепенное самопереваривание Ag ( B ), кривая формирования и травления / эволюции сердцевины Ag ( C ) и рамановский спектр углеродсодержащих нанокабелей Ag @ C ( D )
На рис. 3 показаны дифрактограммы, показывающие, что первоначально образовавшийся осадок коричневого цвета показывает два интенсивных дифракционных пика, обозначенных как кубический AgBr (200) и (220) (карта JCPDS № 079-0149), соответственно. Вначале дифракционные пики Ag не наблюдались до тех пор, пока реакция не протекала в течение 8 ч при нагревании, при этом пик металлического Ag (111) появлялся при ~ 38,1 ° (карта JCPDS № 087-0717). Постепенное увеличение интенсивности типичного пика Ag (111) со временем указывает на то, что металлический Ag образовался и достиг своей максимальной интенсивности около 24 часов в описанных условиях. Было отмечено, что некоторые дифракционные пики, например Ag (200) и AgBr (220), каким-то образом перекрываются на рентгенограмме. Интересно отметить, что при понижении температуры реакции до 60 ° C происходил процесс травления ядер Ag, что подтверждается постепенно уменьшающейся интенсивностью типичного дифракционного пика Ag (111), расположенного при ~ 38,1 °. В течение десятков часов травление привело к исчезновению ядер Ag, что подтверждается практически исчезнувшим пиком Ag (111). Был проведен анализ продукта как функции времени реакции, как показано на фиг. 3c. Это указывает на то, что ядра Ag могут быть почти удалены в термических условиях, что согласуется с наблюдениями ПЭМ (рис. 1c, d). Кроме того, спектр комбинационного рассеяния (рис. 3D) показывает образование обоих типов углерода:аморфного и графического в этой реакционной системе.
На основании приведенного выше анализа XRD может существовать термодинамическое равновесие между восстановлением Ag + ионы глюкозой с образованием ядер Ag и окисление Ag Br - ионов, что согласуется с предыдущими сообщениями [38,39,40]. Например, Zhou et al. [39] продемонстрировали, что нанопроволоки Ag не образовывались до тех пор, пока температура реакции не превышала 140 ° C, что подтверждается работой Хуссейна [40]. Для карбонизации углеводов (например, глюкозы, сахарида) было широко признано, что углеродистый продукт можно синтезировать при температуре от 170 до 240 ° C [41, 42]. Однако углеродная оболочка нанокабелей аморфна, в отличие от углеродных нанотрубок или графена, полученных при высокотемпературном отжиге [1,2,3].
В частности, при травлении сердечников из серебра молекулы кислорода обладают высоким электродным потенциалом E 0 =+1,229 В по сравнению со стандартным водородным электродом (SHE), которого достаточно для окисления Ag 0 кому:Ag + ионы в рассматриваемой системе. Это может быть дополнительно подтверждено предыдущими исследованиями, в которых окисленное травление в присутствии галогенид-ионов (Br - ) к металлическим наночастицам правильной формы является анизотропным во всех направлениях [43, 44]. Xu et al. [43] сообщили, что Cl - или Br - ионы предпочитали травить плоскость (110) нанокристаллов Ag. Такая селективность может быть объяснена разницей в поверхностных свободных энергиях плоскостей кристалла Ag (111, 110 и 100). Guo et al. [44] управляли начальной точкой селективного травления со стороны наностержня, уменьшая пассивирование поверхности поверхностно-активным веществом и, следовательно, увеличивая реактивность на боковых плоскостях. Травление сердцевины Ag было также подтверждено нашими экспериментальными наблюдениями для наночастиц Ag @ C в аналогичных условиях реакции, как показано на рис. 4. Маленькие черные точки (рис. 4b) могут возникать в результате разложения AgBr в виде точек Ag под термическая обработка. Схематическая схема может быть использована для иллюстрации процесса синтеза Ag @ C и образования полой углеродистой оболочки (рис. 4c).
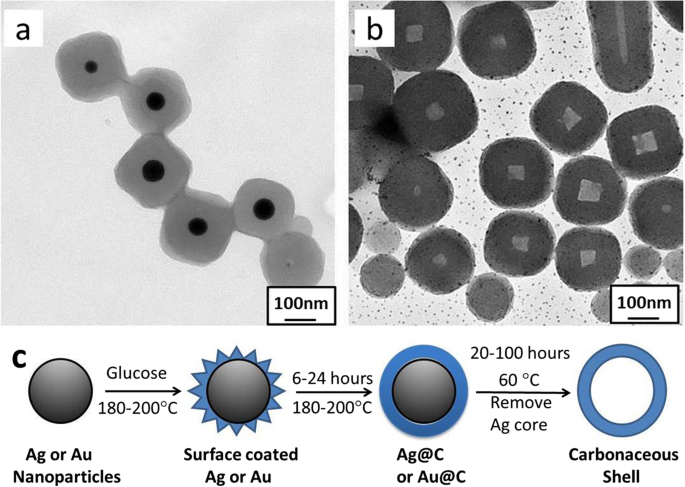
Травление ядра Ag из наночастиц ядро-оболочка Ag @ C ( a ) до полой углеродистой структуры ( b ). c Принципиальная схема, иллюстрирующая формирование и саморазложение наноструктур Ag @ C
Соответствующие УФ-видимые свойства нанокабелей ядро-оболочка Ag @ C в исходном состоянии и полая углеродистая структура также были измерены, как показано на рис. 5. Это также может дополнительно подтвердить, что сердцевина из серебра была вытравлена из нанокабелей. Нанокабели Ag @ C демонстрируют интенсивный пик поглощения, расположенный при ~ 382 нм (кривая A на рис. 5b), что указывает на существование металлического серебра, которое может вызывать сильный поверхностный плазменный резонанс [39]. Напротив, углеродные нанотрубки не показывают пиков поглощения, как показано на кривой C на фиг. 5b. Кроме того, ИК-Фурье спектр (рис. 5а) в основном предназначен для подтверждения образования углеродистой оболочки, богатой функциональными группами, такими как C =O, C – OH и OH [35].
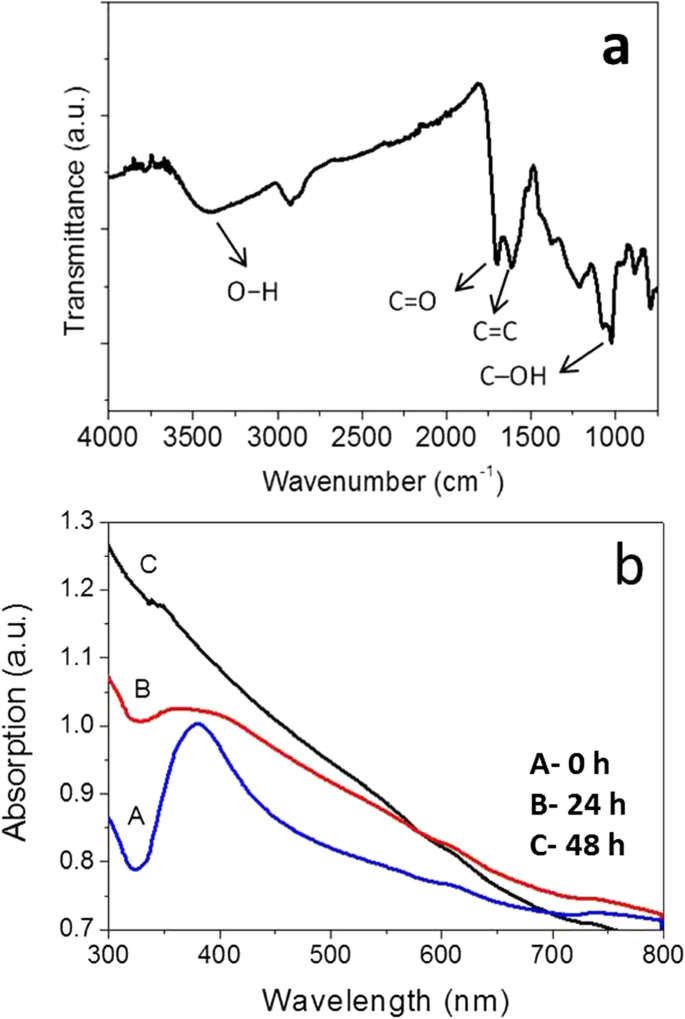
Оптические свойства нанокомпозитов Ag @ C и полых углеродных структур, измеренные с помощью ИК-Фурье спектра ( a ) и УФ-видимого спектра ( b )
Было подтверждено, что этот метод синтеза является общим не только для серебра, но и для других благородных металлов (например, золота). Здесь AuCl 4 - были выбраны ионы, и их легче восстанавливать глюкозой, чем Ag + ионов в тех же условиях, поскольку стандартный электрохимический потенциал AuCl 4 - / Au 0 пара (0,99 В относительно SHE) выше, чем у Ag + / Ag 0 пара (0,799 В относительно SHE) [45, 46]. Важно отметить, что Au более стабилен, чем Ag, и не токсичен, что способствует фототермическому эффекту в биомедицинских приложениях.
На рис. 6 показано, что углеродные наноструктуры Au @ C формировались с течением времени. Было ясно видно, что несферические наночастицы Au (рис. 6а) образовывались в течение 1 часа в описанных условиях, когда AuCl 4 - ионы сначала восстанавливались глюкозой; Между тем углеродная оболочка была сформирована вокруг наночастиц Au путем полимеризации глюкозы при температуре 180 ° C в течение пары часов, как показано на рис. 6c – e. С увеличением времени толщина углеродистой оболочки увеличивалась от нескольких нанометров (рис. 6d) до десятков нанометров (рис. 6e), а геометрия оболочки сильно зависит от формы самих частиц Au. Электронная дифракционная картина наночастиц ядро-оболочка Ag @ C была проиндексирована дифракционными кольцами, соответствующими плоскостям (100), (110), (111), (200) и (210) (рис. 6f) соответственно.

Структура ядра-оболочки Au @ C, сформированная со временем: a 1 ч, б 3 ч., c 6 ч., д 12 ч. И д 24 ч соответственно; е Диаграмма ED для частиц и дифракционных колец были проиндексированы как (100), (110), (111), (200) и (210); г единственная наночастица Au @ C вместе с ее изображением HRTEM ( h ) и индексированный шаблон ED ( i ) в монокристалле
Кристаллическая решетка одиночного нанокристалла Au (рис. 6g) в структуре ядро-оболочка была охарактеризована методом HRTEM. На рисунке 6h показано изображение ПЭМВР, на котором период решетки ~ 0,238 нм можно отнести к плоскости Au (111) [47, 48]. Пятна электронной дифракции на рис. 6i были проиндексированы как плоскости (100), (200) и (300), что указывает на формирование монокристалла Au в указанных условиях.
Чтобы дополнительно подтвердить предложенную стратегию синтеза, наностержни Au также были доступны для углеродистого покрытия в виде структур ядро-оболочка в указанных гидротермальных условиях. На рисунке 7 в качестве примера показан процесс покрытия углеродистой оболочки на наностержнях Au с соотношением сторон ~ 3,7. С увеличением времени толщина углеродистой оболочки на наностержнях Au увеличивалась с ~ 6 нм (рис. 7b) до ~ 15 нм (рис. 7c) и ~ 23 нм (рис. 7d), а углеродистая оболочка становилась сферой. -подобно через 24 ч, не зависит от длины наностержней Au (рис. 7г). Наблюдался значительный контраст для углеродистой оболочки (серый цвет) и золотых наностержней (черный цвет). На рис. 7e и f показаны изображения ПЭМВР одиночного наностержня Au до и после нанесения углеродистого покрытия. Период решетки ~ 0.204 нм можно отнести к плоскости Au (200). Спектроскопический анализ энергодисперсии (EDS) для наноструктур Au @ C и Ag @ C был проведен, как показано в Дополнительном файле 1:Рисунок S1. В данной работе было обнаружено, что углеродистая оболочка в меньшей степени влияет на структуру монокристаллов золота.

Структура Au @ C ядро-оболочка, полученная с разным временем реакции: a 0 ч (оригинальные золотые наностержни), b 4 ч., c 12 ч. И д 24 ч. е Изображение HRTEM для одиночного стержня Au. е Изображение HRTEM для одного углеродистого наностержня Au @ C
Оптические свойства
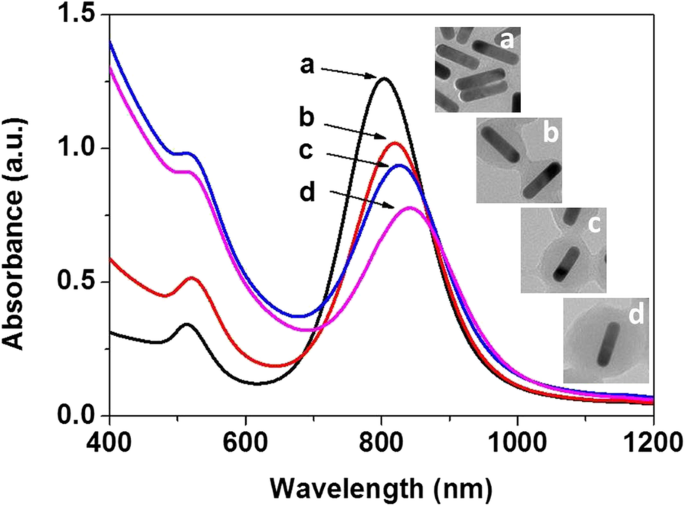
Соответствующие оптические свойства наноструктур Au @ C были измерены с помощью спектроскопии UV-Vis, как показано на рис. 8. Спектры поглощения наночастиц Au @ C (рис. 6a – e) постепенно смещаются в красную область от 560 нм ( а) до ~ 565 нм (б), ~ 580 нм (в), ~ 590 нм (г) и ~ 620 нм (д), соответственно, для интенсивного пика поглощения на фиг. 8А с увеличением толщины оболочки (фиг. 6c – d). Аналогичным образом, для наностержней Au @ C на рис. 7a – d толщина углеродистой оболочки влияет на интенсивный поверхностный плазмонный резонанс (продольная мода) наностержней Au и приводит к красному смещению от исходных ~ 810 нм (a) до ~ 820 нм. (b), ~ 826 нм (c) и ~ 848 нм (d), соответственно, как показано на рис. 8B, в то время как другой поверхностный плазмонный резонанс (поперечная мода), расположенный примерно на 518 нм, почти сохраняется в том же положении. То есть углеродистая оболочка действительно влияет на поверхностный плазмонный резонанс нанокомпозитов Au @ C [36].
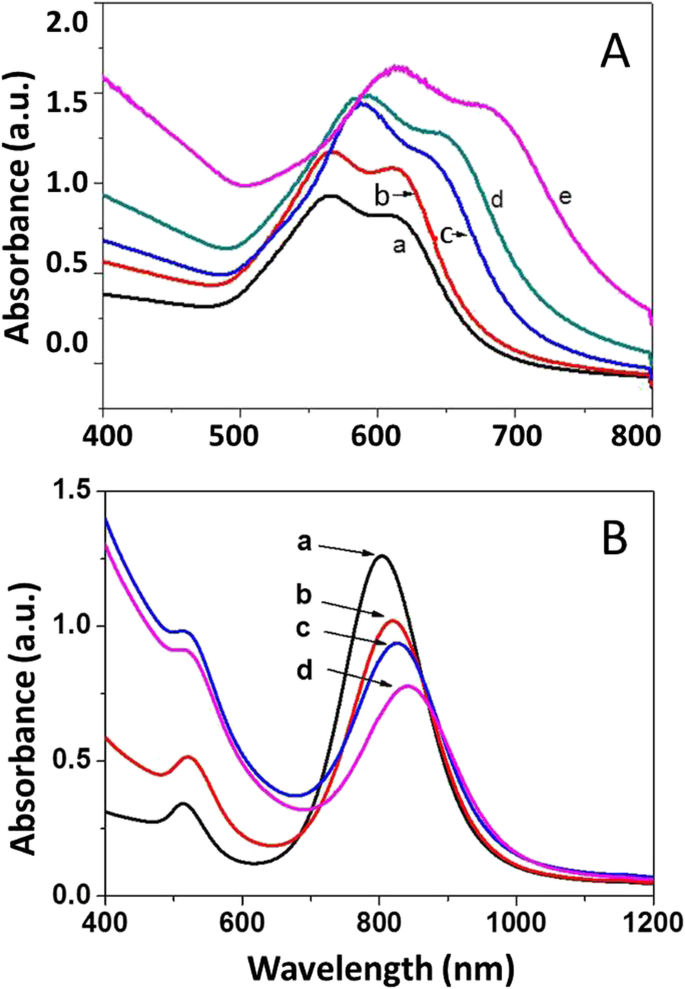
УФ-видимые спектры нанокомпозитов Au @ C: A Углеродные наночастицы несферической формы Au @ C, полученные через 1, 3, 6, 12 и 24 ч соответственно. Б Углеродные наностержни Au @ C, полученные через 0, 4, 12 и 24 ч соответственно
Как хорошо известно, Au - это благородный металл, и его наночастицы могут проявлять интенсивный поверхностный плазмонный резонанс (SPR), на который могут влиять его размер, морфология и окружающие среды. Как несферические наночастицы Au @ C (рис. 6a – e), так и наностержни Au @ C (рис. 7a – d) демонстрируют интенсивный ППР с постепенно смещающимися красными пиками в УФ-видимых спектрах (рис. 8A, B). ), что, вероятно, связано с увеличением толщины углеродистой оболочки на поверхности Au. Это может быть подтверждено предыдущими исследованиями [49,50,51,52]. Авторы сообщили, что модификация поверхности фотонных наноструктур, таких как наночастицы золота (Au), может привести к новым физическим явлениям, включая селективные взаимодействия света и вещества и процессы быстрой передачи энергии [49,50,51]. Другие сообщили, что углеродный компонент также может влиять на взаимодействия света и вещества в таких гибридных системах, например, за счет уменьшения эффектов рассеяния. Наличие многослойной графеновой оболочки (толщиной менее 5 нм) повлияло на оптические свойства и стабильность (химическую и термическую) инкапсулированных наночастиц Au [52].
Исследованы лазерно-индуцированные тепловые (фототермические) свойства углеродных наноструктур Au @ C. Au @ C был выбран в качестве примера, поскольку Au более стабилен, чем Ag, и не токсичен для биосистем. На рисунке 9 показаны фототермические свойства Au @ C с различной толщиной оболочки около 6 нм, 15 нм и 23 нм. Изменение цвета с синего (холодный) на красный (горячий), что указывает на повышение температуры в суспензии Au @ C. Подробные изменения температуры были записаны и показаны на фиг. 9В. В течение первых 600 с облучения для всех четырех образцов наблюдается быстрое повышение температуры. Температура асимптотически приближалась к стационарной в течение 1200 с. Очевидно, что поверхностное покрытие может снизить поглощение света нанокомпозитами Au @ C, имеющими более низкую температуру, чем чистые наностержни Au:от ~ 10,6 ° C до ~ 9,3 ° C и ~ 8,1 ° C, соответственно, что соответствует ~ 6 нм, ~ 15 нм, и наностержни Au, покрытые углеродистой оболочкой размером ~ 23 нм. Аналогичная тенденция наблюдалась для Au @ SiO 2 нанокомпозиты, где более толстый SiO 2 оболочка приводила к снижению температуры, например, 5-нм SiO 2 Оболочка привела к понижению температуры на ~ 5 ° C по сравнению с голыми наностержнями Au [53].
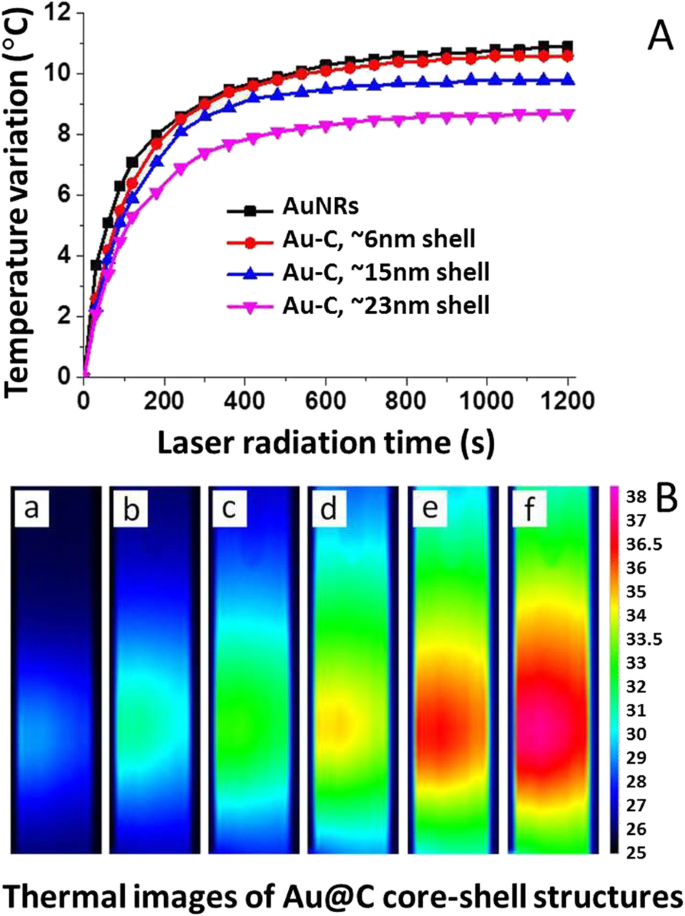
Лазерное испытание фототермического эффекта углеродистого нанокомпозита Au @ C с плотностью мощности лазера 0,17 Вт / см 2 . А Зависимость температуры от времени облучения для водного раствора наноструктур Au @ C разной толщины:голые наностержни Au без углеродистого покрытия, ~ 6 нм, ~ 15 нм и ~ 23 нм, в которых концентрация каждой системы регулировалась чтобы получить интенсивность экстинкции 1,0 при 800 нм. Б Фототермические изображения углеродистых наноструктур Au @ C представляют разное время:(a) 30, (b) 60, (c) 90, (d) 180, (e) 360 и (f) 840 секунд при 0,17 Вт / см −2 облучение
Хотя углеродистая оболочка привела к снижению температуры, она по-прежнему привлекательна, потому что голые наночастицы Au недоступны для прямого применения в биосистемах из-за реакции с биомолекулами (белками, аминами). Конечно, в будущей работе необходимо оптимизировать конкурирующие параметры для конкретного приложения. В общем, углеродная оболочка должна хорошо контролироваться, чтобы не делать ее слишком толстой, чтобы избежать значительного снижения поглощения света, а также оболочка не должна быть слишком тонкой, чтобы ее можно было сломать под воздействием света. Очевидно, что и голые наностержни Au, и нанокомпозиты Au @ C могут привести к значительному повышению температуры до нужного диапазона (например, 37–47 ° C) за счет лазерного облучения, что является потенциалом для фототермической терапии, в то время как они связаны с целевыми молекулами лекарственного средства. Regarding the relationship between optical and photothermal properties, both of them for Au@C nanostructures are dependent on SPR from noble metallic Au. The SPR, a unique phenomenon to plasmonic Au nanoparticles, leads to strong electromagnetic fields on the particle surface and consequently enhances all the radiative properties such as absorption and scattering. Additionally, the strongly absorbed light is converted to heat quickly via a series of nonradiative processes, if external light acts on the surface of Au nanoparticles. As noted, the photothermal property is mainly caused by NIR light but not visible light [54]. It is needed to be pointed out that more works are needed to be conducted in the near future, focusing on the optimization of pertinent parameters in concentration, pH, particle size, and surface modification for real biomedical applications of such Au@C carbonaceous nanocomposites.
Выводы
This study developed a general strategy for the synthesis of noble metal carbonaceous nanocomposities (Au@C, Ag@C) with different morphologies by controlling hydrothermal conditions. A few interesting findings can be summarized as follows:
- i)
A high-temperature hydrothermal reaction (180–200 °C) could result in the formation of noble metal@C core-shell nanostructures, in which the glucose played a multiple role:reductant for metallic ions, shape modifier, and surface protection;
- ii)
A low-temperature (60–100 °C) hydrothermal reaction for the Ag@C core-shell system was beneficial for etching Ag to obtain hollow carbonaceous sheath, due to the etchant (Br − / O 2 ). This may open a simple path for fabricating hollow carbon nanostructures (e.g., tubes). However, the Au@C core-shell nanoparticles are quite stable under the same conditions;
- iii)
The generated Ag or Au cores are well crystallized, but the carbonaceous sheath is amorphous; and
- iv)
The rodlike Au@C nanocomposites were laser-induced to show photothermal effect, and the thickness of carbonaceous shell can tune the photothermal temperature, potential for biomedical applications.
Generally, this work may offer a simple but effective synthesis strategy, not only for noble metals but also for other metals, metal oxides, and inorganic materials to design and construct controllable carbonaceous nanostructures with potential applications in sensor, energy storage, catalysis, and biomedicine.
Доступность данных и материалов
The data and material provided in this study are available in Additional file 1.
Сокращения
- Ag@C:
-
Silver carbonaceous nanostructure
- Au@C:
-
Gold carbonaceous nanostructure
- CCD:
-
Устройство с зарядовой связью
- CTAB:
-
Бромид цетилтриметиламмония
- EDS:
-
Energy dispersion spectroscopy
- FT-IR:
-
Инфракрасное преобразование Фурье
- GO:
-
Оксид графена
- HRTEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- PVA:
-
Поли (виниловый спирт)
- SEM:
-
Сканирующая электронная микроскопия
- ОНА:
-
Стандартный водородный электрод
- SPR:
-
Поверхностный плазмонный резонанс
- ТЕМ:
-
Просвечивающая электронная микроскопия
- УФ-видимый:
-
Ultraviolet-visible spectrometer
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Опорные конструкции для 3D-печати металлом - более простой подход
- Электроспряденные полимерные нановолокна, украшенные наночастицами благородных металлов для определения х…
- Изготовление и фотокаталитические свойства новых нанокомпозитов SrTiO3 / Bi5O7I
- Новая кластерная микроструктура наноконусов с антиотражающими и супергидрофобными свойствами для фотоэлек…
- Производство крупномасштабных дендритных наноструктур серебра с контролем морфологии для катализа и прилож…
- Важность моделей САПР для проектов по изготовлению металлоконструкций
- Обзор для начинающих:что такое металлообработка?
- 4 распространенных заблуждения о ценообразовании на изготовление металлоконструкций
- Почему удаление заусенцев важно для проектов по изготовлению металлоконструкций?
- Какой тип изготовления листового металла мне подходит?



