Новые взгляды на адсорбцию CO2 наноматериалами на основе слоистого двойного гидроксида (LDH)
Аннотация
Межламеллярное расстояние слоистых двойных гидроксидов (LDH) было увеличено сначала додецилсульфонат-ионами, а затем (3-аминопропил) триэтоксисилан (APS) был химически привит (APS / LDH). Структурные характеристики и термическая стабильность полученных образцов были охарактеризованы методами рентгеновской дифракции (XRD), просвечивающей электронной микроскопии (TEM), инфракрасного спектрометра с преобразованием Фурье (FTIR), термогравиметрического анализа (TG) и элементного анализа (EA) соответственно. . СО 2 Адсорбционные характеристики были исследованы с использованием ТГ и инфракрасной спектроскопии с преобразованием Фурье с диффузным отражением (DRIFTS). Результаты показали, что CO 2 адсорбционная емкость на APS / LDH составила 90 мг / г и не показала очевидного снижения во время пяти циклических испытаний адсорбции-десорбции, что указывает на его превосходную стабильность характеристик. Результаты DRIFTS показали, что как карбаматы, так и слабо связанный CO 2 виды были созданы на APS / LDH. Слабо адсорбируемые частицы были вызваны различной химической средой для CO 2 захват обеспечивается поверхностными частями СДГ, такими как свободный силанол и водородные связи.
Фон
Парниковый эффект и глобальное изменение климата в основном вызваны значительным выбросом CO 2 выбросы угольных электростанций вызвали озабоченность широкой общественности [1,2,3]. Таким образом, CO 2 улавливание должно быть принято для его последующего хранения или утилизации, чтобы снизить уровень его концентрации в атмосфере. Большое внимание для CO 2 привлекли различные сорбенты на основе растворителей и твердых веществ. улавливание, особенно модифицированные амином пористые композиты из-за их сравнительно низкого энергопотребления на регенерацию и легкости реализации в широком диапазоне температур и давлений [4,5,6].
Высокий и стабильный CO 2 Адсорбционная способность является основной для крупномасштабного процесса отделения углерода от дымового газа с большим объемом и низким парциальным давлением в диапазоне температур 50 ~ 100 ° C [1]. Поскольку аминогруппы показывают сродство к CO 2 молекул, различные пористые носители с большой площадью поверхности и объемом пор были адаптированы для получения композитных адсорбентов на основе их аккомодации к пропитанным аминам после работы Сонга в 2002 году [7]. И самый высокий CO 2 адсорбционная способность, описанная в литературе, может достигать 7,9 ммоль / г [8]. Однако эти виды пропитанных композитов подвержены ухудшению рабочих характеристик во время операции циклической адсорбции-десорбции, что свидетельствует о плохой стабильности, что также является важным критерием для реальных приложений [9]. Кроме того, сильное ограничение диффузии также создается агломерированными аминами и покрытыми частицами для CO 2 с поверхности в объемные аминогруппы, что снизит эффективность амина, определяемую как количество адсорбированного CO 2 молекул на каждый моль атома азота.
Для улучшения термической стабильности и аминовой эффективности композитных адсорбентов монослой CO 2 или меньше сайты сродства формируются путем прививки аминосиланов на материалы носителя на основе их реакции соконденсации, которая была широко изучена с использованием 3-аминопропилтриметоксисилана (APS), 3- (триметоксисилил) пропилэтилендиамина (диамина) или 3- [2- (2 -аминоэтиламино) этиламино] пропилтриметоксисилан (триамин) и др. [2, 10, 11, 12]. Эти виды привитых композитов демонстрируют более низкие диффузионные ограничения и превосходную стабильность, даже несмотря на то, что может быть верхний предел CO 2 адсорбционная способность, поскольку предполагается, что для захвата одного моля CO 2 требовалось два моля незащищенных аминогрупп. молекул по цвиттерионному механизму [13, 14]. Тем не менее, химическая природа материалов носителя также может влиять на CO 2 адсорбционная производительность. Вклады поверхностных гидроксилов в CO 2 был исследован захват либо за счет их прямой слабой физической силы [15], либо за счет водородной связи с привитыми аминами [13, 16] на адсорбентах на основе диоксида кремния / диоксида титана.
Слоистые двойные гидроксиды (СДГ) представляют собой упорядоченные соединения, которые собираются за счет интерламинирования анионов и положительно заряженных слоистых пластиков с общей формулой [M 1 - x 2+ M x 3+ (ОН) 2 ] x + (A n - ) x / н · МГн 2 O, где M 2+ и M 3+ представляют собой катионы металлов, а A - анион [17]. СДГ нашли широкое применение в адсорбции, катализе, фотохимии и т. Д. Из-за их настраиваемой структуры и низкой стоимости сырья [6, 18,19,20], что также делает их возможным кандидатом для дожигания CO 2 захватывать. Wang et al. [21] синтезировали модифицированные амином СДГ посредством отшелушивания и прививки и сообщили, что эти адсорбенты могут быть полезны в CO 2 улавливают процессы с высокой температурой 80 ° C, в то время как CO 2 адсорбционная емкость на модифицированном амином гексагональном мезопористом диоксиде кремния (ГМС) снизилась с 1,34 ммоль / г при 25 ° C до 0,45 ммоль / г при 75 ° C [22]. Это говорит о том, что местные химические вещества LDH в качестве вспомогательных материалов могут влиять на CO 2 адсорбция отличается от кремнеземных опор. Однако, насколько нам известно, об этом говорится в нескольких отчетах. Систематическое исследование необходимо для изучения сорбентов на основе ЛДГ и дальнейшего понимания их CO 2 механизмы адсорбции.
Имея это в виду, в данной статье были приготовлены модифицированные (3-аминопропил) триэтоксисиланом (APS) LDH (APS / LDH) с использованием додецилсульфата (DS) для предварительной интеркаляции. Структурные характеристики APS / LDH подробно рассматривались в [21]. Тем не менее, некоторые количества будут повторно введены, чтобы проиллюстрировать связь между CO 2 адсорбционные характеристики и особенности поверхности СДГ. СО 2 Адсорбционно-десорбционные свойства APS / LDH изучались в основном с использованием in situ измерений инфракрасной спектроскопии с преобразованием Фурье диффузного отражения (DRIFTS).
Методы
Все использованные химические вещества были приобретены у Aladdin reagent Co., Ltd., и принадлежали A.R. оценка. И эти химические вещества использовались без дополнительной обработки.
Синтезированные СДГ получали в качестве контрольного образца методом соосаждения. Смешанный раствор, содержащий 0,075 моль Mg (NO 3 ) 2 · 6H 2 O и 0,025 моль Al (NO 3 ) 3 · 9H 2 Сначала был получен O, который затем был добавлен к Na 2 CO 3 водный раствор (0,5 моль / л, 100 мл) при интенсивном перемешивании при 70 ° C. Значение pH этой смеси поддерживали около 10, используя водный раствор NaOH (4 M), с последующим перемешиванием в течение еще 4 часов. После этого образовавшийся осадок отфильтровали, несколько раз промыли дистиллированной водой и сушили в условиях вакуума при 120 ° C в течение ночи. DS-интеркалированные LDH (DS / LDH) были синтезированы 7 согласно предыдущему сообщению [21]. Обычно 4,00 г Mg (NO 3 ) 2 · 6H 2 O и 1,95 г Al (NO 3 ) 3 · 9H 2 О растворяли в 50 мл деионизированной воды. Полученный раствор по каплям добавляли к водному раствору додецилсульфата натрия (3 г / 100 мл дистиллированной воды) при непрерывном перемешивании при 70 ° C. Особое внимание следует уделить доведению pH примерно до 10. Та же дополнительная обработка, описанная выше, была применена и к DS / LDH.
LDH с привитыми APS (APS / LDH) получали следующим образом. Два грамма DS / LDH растворяли в конической колбе с 500 мл толуольного растворителя, а затем подвергали обработке ультразвуком в течение 5 часов. Через полчаса собрался обильный белый гель. Добавляли пятнадцать миллилитров (3-аминопропил) триэтоксисилана, и раствор смеси выдерживали при 60 ° C в атмосфере азота в течение 5 часов. Осадок экстрагировали фильтрацией, многократно промывали, а затем сушили в вакуумной печи при 120 ° C в течение ночи.
Кристаллические фазы образцов анализировали с помощью рентгеновского дифрактометра с CuKα-излучением (XRD:модель D / max RA; Rigaku Co., Япония, CuKα-излучение 0,15418 нм), и собирали данные для углов рассеяния (2 θ ), который составлял от 5 ° до 70 ° с шагом 0,02 °. Микроморфологию исследовали с помощью просвечивающей электронной микроскопии (ТЕМ:Tecnai G2 F20; FEI Company, США). Элементный анализ выполнен на Flash EA1112 (Thermo Finnigan, США). Инфракрасный спектрометр с преобразованием Фурье (FTIR, IR Affinity-1; SHIMADZU, Япония) использовали для регистрации ИК-спектров приготовленных образцов. Пластины из бромида калия (KBr), смешанные с 1/50 образца, были изготовлены путем приложения давления масла 20 тонн и затем сканированы от 400 до 4000 см -1 с разрешением 0,2 см −1 . Термическую стабильность твердых образцов определяли с помощью термогравиметрического анализа (TG; NETZSCH STA 409 Luxx, Зельб / Бавария, Германия). Образцы нагревали от комнатной температуры до 600 ° C со скоростью нагрева 10 К / мин в атмосфере азота.
Информация о видах поверхности и молекулярном поведении на поверхности адсорбентов была получена с помощью DRIFTS (спектрометр Nicolet 6700 FT-IR, Thermo Scientific, США), который был оснащен системой контроля температуры и соединен с окнами из ZnSe. В ячейке DRIFTS порошковые адсорбенты предварительно обрабатывали в течение 1 ч при 200 ° C в потоке азота 30 мл / мин. Когда температура стабилизировалась на уровне 50 ° C, CO 2 В кювету вводили поток газа 5 мл / мин на время до полного насыщения. Здесь CO 2 Концентрация (~ 14 об.%) в газовой смеси указывает на ее общую концентрацию в промышленных дымовых газах. Спектры DRIFTS были получены при 4 см -1 разрешение и 64 совместно добавленных безымянных изображения с учетом фоновых спектров, записанных непосредственно перед введением зондирующих молекул.
CO 2 адсорбционная способность также определялась ТГ. Примерно 10 мг образцов предварительно обрабатывали при 120 ° C в течение 1 ч в атмосфере азота со скоростью 100 мл / мин. После охлаждения до температуры адсорбции чистый CO 2 поток включали до тех пор, пока не установилось динамическое адсорбционное равновесие. Окончательный набранный вес считался его CO 2 . адсорбционная способность. Насыщенные образцы регенерировали в условиях предварительной обработки. Эту процедуру адсорбции-регенерации повторяли пять раз для оценки стабильности характеристик модифицированных адсорбирующих материалов.
Результаты и обсуждение
Как показано на рис. 1, возникла серия типичных пиков из-за слоистой структуры для синтезированных СДГ при 2 θ =11.5 °, 23.0 °, 34.5 ° и 60.5 °, которые, согласно ранее опубликованным данным [23, 24], приписывались плоскостям решетки (003), (006), (009) и (110) соответственно. Следует отметить, что более низкий угол брэгговского отражения (003), в дополнение к порядку скважины (00 l ), появившаяся для DS / LDH, образованных расширенной структурой при внедрении органических анионов в слоистые пластины LDH. Этот расширенный промежуточный слой, предполагающий высокое воздействие на поверхностные гидроксильные группы и низкое ограничение диффузии, позволил DS / LDH стать предшественником для последующего введения APS. Прививка APS резко снизила кристалличность. Однако гидроталькитоподобная структура основы сохранялась для наблюдаемого отражения (110). Это было подтверждено ПЭМ-изображением APS / LDH (рис. 2), когда были продемонстрированы агрегаты нерегулярных хлопьевидных частиц.
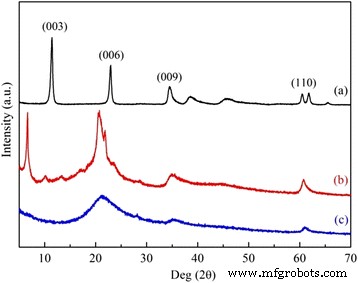
Профили дифракции рентгеновских лучей ( a ) ЛДГ, ( b ) DS / LDH и (c) APS / LDH

ТЕМ-изображение APS / LDH
Молярное отношение C / N составляет 9 в молекуле APS (C 9 H 23 НЕТ 3 Si). Соответственно, молярные отношения C / N будут 7, 5 или 3, если 1, 2 или 3 этоксисилановые группы конденсируются с поверхностными гидроксильными группами на ламинатах LDH соответственно [21]. Здесь молярное соотношение C / N (таблица 1) было принято для дальнейшего подтверждения успешной прививки APS. Так как было получено молярное соотношение C / N 6,59, то по крайней мере одна этоксисилановая группа в каждой молекуле APS была привязана к металлическим слоям, в то время как другие представляли собой интактные этоксисилановые группы или свободные силанольные связи после гидролиза.
Исследование TG-DTG (DTG - производная кривая TG) было проведено для изучения термостабильности модифицированных LDH. Как показано на рис. 3, DS / LDH претерпели три стадии потери массы, которая была приписана удалению адсорбированной воды при температуре ниже 150 ° C; дегидроксилирование в интервале температур от 150 до 300 ° C с заметной потерей происходило при 240 ° C, а также дальнейшее дегидроксилирование и разложение додецилсульфата при температуре более 300 ° C [24, 25]. Поведение при термическом разложении APS / LDH значительно отличалось (рис. 4). Было отмечено, что потеря веса APS / LDH из-за дегидроксилирования (150 ~ 300 ° C) составила около 10%, что намного меньше, чем потеря веса DS / LDH (приблизительно 30%). В основном это может быть связано с потреблением -ОН на ламинатах LDH после прививки APS в результате реакции конденсации, как показано на рис. 5. Кроме того, потеря веса достигла пика даже при более высокой температуре 321 ° C, что вызвано замедленным дегидроксилированием. на APS / LDH, которые могут получить выгоду от водородной связи между концом –NH 2 молекул APS и поверхностных гидроксилов на ламинатах LDH.
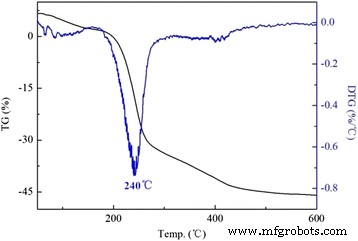
Кривые ТГ-ДТГ ДС / ЛДГ
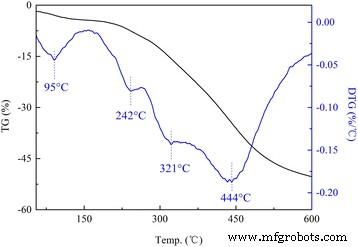
Кривые ТГ-ДТГ APS / LDH
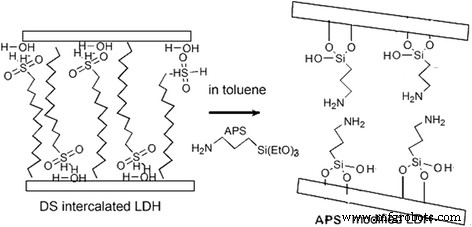
Схематическое изображение образования APS / LDH
ИК-спектры модифицированных СДГ показаны на рис. 6. Для СДГ сильный широкий пик с центром при 3460 и полоса при 1650 см −1 был связан с растягивающими и изгибными колебаниями гидроксильных групп с поверхности и / или прослойки соответственно. Полосы поглощения при 1370 см −1 были отнесены как к монодентатному карбонату, так и к интеркалированному NO 3 - в межслоевом пространстве СДГ. Обертон колебаний решетки Mg – O, а также мод Al – O перекрывает спектр от 800 до 400 см −1 . . Молекулы DS в DS / LDH показали группу характеристических полос при 2920 (валентное колебание –CH 3 групп), 2852 (валентное колебание –CH 2 групп), 1465 (изгибная связь C – H органического скелета) и 1217/1075 см −1 (асимметричные и симметричные валентные колебания –SO 3 2– группы). Однако интенсивности этих характеристических полос были существенно ослаблены после прививки APS, в то время как наблюдались новые полосы, относящиеся к связям N – H и N – C в молекулах APS, например колебание N – H 2 в первичных аминогруппах (RNH 2 ) при 1570/1468 см −1 и изгибное колебание C – N для C – N при 1124 см −1 [13, 23].
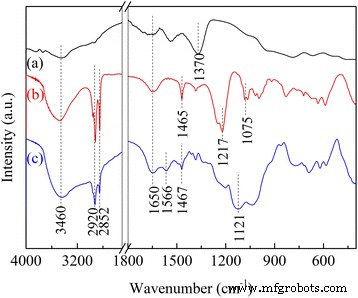
FTIR-спектры ( a ) ЛДГ, ( b ) DS / LDH и ( c ) APS / LDH
Несмотря на то, что часть поверхностных групп -OH на ламинатах LDH была израсходована в результате реакции конденсации с силанолами APS, как было упомянуто выше, полосы, расположенные на 3460 и 1650 см -1 были несколько усилены. Сообщалось, что будет происходить неравномерное распределение привитых APS, например кластеризация аминогрупп через их межмолекулярные водородные связи [16] и протонирование аминов (RNH 3 + ), образующиеся в присутствии воды [26], с поверхностными гидроксилами или со свободными силанольными группами. Также считалось, что основные молекулы или группы могут быть связаны водородными связями с поверхностными гидроксилами СДГ, даже если эта связь была довольно слабой [27]. Таким образом, здесь усиление этих полос поглощения было приписано ограниченному –NH 2 группы перекрываются с группой –OH в том же ИК-диапазоне [28], что указывает на довольно иное локальное окружение для CO 2 адсорбция.
CO 2 Адсорбционные характеристики модифицированных амином СДГ исследовали с помощью ТГА при различных температурах испытаний. Как показано на рис. 7, CO 2 количество адсорбции на APS / LDH резко увеличилось в течение первых 30 минут, после чего последовала стадия медленного насыщения. CO 2 на этой стадии насыщения была получена адсорбционная способность до 2,09 ммоль / г, что намного выше, чем у СДГ (обычно менее 1,0 ммоль / г [29,30,31]). Следовательно, включенные аминогруппы способствовали образованию CO 2 захват значительно. Следует отметить, что APS / LDH показали CO 2 количество адсорбции 1,55 мг / г при 25 ° C, в то время как он показал довольно стабильную адсорбционную способность в диапазоне температур от 30 до 75 ° C. APS начинает реагировать с CO 2 от 28 ° С [21]. Таким образом, более высокая вязкость APS при 25 ° C приведет к большему ограничению массопереноса и еще больше ослабит его функцию для CO 2 захват.
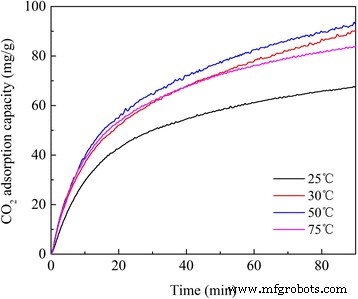
CO 2 профили адсорбции на APS / LDH при разных температурах
Доступность аминогрупп и близость соседних аминопар, по существу, определяли CO 2 адсорбционная способность для материалов, модифицированных амином. Пропитанные амины хотели бы агломерироваться в порах носителей, что создавало сильное ограничение диффузии CO 2 молекулы с поверхности в объем [2, 9, 25, 32]. Однако на доступность активных сайтов в APS / LDH могут также отрицательно влиять углеводородные цепи, интеркалированные между ламинатами LDH, что снижает подвижность и относительную близость аминопар. Это, по-видимому, неблагоприятно сказалось на аминовой эффективности APS / LDH, которая все же оказалась немного выше 0,5, что было максимальным значением, основанным на цвиттерионном механизме (таблица 1). Таким образом, был сделан вывод, что здесь может быть другой механизм адсорбции, способствующий эффективности амина.
Измерение DRIFTS было принято для исследования CO 2 механизм адсорбции на APS / LDH (рис. 8). Воздействие CO 2 / N 2 смесь газов приводила к появлению нескольких типичных пиков поглощения, которые были связаны с деформацией N – H в RNH 3 + при 1629 и 1489 см −1 , режим асимметричного растяжения COO - при 1567 см −1 , и вибрация скелета NCOO на 1428 и 1326 см −1 [13]. Очевидно, CO 2 адсорбция на первичных аминах происходит по цвиттер-ионному механизму с двухступенчатой последовательностью, то есть сначала образование цвиттер-иона и последующий перенос протона [13, 14].
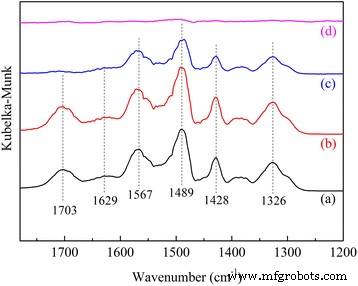
ДРИФТ-спектры CO 2 адсорбция и десорбция на APS / LDH:( a ) адсорбция в течение 5 мин, ( b ) адсорбция в течение 20 мин, ( c ) продувка в течение 30 мин при комнатной температуре, ( d ) продувайте еще 30 мин при 120 ° C
В частности, появившаяся полоса 1703 см −1 требовалась дальнейшая идентификация. Поскольку он полностью исчез в мягких условиях регенерации, в то время как образовавшиеся карбаматы разлагались при более высокой температуре, эта полоса может быть связана со слабосвязанным CO 2 виды вокруг ограниченного −NH 2 группа [33], которая предоставила другую локальную среду для адсорбции. CO 2 молекулы могут быть захвачены этими аминогруппами посредством водородных связей. Wu et al. [13] приписали полосу поглощения 1706 см −1 с водородно-связанным CO 2 частицы, образующиеся в результате его адсорбции рядом с протонированными аминогруппами. Danon et al. [16] также обнаружили, что поверхность SBA-15 играет значительную роль в специфических взаимодействиях между CO 2 и фрагменты, связанные с поверхностью SBA-15.
Стабильная циклическая адсорбция / десорбция адсорбентов особенно желательна для практического процесса разделения. Циклические характеристики APS / LDH были получены (рис. 9) за счет воздействия CO 2 при различных температурах адсорбции, а затем повторная регенерация при 120 ° C. СО 2 адсорбционная способность колебалась вокруг начальной величины адсорбции в течение этих пяти циклов при этих температурах испытаний, показывая отличные циклические характеристики. Это дало возможность APS / LDH улавливать CO 2 . от тепловых электростанций, работающих на ископаемом топливе [1]. Во-первых, можно добиться экономии энергии на регенерацию по сравнению с прокаленными образцами СДГ, которые требовали активации при повышенных температурах, например, 400 ° C [34]. Более того, CO 2 адсорбция на прокаленных образцах СДГ снижалась с увеличением количества циклов термической адсорбции / десорбции из-за необратимой хемосорбции, вызванной плохой термостабильностью и агломерацией частиц [35], в то время как APS / LDH здесь показали превосходную стабильность рабочих характеристик.
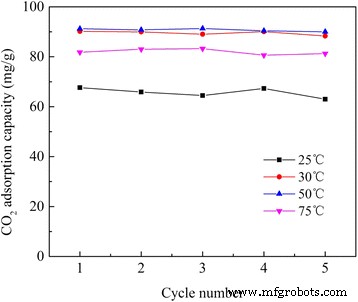
Стабильность характеристик APS / LDH во время последовательных циклов адсорбции-десорбции
Выводы
Монослой концевых аминогрупп APS прививали на LDH (APS / LDH) для CO 2 захватывать. Было обнаружено, что увеличенное расстояние между слоями, заполненное додецилсульфонатом, было благоприятным для введения APS. APS был связан с ламинатами LDH ковалентным взаимодействием. Включенные аминогруппы вносят большой вклад в CO 2 захват на APS / LDH как за счет механизма цвиттериона, так и за счет слабого связывания, что подтверждается результатами DRIFTS. СО 2 адсорбционная способность стабилизировалась на уровне около 90 мг / г в течение пяти циклов адсорбции-десорбции, что демонстрирует большой потенциал применения в процессах адсорбции с переменным температурным режимом.
Для оксидных адсорбентов на основе СДГ постепенно сниженное содержание CO 2 рост наблюдался, прежде всего, из-за все большей недоступности основных сайтов. Однако APS / LDH более устойчивы к различным условиям обработки, поскольку они основаны на химической комбинации (3-аминопропил) триэтоксисилана и металлических слоев. Это эффективно предотвращает значительную потерю адсорбционной способности из-за выщелачивания органических веществ из твердых частиц во время циклических испытаний. И захваченный СО 2 может быть полностью десорбирован при температуре ниже 120 ° C на APS / LDH, что является довольно безопасной рабочей температурой, чтобы избежать разложения амина или термического конформационного изменения.
Сокращения
- APS:
-
(3-аминопропил) триэтоксисилан
- ДРИФТЫ:
-
Инфракрасная спектроскопия с преобразованием Фурье с диффузным отражением
- DS:
-
Додецилсульфат
- EA:
-
Элементный анализ
- FTIR:
-
Инфракрасный спектрометр с преобразованием Фурье отражательной способности
- HMS:
-
Гексагональный мезопористый кремнезем
- LDH:
-
Слоистые двойные гидроксиды
- ТЕМ:
-
Просвечивающая электронная микроскопия
- TG-DTG:
-
Термогравиметрический анализ - кривая производной ТГ
- XRD:
-
Рентгеновская дифракция
Наноматериалы
- Новый технический документ OMP:глубокое погружение в решения на основе данных
- Представляем новые технологии на рабочем месте? Вот что вам нужно знать
- Графен заменяет наноматериалы
- Виттманн Баттенфельд переезжает в новую бразильскую локацию
- Новое гибкое устройство может преобразовывать сигналы WiFi в электричество
- Новый ИИ может преобразовывать неподвижные изображения в 3D-анимацию
- Новый метод может превратить любой объект в блок хранения данных
- Проект логотипа и веб-сайта направляет новую поплавковую удочку в прибыльные воды
- Промышленный Интернет вещей вдыхает новую жизнь в завод Aircon
- Оливер Вайман:Взгляд на фабрику будущего



