Безферментные биосенсоры глюкозы на основе нанокомпозитов MoS2
Аннотация
Высокопроизводительные биосенсоры глюкозы очень востребованы в здравоохранении. Чтобы удовлетворить эти требования, биосенсоры глюкозы, особенно биосенсоры глюкозы, не содержащие ферментов, получили большое внимание. Двумерные материалы, например графен, с большой площадью поверхности, превосходными электрическими свойствами и хорошей биосовместимостью, были основным направлением исследований биосенсоров в последнее десятилетие. В этом обзоре представлены последние достижения в области разработки безферментных биосенсоров глюкозы на основе MoS 2 . нанокомпозиты. Представлены два различных метода определения глюкозы с упором на электрохимические биосенсоры глюкозы. Проблемы и перспективы MoS 2 Также обсуждаются нанокомпозитные биосенсоры глюкозы.
Введение
Концентрация глюкозы в крови человека - важный показатель здоровья. Например, у здоровых людей уровень глюкозы в крови обычно составляет около 3,9–6,1 мМ (1 мМ =18 мг / дл), а концентрация глюкозы за пределами этого диапазона может указывать на дисфункцию почек, диабет и т. Д. [1]. В связи с постоянно растущим спросом на здравоохранение, много усилий было направлено на создание ферментативных биосенсоров глюкозы на основе глюкозооксидазы (GO x ) после сообщения Апдайка и Хикса об энзимном электроде в 1967 г. [2]. Несмотря на простоту, эффективность, высокую чувствительность и селективность ферментативных биосенсоров глюкозы, две основные проблемы, а именно высокая стоимость и нестабильность, все еще не могут быть удовлетворительно решены. Это связано с тем, что ферментные сенсоры глюкозы используют ферменты, такие как GO x для косвенного определения глюкозы, что часто требует дорогостоящих катализаторов и сложной конструкции устройства, а, следовательно, относительно высокой стоимости [3, 4]. Кроме того, такие ферменты, как GO x уязвимы к температуре, влажности, pH и нефизиологическим химическим веществам из-за их внутренней термической и химической нестабильности [5, 6]. Иммобилизация ГО x на поверхности электрода часто добавляет еще один уровень сложности при изготовлении ферментативных сенсоров глюкозы с хорошей стабильностью и воспроизводимостью [7, 8].
Благодаря развитию Интернета вещей, датчики низкой стоимости и высокой надежности привлекают все больше внимания. В поисках сенсоров глюкозы, отвечающих этим требованиям, электрохимические биосенсоры, не содержащие ферментов, приобрели популярность благодаря ряду преимуществ, включая простоту, высокую чувствительность и стабильность [9,10,11,12]. Безферментные электрохимические биосенсоры непосредственно обнаруживают глюкозу посредством электрокаталитического окисления, что позволяет избежать использования дорогостоящих ферментов, а также повышает стабильность в условиях окружающей среды. Ожидается, что такие биосенсоры откроют новые возможности для использования с портативными устройствами и определения уровня глюкозы в реальном времени [13]. Ключом к реализации практических сенсоров глюкозы, не содержащих ферментов, являются недорогие, надежные, биосовместимые и многочисленные катализаторы. С этой целью нанокомпозиты, например, композиты из двумерных материалов и наночастиц, были широко приняты в качестве электродных материалов биосенсоров [14]. В частности, биоэлектроника, основанная на двумерных (2D) материалах, становится новой захватывающей междисциплинарной областью благодаря множеству уникальных физических и химических свойств 2D-материалов, включая большую удельную поверхность, отличную проводимость и простой синтез. Например, большая удельная поверхность 2D-материалов позволяет легко функционализировать поверхность за счет гибридизации. Высокая проводимость позволяет эффективно переносить и собирать заряд в 2D-материалах. Среди различных 2D-материалов графен и его производные, несомненно, являются наиболее изученным материалом в биосенсорах [15]. Другой тип 2D-материалов, который широко исследовался в электронике и оптоэлектронике, также демонстрирует достоинства того, что они являются материалами для биоэлектроники. Дихалькогениды переходных металлов (TMD), особенно дисульфид молибдена (MoS 2 ), обладают аналогичными преимуществами большой удельной поверхности, химической инертности и функциональности поверхности. Интеркаляция посторонних ионов или молекул в нанолисты TMD может быть легко достигнута благодаря их уникальной атомной структуре [16]. Важное свойство, которое делает MoS 2 Они выгодно отличаются от других 2D-материалов своей высокой каталитической активностью, обусловленной открытыми краями [13]. Однако недостаток MoS 2 тоже довольно очевидно. По сравнению с графеном, 2D MoS 2 листы имеют гораздо более низкую электропроводность. Перестановка MoS 2 нанолисты дополнительно ограничивают перенос заряда, а также активные реакционные центры.
Незначительные усилия были предприняты в области сенсоров глюкозы, не содержащих ферментов, на основе 2D MoS 2 до самых последних лет. Низкая производительность MoS 2 с электрохимическими устройствами, с которыми хорошо справились с помощью ряда методов, которые успешно решили проблему низкой собственной проводимости. Несколько MoS 2 Сообщалось, что на основе электрохимических биосенсоров глюкозы производительность превосходит их графеновые аналоги [17]. Помимо электрохимических биосенсоров, недавно были изучены недорогие неэлектрохимические методы для 2D MoS 2 , воспользовавшись прогрессом MoS 2 сделано в электронике и оптоэлектронике [18]. В этом обзоре мы суммируем последние достижения MoS 2 . биосенсоры глюкозы. Особое внимание уделяется MoS 2 на основе электрохимических биосенсоров глюкозы, которые описаны в «МоС на основе электрохимических глюкозных биосенсоров 2 Нанокомпозиты ». В разделе «Высокочувствительное определение глюкозы с использованием MoS 2 » Полевые транзисторы », MoS 2 Кратко представлены полевые транзисторы для определения глюкозы. Наконец, выводы и перспективы MoS 2 представлены нанокомпозитные биосенсоры глюкозы.
МоС на основе электрохимического глюкозного биосенсора 2 Нанокомпозиты
В течение нескольких десятилетий металлы или сплавы были основными вариантами катализаторов для прямого электрокаталитического окисления глюкозы [19]. В последнее десятилетие двумерные материалы с большой площадью поверхности, а также уникальными химическими и физическими свойствами открывают новые возможности для многих областей, включая электрохимическое зондирование, накопление энергии и электронику [20]. С точки зрения электрохимического биочувствительности нанокомпозиты из различных 2D материалов и катализаторов демонстрируют явные преимущества перед традиционными катализаторами. Синергетическое сочетание этих материалов, а именно синергетические эффекты, может привести к заметному усилению каталитической активности [21]. Большое количество таких нанокомпозитов, особенно на основе графена или производных графена, было разработано и применено для сенсоров глюкозы, не содержащих ферментов. Многослойный MoS 2 Ожидается, что он будет обладать аналогичными преимуществами, поскольку он разделяет свойства материала графена. В частности, слой MoS 2 нанолисты обладают большим количеством краев, которые, как и листы функционализированного графена, действуют как активные центры для каталитических реакций [22, 23].
Действительно, Хуанг и др. синтезированный MoS 2 наноцветки гидротермальным методом [24]. Стеклоуглеродный электрод, модифицированный MoS 2 наноцветки и композиты хитозан / наночастицы Au показали отчетливое перенапряжение при окислении бисфенола А. Нанокомпозитный сенсор показал эффективное электрокаталитическое окисление бисфенола А, о чем свидетельствует значительно увеличенный ток на циклических вольтамперограммах. Хороший линейный диапазон обнаружения от 0,05 до 100 мкМ достигается для определения бисфенола А. Также оценен предел обнаружения в 5 нМ. Эта работа наглядно продемонстрировала превосходную электрокаталитическую активность и синергетические эффекты Au / MoS 2 нанокомпозиты. Точно так же MoS 2 нанокомпозиты на основе были использованы для определения глюкозы без ферментов. MoS 2 цветы с большой площадью поверхности синтезировали гидротермальным методом с использованием бромида цетилтриметиламмония (ЦТАБ) в качестве ПАВ [25]. Морфологию микроцветов можно контролировать с помощью pH реакционного раствора, концентрации поверхностно-активного вещества CTAB и температуры отжига. MoS 2 Микроцветки, полученные при температуре отжига 500 ° C, показали хорошее кристаллическое качество и, следовательно, улучшенный перенос заряда. Интересно, что электрохимические тесты на определение глюкозы без содержания ферментов показали, что MoS 2 Микроцветковый электрод без какой-либо функционализации может обеспечить высокую чувствительность 570,71 мкА мМ −1 см −2 . Кроме того, датчик показывает широкий линейный диапазон обнаружения до 30 мМ.
Синергетический эффект MoS 2 катализаторы, легированные или гибридизированные инородными металлами, такими как Cu, Ni, Co и Fe, также применимы для усиленного электрохимического катализа глюкозы. Хуанг и др. удалось объединить преимущества как сильной электрокаталитической активности меди по окислению глюкозы, так и большой площади поверхности и активных краевых центров MoS 2 нанолисты [26]. Наночастицы Cu декорировали MoS 2 нанолисты показали электрокаталитическую активность по отношению к окислению глюкозы. Высокая чувствительность 1055 мкА мМ −2 см −2 и линейный диапазон обнаружения до 4 мМ был зарегистрирован для Cu / MoS 2 нанокомпозитный сенсор глюкозы. Чувствительность почти вдвое превышает значение, измеренное с помощью MoS 2 . Микроцветковый электрод. Датчик также продемонстрировал хорошую селективность определения глюкозы по отношению к мочевой кислоте, аскорбиновой кислоте и дофамину. Ток помехи, вызванный этими химическими веществами, составляет всего около 2,1–5,2% от тока глюкозы, и такой низкий уровень тока помехи можно считать незначительным при физиологической концентрации.
Еще один привлекательный кандидат - никель (Ni), который широко изучался на предмет гибридов Ni / графен. Подобно Cu, Ni также является металлом с избытком земли. Редокс-пара Ni 3+ / Ni 2+ обладает впечатляющей каталитической активностью в щелочных средах. Таким образом, Huang et al. использовал MoS 2 нанолист в качестве носителя катализатора для иммобилизации наночастиц Ni [27]. MoS 2 нанолист был синтезирован из MoS 2 порошок в смеси этанол / вода посредством жидкого отшелушивания. Наночастицы Ni были восстановлены на MoS 2 нанолист путем нагревания MoS 2 нанолист - раствор этиленгликоля при 60 ° C в течение 1 ч после добавления NiCl 2 · 6H 2 Прекурсор O и N 2 H 4 · H 2 Растворы O и NaOH. Электрод сенсора глюкозы был приготовлен путем нанесения Ni-MoS 2 гибрид на стеклоуглеродном электроде. Циклическая вольтамперограмма Ni / MoS 2 Гибридно-модифицированный электрод четко показал окисление глюкозы при более высоком токе, чем у модифицированного никелем электрода сравнения. Повышенная электрокаталитическая активность была приписана более активным сайтам на MoS 2 нанолистов, а также уменьшенной агрегации наночастиц Ni на 2D материальной подложке. Амперометрические результаты подтвердили хороший линейный диапазон обнаружения до 4 мМ, высокую чувствительность 1824 мкА мМ -1 см −2 и низкий предел обнаружения 0,31 мкМ при соотношении сигнал / шум 3 (S / N =3). По сравнению с Cu / MoS 2 нанокомпозитный датчик глюкозы, чувствительность может быть улучшена за счет использования Ni / MoS 2 нанокомпозиты. Влияние мешающих видов, включая дофамин, аскорбиновую кислоту и мочевую кислоту, на определение глюкозы также было незначительным. Что еще более важно, датчик показал хорошую воспроизводимость и высокую стабильность. Незначительное снижение чувствительности датчика на 3,4% было измерено после 4 недель хранения при комнатной температуре. Кроме того, Anderson et al. сообщили о высокочувствительном неферментативном биосенсоре глюкозы, включающем наночастицы коллоидного серебра с MoS 2 [28]. Введение наночастиц Ag было направлено на решение проблемы низкой проводимости MoS 2 . . Превосходная чувствительность 9044,6 мкА мМ −1 см −2 и низкий предел обнаружения 0,03 мкМ. Однако диапазон линейного обнаружения составляет всего до 1 мМ.
Электрокаталитическая активность MoS 2 может быть дополнительно улучшен путем гибридизации с графеном. Низкая собственная проводимость MoS 2 подрывает его высокую каталитическую активность. Заряд переносится между MoS 2 наноматериалы медленны в электрохимических реакциях или в общих электронных приложениях. С другой стороны, графен обладает превосходной электропроводностью и может служить незамедлительным решением проблемы медленного транспорта электронов в MoS 2 наноматериалы [29]. Jeong et al. изготовлен трехмерный (3D) MoS 2 Нанокомпозиты / графен-аэрогель однореакторным гидротермальным методом [13]. Хотя повышенная электрокаталитическая активность наблюдалась при использовании трехмерной пористой структуры по сравнению с двумерным эталонным образцом, использование глюкозооксидазы усложнило производство и столкнулось с теми же проблемами, что и ферментативные сенсоры. Geng et al. синтезированный MoS, легированный никелем 2 наночастицы, декорированные на восстановленном оксиде графена (Ni-MoS 2 / rGO) простым и масштабируемым методом [30]. Как показано на рис. 1а, оксид графена, синтезированный методом Хаммерса и Оффемана, был смешан с CH 3 COOH и деионизированная вода. Раствор предшественника Ni-Mo готовили путем добавления (NH 4 ) 2 MoS 4 и Ni (CH 3 COO) 2 · 4H 2 O с различным мольным соотношением в раствор оксида графена. Ni-MoS 2 / rGO получали после центрифугирования и сушки при 80 ° C. Собранный Ni-MoS 2 Затем суспензию rGO прокаливали в течение 4 ч при 600 ° C в N 2 Атмосфера. Полученный Ni-MoS 2 Нанокомпозиты / rGO использовали для неферментативного определения глюкозы. На рисунке 1b показан амперометрический отклик сенсорного электрода, модифицированного Ni-MoS 2 . Нанокомпозиты / rGO с последовательным добавлением раствора глюкозы. После каждого добавления глюкозы наблюдалось явное увеличение силы тока. Кроме того, вставка на рис. 1b показывает, что датчик был способен реагировать на такую низкую концентрацию глюкозы, как 5 мкМ. Полученный сигнал тока как функция концентрации глюкозы показан на рис. 1c, который ясно показывает широкий линейный диапазон обнаружения датчика, 0,005–8,2 мМ, хорошо покрывающий типичный уровень глюкозы в крови человека. Расчетная чувствительность и предел обнаружения составляют 256,6 мкА мМ −1 . см −2 и 2,7 мкМ (S / N =3) соответственно. Хотя чувствительность и предел обнаружения датчика явно ниже, чем у более ранних, линейный диапазон обнаружения значительно улучшен. В работе также сообщалось об улучшении скорости переноса электронов и электрокаталитической активности с коэффициентом диффузии 1,83 × 10 −3 . см 2 s −1 и константы каталитической скорости 6,26 × 10 5 см 3 моль −1 s −1 с помощью Ni-MoS 2 / композиты рГО. Как показано на рис. 1d, когда датчик хранился в сухих условиях, его текущий ответ на 1 мМ глюкозы остается почти неизменным в течение 15 дней, показывая хорошую стабильность. Влияние обычных интерферирующих химических веществ, NaCl, дофамина, мочевой кислоты, аскорбиновой кислоты и V B , также был исследован. Результаты показаны на рис. 1e, и влияние этих химикатов на ток сигнала незначительно. Текущее изменение, вызванное 0,1 мМ NaCl, дофамином, мочевой кислотой, аскорбиновой кислотой и V B , типичная концентрация интерферирующих химических веществ в нормальной сыворотке составляет всего 0,76%, 2,77%, 6,03%, 0%, 2,51% и 0,63% текущего ответа на 2,5 мМ глюкозы. Наконец, работа продемонстрировала хорошее соответствие между концентрациями, измеренными Ni-MoS 2 / rGO и зарегистрированные в больнице значения, демонстрирующие большой потенциал датчиков для практического применения [30].
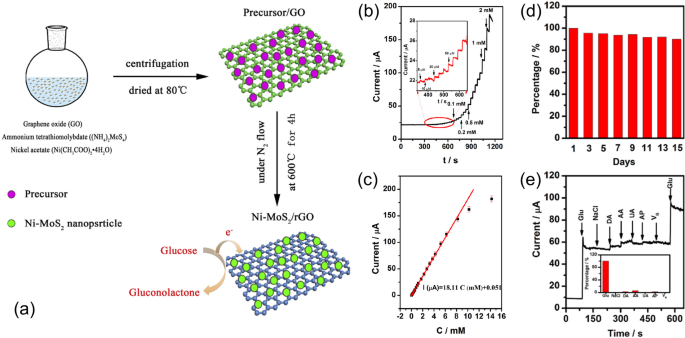
а Схема синтеза Ni-MoS 2 / композиты рГО. б Амперометрический отклик Ni-MoS 2 / rGO для последовательного добавления глюкозы. c Извлеченный ток отклика на различные концентрации глюкозы. г Проверка стабильности датчика амперометрическим измерением в течение 15 дней. е Сравнение амперометрических ответов 2,5 мМ глюкозы и 0,1 мМ интерференционных химикатов. Перепечатано из [25], Copyright 2017, с разрешения Elsevier
Альтернативный способ улучшить передачу заряда в MoS 2 нанокомпозиты должны гибридизоваться с другим высокопроводящим и биосовместимым углеродным материалом, углеродными нанотрубками (УНТ). Между тем, этот способ вполне может ограничить повторную укладку MoS 2 наноматериалы, тем самым обеспечивая более активные реакционные центры. УНТ также широко синтезируются в трехмерных структурах и применяются в накоплении энергии, сборе энергии, зондировании и т. Д. [31,32,33]. Ли и др. подготовили 3D нанокомпозиты из MoS 2 нанолисты гибридизуются с наночастицами оксида кобальта и УНТ [34]. Наночастицы оксида кобальта использовались для повышения электрокаталитической активности, а УНТ - для улучшения проводимости. Однокамерный гидротермальный метод, используемый для синтеза Co-MoS 2 Нанокомпозиты / УНТ кратко показаны на рис. 2а. Смесь УНТ, 0,1 ммоль Co (CH 3 COO) 2 4H 2 O, 1,35 ммоль Na 2 МоО 4 , и 7,5 ммоль l-цистеина переносили в автоклав из нержавеющей стали с тефлоновым покрытием и выдерживали при 180 ° C в течение 24 часов. Затем продукт охлаждали, центрифугировали и промывали деионизированной водой и абсолютным этанолом. Очищенный Co-MoS 2 Нанокомпозиты / УНТ окончательно сушили в вакуумной печи при 60 ° C в течение 6 ч. Сканирующая электронная микроскопия (SEM) и просвечивающая электронная микроскопия (TEM) изображения Co-MoS 2 / Нанокомпозиты УНТ показаны на рис. 2б, в. Наблюдались типичные трехмерные связанные УНТ диаметром около 20 нм. На изображении ПЭМ четко видны полые УНТ, прикрепленные к MoS 2 нанолисты. Такая структура служит высокопроводящей матрицей для поддержки MoS 2 нанолистов и иммобилизовать наночастицы Co. Такой плотно упакованный Co-MoS 2 / Нанокомпозиты УНТ не только обеспечивают хорошее количество каталитических активных краев, но также обеспечивают эффективный перенос заряда во время реакций. Что еще более важно, плотно упакованный Co-MoS 2 / Структура УНТ и достаточно большое расстояние между слоями 0,65 нм для MoS 2 (больше, чем 0,34 нм для УНТ) эффективно подавляют повторную укладку MoS 2 / УНТ композит. Типичные циклические вольтамперометрические и амперометрические измерения были выполнены для проверки характеристик безферментного сенсора, изготовленного из Co-MoS 2 / Нанокомпозиты УНТ. Амперометрические характеристики Co-MoS 2 Измерение чувствительного электрода / CNT (при 0,65 В по сравнению с Ag / AgCl) с последовательным добавлением глюкозы показано на рис. 2d. Наблюдали отчетливое ступенчатое увеличение тока ответа на добавление глюкозы. Хороший линейный диапазон обнаружения был достигнут до 5,2 мМ, как показано на рис. 2e. Расчетная чувствительность составляет 131,69 мкА мМ −1 . см −2 . Несмотря на относительно низкую чувствительность, на рис. 2f был получен чрезвычайно низкий предел обнаружения 80 нМ (S / N =3).
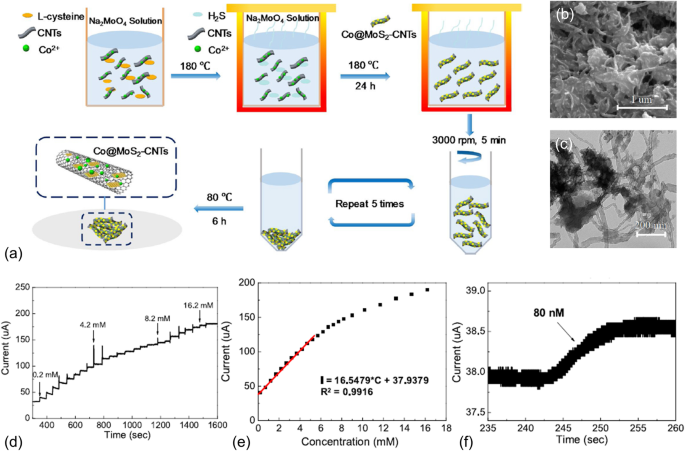
а Принципиальная схема гидротермальной сборки Co-MoS2 / CNT. б SEM и c ПЭМ-изображения синтезированных Co-MoS2 / УНТ. г Амперометрические характеристики Co-MoS 2 / Датчик CNT для последовательного добавления глюкозы. е Извлеченный ток отклика на различные концентрации глюкозы. е Амперометрическая кривая Co-MoS 2 / Датчик CNT до 80 нМ глюкозы. Перепечатано из [29], Copyright 2019, с разрешения Elsevier
Подобно синергетическим эффектам, проявляемым гибридами металл-2D материалов, биметаллические сплавы и наноструктуры также показали улучшенные каталитические характеристики и показали хороший потенциал для многих приложений, включая зондирование [35], сбор энергии [36, 37] и т. Д. Li et al. . недавно синтезировали биметаллические наночастицы Au-Pd для неферментативного определения перекиси водорода и глюкозы [5]. Изготовление Au-Pd / MoS 2 электрод датчика показан на рис. 3а. MoS 2 нанолисты были приготовлены методом жидкого отшелушивания. Биметаллические наночастицы Au-Pd были синтезированы методом химического восстановления. Подготовленный Au-Pd / MoS 2 Затем нанокомпозиты были нанесены на стеклоуглеродный электрод для химического анализа. Как показано на рис. 3b, при последовательном добавлении глюкозы наблюдались хорошие скачки тока. Диапазон линейного обнаружения, измеренный как 0,5–20 мМ, значительно превышает нормальный уровень глюкозы в крови человека (рис. 3c). Вместо использования обычных биметаллических наночастиц, которые часто изготавливают из дорогих металлов, Ma et al. разработали наночастицу золота и полипиррол (PPY), совместно декорированную MoS 2 нанокомпозит [38]. Ожидается, что гибриды металл / проводящий полимер улучшат площадь поверхности и проводимость сенсорного электрода. Более того, использование проводящих полимеров может дополнительно снизить стоимость электрохимических датчиков. Изготовленный MoS 2 -PPY-Au / стеклоуглеродный электрод показал невероятно низкий уровень обнаружения 0,08 нМ, почти полную селективность и длительную стабильность в течение 3 недель. Однако чувствительность сенсора составляет всего 37,35 мкА · мкМ –1 . · См –2 и диапазон обнаружения довольно ограничен (0,1–80 нМ).
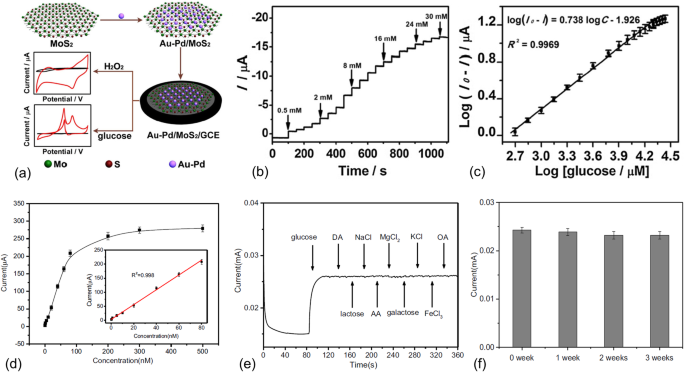
а Иллюстрация синтеза Au-Pd / MoS 2 нанокомпозиты и сборка на стеклоуглеродном электроде для неферментативного электрохимического определения H 2 О 2 и глюкоза. б Амперометрические характеристики Au-Pd / MoS 2 нанокомпозитный сенсор на последовательное добавление глюкозы. c Извлеченный ток отклика на различные концентрации глюкозы. Перепечатано из [5], Copyright 2017, с разрешения Elsevier
Помимо металлов, оксиды металлов с высокой каталитической активностью также пытались улучшить электрохимический катализ. Помимо высокой электрокаталитической активности, низкая стоимость оксидов металлов является еще одним преимуществом, которое нельзя переоценить для дешевых электрохимических датчиков. Среди различных оксидов металлов Cu 2 Наноматериалы O с различной морфологией перспективны для катализа в различных приложениях. Fang et al. были изучены MoS 2 украшен медью 2 Наночастицы O для неферментативного определения глюкозы [39]. Амперометрические измерения Cu 2 O / MoS 2 гибридно-модифицированный электрод показывает хороший линейный диапазон от 0,01 до 4 мМ. Извлеченный предел обнаружения составляет около 1 мкМ. Чувствительность составила 3108,87 мкА мМ -1 . см −2 , что выше, чем у большинства MoS 2 неферментные датчики глюкозы. Результаты также указывают на хороший потенциал оксидов металлов для недорогих неферментных сенсоров глюкозы. Сравнение безферментных биосенсоров глюкозы на основе MoS 2 нанокомпозиты представлены в таблице 1.
Высокочувствительное определение уровня глюкозы с использованием MoS 2 Полевые транзисторы
MoS 2 полевые транзисторы (FET) обладают рядом преимуществ, таких как высокий коэффициент коммутируемого тока, низкий ток утечки, небольшой подпороговый размах и высокая подвижность [41, 42]. Благодаря отличным электронным свойствам и механической прочности MoS 2 Транзисторы перспективны для низкоэнергетической, недорогой и носимой электроники [43, 44]. Биосенсоры, фотодетекторы, газовые сенсоры и их гибкие аналоги на основе MoS 2 о транзисторах недавно сообщалось [45]. Преимущества MoS 2 транзисторы делают эти датчики высокочувствительными, низко потребляемыми, портативными и т. д. MoS 2 Сообщается, что полевые транзисторы представляют собой различные датчики влажности, H 2 О 2 , НЕТ, НЕТ 2 , NH 3 , ДНК и др. [46,47,48,49]. Shan et al. сообщил о первом MoS 2 полевой транзистор для определения глюкозы [40]. Как показано на рис. 4a, обратный шлюз MoS 2 Полевой транзистор был изготовлен на SiO 2 . / Si подложка. Образцы электродов истока и стока были сформированы методами фотолитографии и электронно-лучевой литографии. Контакты Au / Ni (70 нм / 10 нм) наносились напылением. Следует отметить, что MoS 2 материал канала размером примерно 2 мкм × 3 мкм был механически расслоен и перенесен на предварительно сформированные электроды, как показано на фиг. 4b. Изготовленный транзистор был помещен в образец ячейки и испытан.
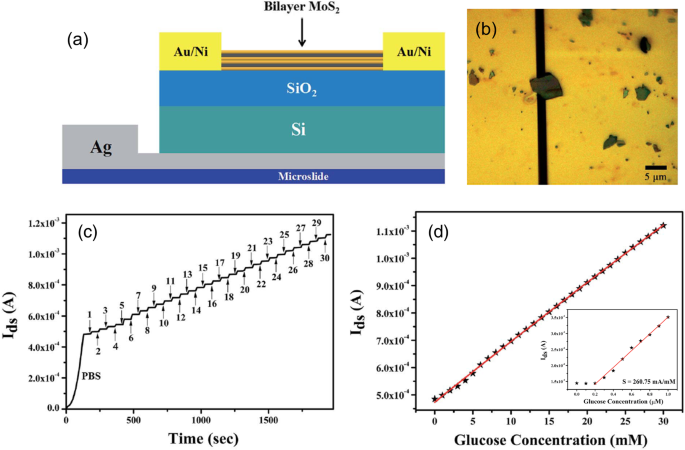
а Схема обратного стробирования MoS 2 транзистор. б Изображение MoS 2 с оптической микроскопии материал канала между электродами истока и стока. c Текущие реакции в реальном времени на различные концентрации глюкозы. г Ток отклика I ds МОС 2 FET как функция концентрации глюкозы от 0 до 30 мМ. На вставке показан ответный ток, извлеченный для более низких концентраций глюкозы, от 0 до 1,0 мкМ. Перепечатано под CC BY-NC 3.0 из [44]
Измеренный I ds - V ds Кривые с разными концентрациями растворов глюкозы четко показали увеличение тока сток-сток с увеличением концентрации глюкозы. Следует отметить, что GO x фермент был добавлен до концентрации глюкозы. Следовательно, зондирование не является полностью свободным от ферментов. Повышенный ток в канале при увеличении концентрации глюкозы был приписан ферментативному окислению глюкозы. Электроны, образовавшиеся в результате реакции, были перенесены в MoS 2 n-типа. канал и, следовательно, увеличил его проводимость. Чтобы проиллюстрировать реакцию сенсора на глюкозу, в реальном времени I ds измерение проводилось с последовательным добавлением разных концентраций глюкозы, как показано на фиг. 4c. Измерения начинались с чистого раствора PBS, а раствор с более высокой концентрацией и на 1 мМ больше глюкозы помещали в предыдущий каждую минуту. Реакция тока сток-исток на различные концентрации глюкозы представлена на рис. 4d. Ясно, что MoS 2 Датчик FET показывает очень большой линейный диапазон для определения глюкозы, до 30 мМ. Тесты были повторены для низкой концентрации растворов глюкозы для проверки предела обнаружения и чувствительности MoS 2 Датчик на полевом транзисторе. Как показано на вставке к рис. 4d, датчик может четко определять присутствие глюкозы с концентрацией всего 300 нМ. Чувствительность MoS 2 Биосенсор глюкозы FET рассчитан как 260,75 мА мМ -1 . Помимо высокой чувствительности и низких пределов обнаружения, устройство также показало высокую стабильность до 45 дней. Однако текущее устройство должно включать добавление GO x фермент в тестируемом растворе глюкозы, что делает его менее практичным для портативных приложений.
Заключение и перспективы
В этом мини-обзоре представлены недавние усилия по разработке безферментного биосенсора MoS 2 нанокомпозиты. Во всех этих публикациях представлены простые и недорогие средства создания высокопроизводительных сенсоров глюкозы с точки зрения чувствительности, линейного диапазона и предела обнаружения. Эти исследования, несомненно, открывают новые возможности для недорогих и чувствительных сенсоров глюкозы. Достижения во многом зависят от недавнего прогресса, достигнутого в синтезе новых нанокомпозитов из 2D-материалов, металлических наноматериалов и наночастиц каталитического оксида. Можно ожидать, что в этом направлении будут вложены больше усилий, а накопленный опыт очень полезен для будущих исследований соответствующих материалов для сенсорных приложений.
Однако в то же время следует понимать, что для клинического или любого другого практического применения требуется еще много усилий. Стабильность и воспроизводимость этих устройств еще предстоит улучшить. До сих пор использовались либо ограниченное время хранения, либо в сухих условиях. Во-вторых, методы химического синтеза просты и дешевы, но остается неясным, можно ли масштабировать методы. Новые методы, такие как струйная печать, могут быть использованы для воспроизводимого крупномасштабного изготовления датчиков. Хотя MoS 2 Электрохимические датчики на основе демонстрируют конкурентоспособные характеристики по сравнению с аналогами на основе углеродных материалов, преимущества, например, краевые каталитические участки MoS 2 , не существенны. Очевидно, что есть много возможностей по-настоящему воспользоваться уникальными свойствами MoS 2 для дальнейшего улучшения неферментативного определения глюкозы. Кроме того, разработка гибкого MoS 2 на основе биосенсора глюкозы нанокомпозиты важны для гибкости восприятия в здравоохранении и должны быть более конкурентоспособными на рынке, который, несомненно, станет центром исследований в будущем.
Наконец, MoS 2 Датчики на основе полевых транзисторов показывают отличные характеристики при измерении уровня глюкозы. Учитывая недавнюю разработку MoS 2 Полевые транзисторы, это направление кажется очень перспективным при разработке недорогих сенсоров глюкозы и других типов химических сенсоров. Следует отметить, что текущая работа, представленная на MoS 2 Датчики глюкозы FET работали только на GO x -допированный раствор глюкозы. В будущей работе необходимо найти альтернативы, позволяющие избежать использования GO x для более практичного развертывания MoS 2 Датчики глюкозы FET.
Доступность данных и материалов
Не применимо.
Сокращения
- 2D:
-
Двумерный
- 3D:
-
Трехмерный
- CNT:
-
Углеродные нанотрубки
- CTAB:
-
Бромид цетилтриметиламмония
- полевые транзисторы:
-
Полевые транзисторы
- GO x :
-
Глюкозооксидаза
- Инициалы:
-
Полное имя
- MoS 2 :
-
Дисульфид молибдена
- Ни:
-
Никель
- SEM:
-
Сканирующая электронная микроскопия
- ТЕМ:
-
Просвечивающая электронная микроскопия
- TMD:
-
Дихалькогениды переходных металлов
Наноматериалы
- Нанографема, гибкая прозрачная память на основе кремния
- Обзор применения биосенсоров и наносенсоров в агроэкосистемах
- Видимые световые фотокаталитические характеристики нанокомпозитов ZnO / g-C3N4, легированных азотом
- Зависящая от смещения фоточувствительность многослойных фототранзисторов MoS2
- Плазмонный датчик на основе диэлектрических нанопризм
- Чувствительное неферментативное электрохимическое определение глюкозы на основе полого пористого NiO
- Оценка накопления энергии суперконденсатором на основе дробно-дифференциальных уравнений
- Высокопроизводительный автономный УФ-детектор на основе массивов наночастиц SnO2-TiO2
- Суперконденсатор на основе оксида марганца
- Понимание конфигурации двигателя



