Управление температурой серы для синтеза наносферной пленки α-NiS для длительного хранения неферментативных сенсоров глюкозы
Аннотация
В этом исследовании наносферные пленки альфа-сульфида никеля (α-NiS) были успешно синтезированы путем гальванического осаждения пленки нанолиста никеля на стеклянной подложке из оксида индия и олова (ITO) и сульфидирования покрытой никелем стеклянной подложки ITO. Сначала мы электроосаждали пленки нанолистов никеля на стеклянные подложки ITO, которые были разрезаны на 0,5 × 1 см 2 размер. Во-вторых, нанолистовые никелевые пленки отжигались в запаянных под вакуумом стеклянных ампулах с листами серы при различных температурах отжига (300, 400 и 500 ° C) в течение 4 ч в запаянных под вакуумом стеклянных ампулах. Пленки α-NiS были исследованы с помощью дифракции рентгеновских лучей (XRD), сканирующей электронной микроскопии в вакууме (VVSEM), автоэмиссионной сканирующей электронной микроскопии / энергодисперсионного спектрометра (FE-SEM / EDS), циклической вольтамперограммы (CV), электрохимической микроскопии. спектроскопия импеданса (EIS), спектры ультрафиолетового / видимого / ближнего инфракрасного (УФ / видимого / ближнего инфракрасного) диапазона и спектры фотолюминесценции (PL). Многие наносферы наблюдались на поверхности пленок α-NiS при температуре отжига 400 ° C в течение 4 часов. Мы также использовали просвечивающую электронную микроскопию высокого разрешения (HR-TEM) для анализа наносфер α-NiS. Мы продемонстрировали, что наша пленка наносфер α-NiS имеет линейный отклик тока на различные концентрации глюкозы. Кроме того, наши пленки наносфер α-NiS хранились при комнатной температуре в течение пяти с половиной лет и по-прежнему использовались для обнаружения глюкозы в низкой концентрации.
Фон
За последнее десятилетие сульфид никеля (NiS) был признан обладающим хорошей проводимостью. Его можно плавить как катодный материал для литиевых аккумуляторных батарей [1,2,3]. Кроме того, NiS применялся для накопления солнечной энергии [4, 5]. Было также доказано, что он имеет отличные свойства для применения в фотокатализаторах [6, 7]. Пленка NiS также может быть использована для неферментативного сенсора глюкозы [8, 9]. Что касается обнаружения глюкозы, было разработано множество методов определения глюкозы. К наиболее широко используемым и исторически значимым методам относились йодометрия меди, высокоэффективная жидкостная хроматография (ВЭЖХ), глюкозооксидаза (ГХ), капиллярный зональный электрофорез (CZE) и неферментативный сенсор глюкозы [10]. Неферментный датчик глюкозы будет важным приложением для определения глюкозы в будущем [11]. Мы заинтересованы в синтезе пленки NiS и исследуем этот вид материала для одного из важных применений неферментативного сенсора глюкозы. В исследовании сохранения сенсора неферментативный сенсор глюкозы может хранить больше времени, чем ферментативный сенсор глюкозы [12]. В этой статье мы опишем процесс синтеза пленки α-NiS и продемонстрируем наши образцы, которые могут быть использованы для определения глюкозы с помощью измерений циклической вольтамперограммы (CV) и амперометрии. Мы также обнаружили, что не было сообщений о хранении неферментативных сенсоров глюкозы при комнатной температуре в течение пяти с половиной лет. В этой статье мы продемонстрировали, что наши пленки наносфер α-NiS хранились при комнатной температуре в нашей лаборатории в течение пяти с половиной лет и все еще были полезны для обнаружения глюкозы в различных концентрациях в различных растворах (0,1 М NaOH и буфер Кребса).
Методы
Подготовка пленок α-NiS
Для изготовления пленки α-NiS условием синтеза был двухэтапный процесс:первым этапом было изготовление пленки нанолиста никеля [13, 14], а вторым этапом был процесс синтеза пленки α-NiS с помощью метод физического переноса паров (PVT) для сульфуризации пленки нанолистового никеля [15, 16]. На первом этапе пленка нанолиста никеля была синтезирована с помощью простого метода электроосаждения. Мы использовали плоский анод Pt и стеклянный катод из оксида индия и олова (ITO), обработанный в процессе катодного электроосаждения, для изготовления пленки нанолиста никеля. Пленки никеля были электроосаждены на проводящие стеклянные подложки, покрытые ITO, которые были разрезаны на 0,5 × 1 см 2 размер. Каждый из них имел сопротивление <15 Ом / см 2 . . 0,1 М гексагидрат сульфата никеля (NiSO 4 .6H 2 O, Sigma-Aldrich, ≥ 98,5%) и 0,05 М гидроксид натрия (NaOH, SHOWA, 96%) использовали для приготовления раствора предшественника в бидистиллированной воде. Пленку наплавленного никеля использовали в потенциостатическом режиме. Мы устанавливаем потенциал электроосаждения на уровне 3,0 В постоянного тока с помощью раствора с pH 7,7. Пленки никеля высокого качества подвергали электроосаждению при 40 ° C в течение 10 мин. После получения никелевых пленок нанолистовые пленки никеля отжигались в запаянных под вакуумом стеклянных ампулах с листами серы. Пленки α-NiS отжигались при различных температурах отжига (300, 400 и 500 ° C) в течение 4 ч. Мы хотим подтвердить оптимальную продолжительность отжига, и мы отожгли пленки α-NiS при температуре отжига 400 ° C в течение разного времени (3 и 6 часов).
Характеристика пленки α-NiS
Морфология пленок α-NiS была охарактеризована с помощью XRD (SHIMADZU XRD-6000) с использованием излучения Cu Kα, сканирующей электронной микроскопии в переменном вакууме (VVSEM) (HITACHI S-3000N) и FE-SEM / EDS (HITACHI S-4800). при 3,0 кВ. Электрохимические свойства пленок α-NiS измеряли с помощью измерений CV и амперометрии с электродом сравнения Ag / AgCl с помощью потенциостата (Jiehan, ECW-5000) в трехэлектродной конфигурации. Пленку α-NiS оценивали с помощью CV-измерений и амперометрии в 15 мл раствора 0,1 М NaOH с различными концентрациями глюкозы. Измерения импеданса пленок α-NiS были оценены с помощью спектроскопии электрохимического импеданса (EIS) (Zennium IM6) в 0,1 М KCl, содержащем 1,5 мМ Fe (CN) 6 3– / 4– . Пленку α-NiS оценивали с помощью измерений CV и амперометрии в буфере Кребса (115 мМ NaCl, 2 мМ KCl, 25 мМ NaHCO 3 , 1 мМ MgCl 2 , 2 мМ CaCl 2 0,25% бычий сывороточный альбумин [pH 7,4]; уравновешен 5% CO 2 ) [17]. Спектры поглощения пленок α-NiS измеряли с помощью спектрофотометра УФ / видимого / ближнего ИК-диапазона (HITACHI U-3501) после диспергирования пленок α-NiS в дистиллированной воде с использованием сверхзвукового диспергатора. Спектры фотолюминесценции (ФЛ) получали на флуоресцентном спектрометре (RF-5301PC) с ксеноновым лазером при комнатной температуре. Наконец, кристаллическая структура наносфер α-NiS была исследована с помощью системы HR-TEM (JEOL TEM-2010 HR-TEM).
Результаты и обсуждение
Пленки нанолистов никеля были получены методом электроосаждения. Мы устанавливаем электроосаждение на постоянном токе с потенциалом 3,0 В постоянного тока и 4,0 В постоянного тока. Мы выдерживали гальванический раствор при 40 ° C в течение 10 мин и наблюдали за электроосаждением никелевой пленки на стеклянной подложке ITO. На рис. 1 представлены результаты электроосаждения пленок никеля. Как видно на рис. 1a, b, наблюдаемая поверхность пленки нанолиста никеля имела средний размер зерна 0,01–0,3 мкм при потенциале осаждения 3,0 В постоянного тока. Поперечное сечение пленки нанолиста никеля толщиной примерно 500 нм показано на вставке к рис. 1б. Было обнаружено, что на поверхности никелевой пленки средний размер зерна составлял 0,5–1,0 мкм при потенциале осаждения 4,0 В постоянного тока. На рис. 1г показаны рентгенограммы никелевых пленок. Пики дифракции, соответствующие картинам XRD для различных пленок никеля, были подтверждены сравнением с картой Объединенного комитета по порошковым стандартам дифракции (JCPDS870712). Таким образом, мы подтвердили, что конечными продуктами были пленки никеля, когда они наблюдались на стеклянной подложке ITO.
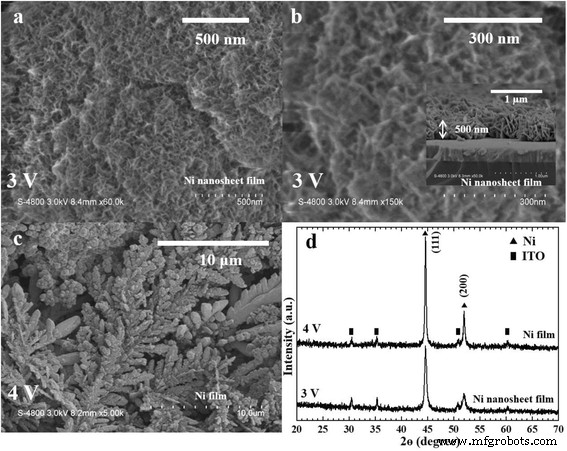
FE-SEM изображения пленок никеля. а , b Пленка никелевого нанолиста, вид сверху, была электроосаждена при 3,0 В постоянного тока. На вставке:поперечное сечение пленки нанолиста никеля. c Пленка никеля, вид сверху, была электроосаждена при 4,0 В постоянного тока. г Рентгенограммы никелевых пленок были электроосаждены при различных потенциалах (3,0 и 4,0 В постоянного тока)
Мы посчитали, что пленка нанолиста никеля лучше, чем пленка никеля, для проявления наноструктуры пленки α-NiS. В наших экспериментах по получению пленок нано-NiS мы сульфировали никелевые нанолистовые пленки. После отжига никелевых пленок в вакуумных стеклянных ампулах были получены пленки α-NiS. На рисунке 2 показаны результаты контроля различных температур сульфуризации для синтеза пленок α-NiS. На рис. 2а рентгенограммы показали, что три пленки α-NiS были синтезированы при трех различных температурах отжига (300, 400 и 500 ° C). На рентгенограмме каждого образца мы наблюдали, что дифракционные пики от различных пленок α-NiS находятся в одной и той же фазе. Пики дифракции, соответствующие дифрактограммам пленок α-NiS, были подтверждены сравнением с картами Объединенного комитета по порошковым стандартам дифракции (JCPDS750613). Таким образом, мы подтвердили, что конечными продуктами были пленки α-NiS. На рис. 2b – d показаны различные морфологии пленок α-NiS при трех различных температурах отжига (300, 400 и 500 ° C) в течение 4 часов. Результаты EDS пленок α-NiS с массовыми процентными содержаниями (мас.%) Элементов серы (S) и никеля (Ni) показаны на вставках к рис. 2b – d. На рис. 2б видны частицы неправильной формы на поверхности пленки α-NiS при температуре отжига 300 ° C. Мы наблюдали частицы размером примерно 0,5–2 мкм на рис. 2б. Результат EDS пленки α-NiS при температуре отжига 300 ° C, 34,99 мас.% S и 65,01 мас.% Ni с молярным соотношением 0,99 (S / Ni) показан на вставке к рис. 2b. Мы наблюдали сферические частицы и пористую структуру α-NiS с приблизительным средним размером 0,1–0,2 мкм на поверхности пленки α-NiS при температуре отжига 400 ° C на рис. 2в. Результат EDS пленки α-NiS при температуре отжига 400 ° C, 35,75 мас.% S и 64,25 мас.% Ni с молярным соотношением 1,02 (S / Ni) показан на вставке к рис. 2c. Мы также наблюдали цепочечные частицы α-NiS с приблизительным средним размером 1–5 мкм на поверхности пленки α-NiS при температуре сульфуризации 500 ° C на рис. 2d. Результат EDS пленки α-NiS при температуре отжига 500 ° C, 36,22 мас.% S и 63,22 мас.% Ni с молярным соотношением 1,04 (S / Ni) показан на вставке к рис. 2c. Мы наблюдали, что морфология (частицы неправильной формы, наносферы и цепочечные частицы) поверхности образцов изменялась при различных температурах отжига (300, 400 и 500 ° C). В целом мы наблюдали разную эволюцию роста и формирование наноструктур при разных температурах отжига. Исследователи (Denholme et al.) Также представили, что температура влияет на кинетику роста NiS 2 Пленки контролировали различную морфологию по температурному параметру в системе Ni-S [15]. Это произошло из-за давления паров S. Точно так же было обосновано, что пары S участвуют в реакциях через механизмы пар-твердое тело или пар-жидкость-твердое тело на поверхности металлического Ni в парах S и в реакциях переноса Ni. Таким образом, реакция проводилась в закрытой системе и зависела от давления паров реагентов. Давление пара зависело от температуры реакции и стехиометрического соотношения реагентов. Мы думали, что различные морфологии NiS значительно увеличиваются в давлении паров S с повышением температуры с различным увеличением скорости реакции Ni и S.
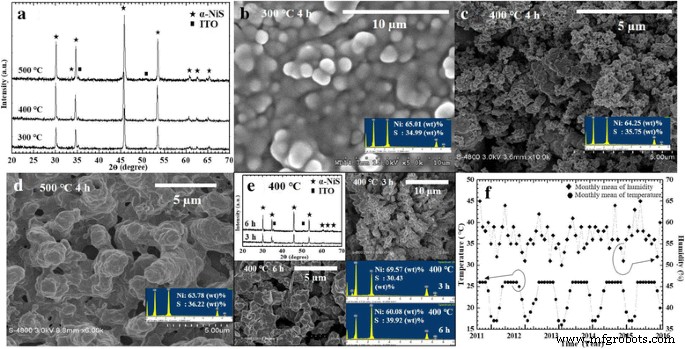
а На рентгенограмме показаны пленки наносфер α-NiS при различных температурах отжига (300, 400 и 500 ° C). Изображение вида сверху пленок α-NiS было отожжено при b . 300, c 400 и d 500 ° C в течение 4 ч. Вставка:спектры EDS были на вставке b - г . е Изображения показали, что рентгенограммы (вверху слева), изображения FE-SEM (вверху справа, 3 часа; внизу слева, 6 часов) и спектры EDS (внизу справа) пленок α-NiS при разном времени отжига (3 и 6 часов). час). е Кривые показали запись об измерениях температуры и влажности в нашей лаборатории для проверки условий сохранения
Мы также хотим подтвердить оптимальную продолжительность отжига. Остальные времена (3 и 6 ч) пленки α-NiS отжигали при 400 ° C. Результаты показаны на рис. 2д. Мы заметили, что дифрактограммы различных пленок α-NiS находились в одной фазе и были подтверждены картами JCPDS750613 на вставке (вверху слева) на рис. 2e. Мы наблюдали частицы размером примерно 0,5–1 мкм на поверхности пленки α-NiS при температуре сульфирования 400 ° C в течение 3 ч на вставке (вверху справа) рис. 2e. На вставке показан результат EDS пленки α-NiS при температуре отжига 400 ° C, 30,43 мас.% S и 69,57 мас.% Ni в течение 3 ч с молярным соотношением 0,8 (S / Ni). (справа внизу) на рис. 2e. Мы наблюдали частицы размером примерно 0,5–2 мкм на поверхности пленки α-NiS при температуре сульфирования 400 ° C в течение 6 часов на вставке (внизу слева) на рис. 2e. На вставке показан результат EDS пленки α-NiS при температуре отжига 400 ° C, 39,92 мас.% S и 60,08 мас.% Ni в течение 6 ч с молярным соотношением 1,21 (S / Ni). (справа внизу) на рис. 2e. Как видно на вставке (результат EDS) на рис. 2c, он показал, что не было избытка или недостатка S для 4-часового образца, что было близко к стехиометрическому отношению 1 (S / Ni). Наконец, СЭМ-изображение на рис. 2с с большим количеством наносфер на поверхности пленки α-NiS для времени отжига 4 часа сравнивалось с двумя СЭМ-изображениями для разного времени отжига (3 и 6 часов) с более крупными частицами на вставках (вверху справа и снизу слева) на рис. 2д. Мы подтвердили, что оптимальная продолжительность отжига составляет 4 часа.
После синтеза наносферных пленок α-NiS мы поместили часть наносферных пленок α-NiS в небольшие пластиковые контейнеры с пластиковыми крышками в нашей лаборатории с кондиционированием воздуха на пять с половиной лет. Время испытания на консервацию наших пленок наносфер α-NiS было с 1 августа 2011 г. по 31 декабря 2016 г. Как видно на рис. 2f, кривые показывают температуру (16–26 ° C) и относительную влажность (50–65%). ), которые были записаны в нашей лаборатории для теста на консервацию с 1 августа 2011 года по 31 декабря 2016 года. После завершения теста на консервацию мы хотели подтвердить с помощью CV-измерений и амперометрии пленки наносфер α-NiS, которые все еще имели текущие отклики при различных концентрациях глюкозы. в растворе в январе 2017 года. Мы провели обзор некоторых работ об измерении электрохимического поведения образца NiS для неферментативного сенсора глюкозы. Многие исследователи измеряли образцы с помощью CV-измерений и амперометрии в 0,1 М растворе NaOH, потому что они легко сравнивали результаты в тех же условиях [8,9,10,11,12]. На рис. 3 показаны характеристики CV и амперометрии пленок α-NiS. Относительно площади рабочего электрода 0,2 × 0,5 см 2 для обнаружения глюкозы на поверхности пленки наносфер α-NiS во всех экспериментах. Окислительно-восстановительная (окислительно-восстановительная) реакция пленок α-NiS оценивалась методом CV с помощью электрода сравнения Ag / AgCl с потенциостатом. CV-характеристики пленок α-NiS сканировали в диапазоне от 0 до 0,8 В за 1 цикл с помощью потенциостата. Образцы были измерены в трехэлектродной конфигурации при скорости сканирования 20 мВс -1 . . Что касается концентрации NaOH, мы выбрали 0,1 M для раствора, потому что мы видели следующую формулу (1), что чем больше OH - анионов у нас было, тем больше е - анионы в растворе [8].
$$ \ mathrm {NiS} + {\ mathrm {OH}} ^ {-} \ leftrightarrow \ mathrm {NiS} \ mathrm {OH} + {\ mathrm {e}} ^ {-} $$ (1) <рисунок>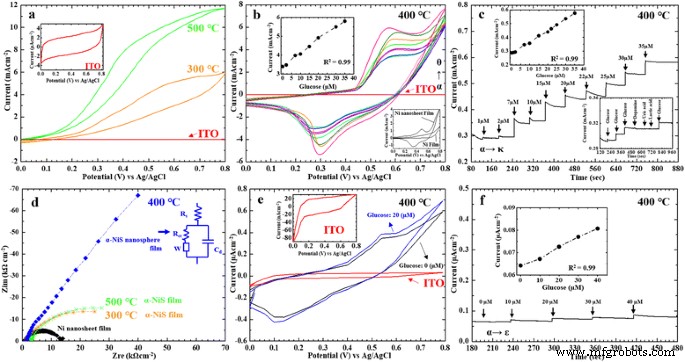
а Три CV на изображении:красная кривая показывает CV чистого ITO; оранжевая и зеленая кривые - ЦВА пленок α-NiS при различных температурах отжига (300 и 500 ° C). Врезка:CV голого ITO / стекла. б CV нано-NiS / ITO в 0,1 М NaOH с разными концентрациями глюкозы:(α) 0 мкМ, (β) 2 мкМ, (γ) 7 мкМ, (δ) 10 мкМ, (ε) 15 мкМ, (ζ) 20 мкМ, (η) 30 мкМ и (θ) 35 мкМ. Вставка:вверху слева - график зависимости тока пика окисления от концентрации глюкозы; внизу - ЦВА пленки Ni и пленки нанолиста Ni. c Пленку наносфер α-NiS оценивали амперометрическим методом в 0,1 М NaOH с различными концентрациями глюкозы:(α) 1 мкМ, (β) 2 мкМ, (γ) 7 мкМ, (δ) 10 мкМ, (ε) 15 мкМ, (ζ) 20 мкМ, (η) 22 мкМ, (θ) 25 мкМ, (ι) 30 мкМ и (κ) 35 мкМ. Вставка:вверху слева - график зависимости текущих ответов от концентраций глюкозы; внизу - хроноамперометрический отклик NiS / ITO в 0,1 М NaOH с 2 мкМ глюкозы и в присутствии 2 мкМ дофамина, мочевой кислоты и молочной кислоты при приложенном потенциале 0,6 В постоянного тока. г Графики Найквиста для пленки нанолиста никеля, пленки наносфер α-NiS и пленок α-NiS при разной температуре отжига (300 и 500 ° C) в 0,1 M KCl, содержащем 1,5 мМ Fe (CN) 6 3– / 4– . е CV нано-NiS / ITO в Кребсе с разными концентрациями глюкозы:(α) 0 мкМ и (β) 20 мкМ. Врезка:вверху слева - резюме чистого ITO / стекла. е Пленку наносфер α-NiS оценивали амперометрическим методом в буфере Кребса с различными концентрациями глюкозы:(α) 0 мкМ, (β) 10 мкМ, (γ) 20 мкМ, (δ) 30 мкМ и (ε) 40 мкМ. Вставка:вверху - график зависимости текущих ответов от концентрации глюкозы
Согласно приведенной выше формуле (1) мы посчитали, что чем больше e - анионов мы имели в растворе, большее значение тока показало в потенциостате. На рис. 3а представлены три кривые. Красная CV-кривая голого ITO показана на вставке к рис. 3а. Оранжевая и зеленая CV-кривые представляют собой окислительно-восстановительную реакцию пленок α-NiS при различных температурах отжига (300 и 500 ° C). Мы наблюдали, что кривые CV не имели отрицательных потенциалов восстановления на рис. 3а. Мы также обнаружили, что две пленки α-NiS не реагируют по току на разные концентрации глюкозы. Как видно на рис. 3b, он показал, что пленка наносферы α-NiS оценивалась путем измерения CV в растворе 0,1 М NaOH с различными концентрациями глюкозы (2, 7, 10, 15, 20, 30 и 35 мкМ) при температуре скорость сканирования 20 мВс −1 . Очевидно, мы видели окислительно-восстановительный потенциал пленки наносферы α-NiS на рис. 3б. Аналогичные окислительно-восстановительные кривые пленки нано-NiS были обнаружены в другой работе [8]. Исследователи (Padmanathan et al. 2015) сообщили, что механизм реакции объясняется двумя уравнениями окислительно-восстановительного потенциала. (2) и (3) об обнаружении глюкозы пленки нано-NiS. Два уравнения показаны ниже [8]:
$$ {\ mathrm {Ni}} ^ {\ mathrm {II}} \ to {\ mathrm {Ni}} ^ {\ mathrm {II} \ mathrm {I}} + {\ mathrm {e}} ^ {- } $$ (2) $$ {\ mathrm {Ni}} ^ {\ mathrm {II} \ mathrm {I}} + \ mathrm {глюкоза} \ to {\ mathrm {Ni}} ^ {\ mathrm {II} } + \ mathrm {глюконолактон} $$ (3)Как видно на рис. 3b, разные значения тока пиков окисления, очевидно, изменились при 0,6 В. Мы наблюдали, что пунктирная линия имела линейную зависимость относительно различных токовых откликов пиков окисления против различных концентраций глюкозы на вставке (слева) на фиг. 3b. Кривые CV для пленки нанолиста никеля и пленки никеля также показаны на вставке (внизу) к рис. 3b. Токовые характеристики кривой CV для пленки нанолиста никеля были больше, чем у пленки Ni, от 0 до 0,8 В на вставке (внизу) на рис. 3b. Мы посчитали, что использовали пленку нанолиста никеля в качестве прекурсора в процессе синтеза наносферной пленки α-NiS, и у нас было больше возможностей для получения больших токовых откликов на кривой CV. На рисунке 3c показано, что разные токовые характеристики пленки наносферы α-NiS предназначены для обнаружения глюкозы в различных концентрациях (1, 2, 7, 10, 15, 20, 22, 25, 30 и 35 мкМ) с помощью амперометрии. Мы наблюдали различные текущие отклики концентраций глюкозы от 1 до 35 мкМ с линейной зависимостью, имеющей коэффициент корреляции 0,99 на вставке (слева) на фиг. 3c. Его описал:
$$ I \ left [{\ mathrm {mAcm}} ^ {- 2} \ left] =0,0084 \ right [\ mathrm {глюкоза} \ right] \ upmu \ mathrm {M} +0,2821 $$ (4)Значение чувствительности составило 8,4 мкА мкМ -1 . см −2 для уравнения. (4). На вставке (внизу) на рис. . 3c. Мы продемонстрировали, что наша наносферная пленка α-NiS является неферментативным сенсором глюкозы в 0,1 М NaOH с противоинтерференционной способностью по отношению к дофамину, мочевой кислоте и молочной кислоте.
Что касается электрохимических результатов на пленках наносфер α-NiS, мы посчитали, что только образец при 400 ° C показал много мелких наночастиц и пористую структуру на поверхности пленки наносфер α-NiS на рис. 2c. Наночастицы меньшего размера и пористая структура были нанесены на поверхность наносферной пленки α-NiS, поэтому наносферная пленка обеспечивала большую площадь поверхности и более высокие отклики при электрохимическом обнаружении. Мы наблюдали, что образцы были отожжены при 400 ° C в течение 4 часов с текущими откликами при низких концентрациях глюкозы. Только образец с температурой 400 ° C, имеющий хороший отклик глюкозы, был обусловлен множеством мелких наночастиц и пористой структурой на поверхности наносферной пленки α-NiS.
На рисунке 3d показано, что спектроскопия электрохимического импеданса (EIS) пленок α-NiS обнаруживает в растворе 0,1 М KCl (содержащем 1,5 мМ Fe (CN) 6 3– / 4– ). Мы заметили, что Варбург ( W ) импеданс наносферной пленки α-NiS был больше, чем у двух других пленок α-NiS. Элементы модели EIS для пленки наносферы α-NiS были R s =133 Ом, R ct =42,1 Ом, C d =22,1 мкФ и Вт =11,7 кОм. Электрохимический импеданс пленки нанолиста Ni также показан на рис. 3d, и на этих рисунках он имел более низкое значение импеданса. Мы также рассчитали значения нашего неферментативного сенсора глюкозы для стабильности, стандартного отклонения (SD) стабильности и возможности повторного использования (см. Таблицу 1). Из значений SD стабильности в Таблице 1 мы наблюдали, что среднее значение стабильности (0,011 мА / мин) измерения в 14 раз было больше, чем среднее значение стабильности (0,006 мА / мин) измерения в 13 раз. Мы полагали, что числовое значение возможности повторного использования составляет приблизительно 13 (стандартное отклонение ≤ 0,002 мА / мин).
После завершения измерения электрохимического поведения образца NiS в 0,1 М NaOH мы также изучили множество работ на предмет физиологического состояния. Эти исследователи использовали различные растворы, такие как фосфатно-солевой буфер (PBS), буфер связывания аннексина V, раствор aECF и буфер Кребса для внесения культур клеток [17,18,19,20,21]. Некоторые исследователи выбрали буфер Кребса в качестве буфера для клеточной культуры при низкой концентрации глюкозы [20, 21]. Линейный диапазон нашей наносферной пленки α-NiS для обнаружения низкого освящения глюкозы составлял от 1 до 35 мкМ в 0,1 М NaOH, поэтому для нас имело практическое значение использование нашего сенсора для обнаружения низкого освящения глюкозы в буфере Кребса для физиологического состояния. . Наносферная пленка α-NiS использовалась для обнаружения глюкозы в различных концентрациях в буфере Кребса. Мы использовали нашу наносферную пленку α-NiS для обнаружения при различных концентрациях глюкозы (0 и 20 мкМ) с помощью циклической вольтамперограммы (CV) в буфере Кребса (115 мМ NaCl, 2 мМ KCl, 25 мМ NaHCO 3 , 1 мМ MgCl 2 , 2 мМ CaCl 2 0,25% бычий сывороточный альбумин [pH 7,4]; уравновешен 5% CO 2 , доводят до pH 7,4 с помощью 0,01 M NaOH) [20]. Как видно на вставке к рис. 3e, на нем показана фоновая CV-кривая чистого ITO. На рисунке 3e также показаны CV-кривые NiS / ITO-электрода в буфере Кребса, содержащем 0 и 20 мкМ глюкозы. Очевидно, мы наблюдали кривые CV с разными характеристиками тока около 0,6 В. Как видно на рис. 3f, пленка наносферы α-NiS была оценена амперометрически в буфере Кребса (pH доведен до 7,4 с помощью 0,01 M NaOH) для определения различных концентраций глюкозы:(α) 0 мкМ, (β) 10 мкМ, (γ ) 20 мкМ, (δ) 30 мкМ и (ε) 40 мкМ. На вставке показан график зависимости тока пика окисления от концентрации глюкозы. Кривая амперометрического отклика показана на вставке (вверху) фиг. 3f, которая демонстрирует линейную зависимость с коэффициентом корреляции 0,99. Его описал I [мкАсм −2 ] =0,0004 [глюкоза] мкМ + 0,0638.
На рис. 4 показаны спектры поглощения и флуоресценции в УФ / видимом / ближнем ИК-диапазоне. Мы регистрировали поглощение пленок α-NiS в УФ / видимом / ближнем ИК-диапазоне в спектральном диапазоне 300–800 нм (рис. 4a – c) для различных температур отжига (300, 400 и 500 ° C). Чтобы определить запрещенную зону ( E g ) наносфер следующая зависимость коэффициента поглощения ( α ) по уравнению энергии фотона [22]:
$$ \ alpha hv =A {\ left (hv- {E} _ {\ mathrm {g}} \ right)} ^ m $$ (5)где E г была энергетическая щель, A - константа, имеющая отдельные значения для разных переходов, hν была энергия фотона, а м был показателем, принимающим значения 1/2, 3/2, 2 и 3, которые были взаимосвязаны с природой электронного перехода. Он отвечал за абсорбцию. Он показал ( αhν ) 2 против hν график на вставке к рис. 4а – в. Когда м =1/2, эти спектры поглощения пленок α-NiS допускают подходящие значения для прямого перехода. Как видно на вставке к рис. 4a – c, мы оценили три запрещенной зоны ( E g ) значения (1,08, 1,8 и 0,66 эВ) пленок α-NiS. Мы использовали пунктирные линии для аппроксимации кривых от 0,6 до 2,8 эВ на вставке к рис. 4a – c. Как видно на вставке к рис. 4a – c, мы также заметили, что самая высокая запрещенная зона ( E g ) пленки наносферы α-NiS составляла примерно 1,8 эВ при температуре отжига 400 ° C. В этом исследовании также использовалось флуоресцентное оборудование для изучения оптических свойств образцов. Предыдущие исследователи сосредоточились на спектрах флуоресценции частиц α-NiS, на которые влияли различные фазы, формы, структуры и соотношение поверхность / объем [23]. Как видно на рис. 4d, мы наблюдали спектры флуоресценции пленок α-NiS с ультрафиолетовым излучением при различных температурах отжига (300, 400 и 500 ° C). Спектры ФЛ образцов показали острые пики эмиссии при 448 нм и пики эмиссии при 369 нм (возбужденные при λ бывший =277 нм) [23, 24]. В соответствии с результатами по оптическим свойствам наших пленок α-NiS мы посчитали, что разные температуры отжига могут привести к получению разного размера зерна на пленке NiS. Что касается наночастиц, обладающих квантовым ограничением, увеличение размера наночастиц влияло на уменьшение ширины запрещенной зоны с температурой от 400 до 500 ° C [25]. Оптические свойства NiS изменяются при разном размере зерна, поэтому оптические свойства NiS существенно меняются при разных температурах [25]. Значительно меняющиеся оптические свойства пленки NiS при разных температурах должны быть связаны с проявлением размерного эффекта, уменьшающего размер частиц, влияющих на ширину запрещенной зоны.
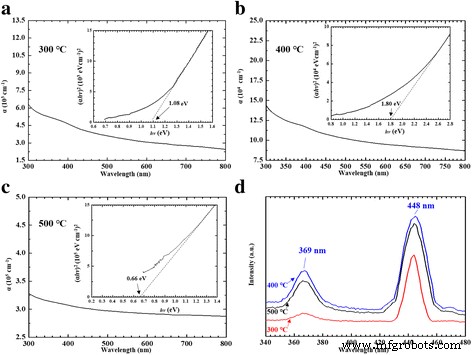
Спектры поглощения УФ / видимого / ближнего ИК-диапазона и ( αhν ) 2 по сравнению с hν график на вставках к рисункам для синтеза пленок α-NiS на a 300, b 400 и c 500 ° С. г Спектры флуоресценции пленок α-NiS были получены при различных температурах отжига (300, 400 и 500 ° C в течение 4 ч)
Мы рассмотрели возможность фокусирования HR-TEM-анализа на пленке наносфер α-NiS, потому что мы получили много наносфер α-NiS для неферментативных сенсоров глюкозы при температуре отжига 400 ° C. Как видно на рис. 5, мы наблюдали, что наносферы α-NiS отжигались при 400 ° C в течение 4 часов. Информация о микроструктуре свежеприготовленной наносферы α-NiS была получена с помощью HR-TEM. На рис. 5а, б представлены изображения наносфер с помощью ПЭМ-ВР. Диаметр наносферы составлял от 150 до 250 нм. На рисунке 5c изображение HR-TEM также показало четкие полосы решетки с промежутком 0,7786 нм, которые соответствовали расстоянию между двумя соседними (101) плоскостями наносферы α-NiS. На рисунке 5d показан SAED-рисунок наносферы, а пятна дифракционного кольца проиндексированы как (101) наноструктуры α-NiS.

а - c ВР-ПЭМ изображения наносферы α-NiS. г Образец SAED наносферы α-NiS отжигался при 400 ° C в течение 4 часов
Заключение
Таким образом, наносферные пленки α-NiS были исследованы с использованием оборудования XRD, VVSEM, FE-SEM, EDS, EIS, UV, PL и HR-TEM. Мы наблюдали, что пленка наносферы α-NiS была сформирована путем регулирования температуры отжига при 400 ° C в течение 4 часов в запаянных под вакуумом стеклянных ампулах. Энергетическая щель ( E g ) пленки наносферы α-NiS составляла примерно 1,8 эВ. После хранения наших пленок наносфер α-NiS в нашей лаборатории в течение пяти с половиной лет мы обнаружили, что пленки наносфер α-NiS все еще имели отклики тока при различных концентрациях глюкозы с помощью измерений CV и амперометрии в различных растворах (0,1 M NaOH и Krebs буфер). Линейный диапазон определения глюкозы составлял от 1 до 35 мкМ в 0,1 М NaOH. For a physiological condition, the linear range of detecting glucose was approximately from 0 to 40 μM in Krebs buffer.
Сокращения
- CV:
-
Cyclic voltammogram
- EDS:
-
Energy-dispersive spectrometer
- FE-SEM:
-
Field emission scanning electron microscopy
- HR-TEM:
-
High-resolution transmission electron microscopy
- NiS:
-
Nickel sulfide
- PL:
-
Фотолюминесценция
- PVT:
-
Physical vapor transport
- SD:
-
Standard deviation
- UV/Visible/NIR:
-
Ultraviolet/visible/near-infrared
- VVSEM:
-
Variable vacuum scanning electron microscopy
- wt%:
-
Percentage by weight
- XRD:
-
X-ray diffraction
Наноматериалы
- Потребность в высокоточных датчиках сверхнизкого давления
- Медицинские датчики Maxim для носимых устройств сверхмалого размера
- Аналоговые датчики на Raspberry Pi с использованием MCP3008
- Решение для резки для киноиндустрии - цифровая режущая машина
- Ученые IBM изобрели термометр для наномасштаба
- Как сетевые датчики 0G защищают холодовую цепь вакцины
- Как правильно выбрать датчик для заполнения приложений
- Материал для следующего поколения интеллектуальных датчиков
- Новый математический инструмент позволяет выбирать лучшие датчики для работы
- Долгосрочные преимущества профилактического обслуживания вашего грузовика



