Получение наностержней оксида алюминия из хромсодержащего осадка оксида алюминия
Аннотация
Наностержни оксида алюминия были приготовлены из хромсодержащего шлама оксида алюминия, и было исследовано влияние легирующих элементов, таких как Cr, Fe и Mg. Результаты показывают, что кристаллическое превращение оксида алюминия ограничивается легированным Cr и облегчается легированным Fe и Mg, который превращается из θ -Al 2 О 3 до α -Al 2 О 3 в процессе прокаливания. Между тем, кристаллическое превращение оксида алюминия сильно сдерживается совместно легированными элементами из хромсодержащего шлама оксида алюминия. Легированные элементы изменяют ход трансформации фазовой структуры и незначительно трансформируют химическую связь наностержней оксида алюминия. Примесные элементы легированы в кристалл оксида алюминия и сдерживают рост кристаллов наностержней оксида алюминия в соответствии с правилами. В образце, приготовленном из хромсодержащего шлама оксида алюминия, легировано больше Cr и Mg, но меньше Fe, и большая часть Cr присутствует в виде Cr (III). Возможно, что легирование Fe ограничивается конкуренцией Cr и Mg. Кроме того, дефект решетки оксида алюминия вызван легированными ионами, такими как Cr, Fe и Mg, и это влияет на химическое состояние O и Al. Результаты этих экспериментов предоставляют важную информацию для устранения загрязнения и содействия комплексной утилизации хромсодержащего оксида алюминия.
Фон
Низкоразмерные нанооксиды алюминия, такие как нановолокна оксида алюминия [1,2,3] и наностержни оксида алюминия [4], обладают превосходными свойствами высокой прочности, высоким модулем упругости, химической стабильностью, хорошими теплоизоляционными характеристиками и низкой теплопроводностью [5, 6,7,8,9], поэтому он широко применялся в различных областях, таких как усиление композитов с керамической матрицей и композитов с металлической матрицей и катализатора, носителя катализатора, адсорбентов, мембранных реакторов, покрытий и анодных материалов [4, 10, 11,12,13,14,15]. Однако высокая стоимость производства ограничила его применение. Некоторые авторы сообщают об успешных методах синтеза низкоразмерных нанооксида алюминия, в основном включая твердофазный метод, парофазный метод [16] и жидкофазный метод [17, 18]. Среди них жидкофазный метод широко применяется из-за мягких условий реакции, гомогенных продуктов и низкой стоимости производства. Было много сообщений о получении нанооксида алюминия золь-гель методом [5, 19,20,21], методом микроэмульсии [22], гидротермальным методом [23], методом осаждения [23], химическим осаждением из газовой фазы [16], и электроспиннинг [1, 3, 24, 25]. Однако метод осаждения подходит для лабораторий и производств из-за низкого энергопотребления, однородности продукта и контролируемых размеров и формы.
Хромсодержащий глиноземный шлам является разновидностью опасных твердых отходов, которые образуются в процессе производства хромовых продуктов некальциевым методом обжига. Из каждой тонны хромового продукта образуется семь тысяч килограммов хромосодержащего глиноземного шлама. Он состоит из 55 ~ 65% Al 2 О 3 , 7 ~ 13% хрома и несколько соединений кремния, железа, магния и натрия. Компоненты хромсодержащего шлама оксида алюминия показаны в таблице 1 и предоставлены производителем (CITIC Jinzhou Metal Co., Ltd., Китай).
В качестве основного опасного вещества хром существует в форме Cr (III) или Cr (VI) в хромсодержащем глиноземном шламе, а Cr (VI) считается доминирующим загрязнителем из-за его канцерогенности [26]. В настоящее время загрязнения раствора хромсодержащего глиноземного шлама в основном обезвреживаются и утилизируются. Первый преобразует Cr (VI) в Cr (III) с низкой токсичностью и хранит его в виде остатков отходов. Чжан Далей [27] отметил метод пиролиза для преобразования Cr (VI) в Cr (III) с использованием соломы. Дуан Сухуа [28] указал, что хромсодержащий шлак можно обрабатывать техническим спиртом. Однако упомянутые выше методы не только занимают землю, но и приводят к большой трате ресурсов. Более того, вторичное загрязнение может произойти неожиданно. Последний метод заключается в разделении и использовании полезных компонентов хромсодержащего шлама оксида алюминия. Сюэ Вендонг [29] сообщил, что хромсодержащий оксид алюминия можно использовать для приготовления огнеупоров. Однако вышеуказанный метод может быть ограничен из-за его низкой добавленной стоимости. Следовательно, необходимо предложить некоторые новые методы для устранения загрязнения и содействия комплексной утилизации хромсодержащего оксидно-алюминиевого шлама, что может не только решить экологические проблемы, но и принести большую экономическую выгоду.
В этой статье наностержни оксида алюминия получают из хромсодержащего шлама оксида алюминия методом осаждения-прокаливания. Между тем, чтобы исследовать влияние одинарного легирующего иона на наностержни оксида алюминия, были приготовлены и охарактеризованы наностержни оксида алюминия с нелегирующим или одинарным легирующим ионом. Результаты предоставят техническую поддержку для устранения загрязнения и содействия комплексной утилизации хромосодержащего оксида алюминия.
Методы
Материалы
Реагенты (например, октадекагидрат сульфата алюминия, сульфат хрома, сульфат железа, сульфат магния, гидроксид натрия, серная кислота и додецилбензолсульфонат натрия), использованные в этом исследовании, были аналитически чистыми химическими веществами. Хромсодержащий оксид алюминия был предоставлен компанией CITIC Jinzhou Metal Co., Ltd. (Китай). Все растворы были приготовлены на деионизированной воде.
Обработка хромсодержащего глиноземного осадка
Сначала хромсодержащий оксид алюминия промывали и фильтровали деионизированной водой в соответствии с соотношением твердое вещество – жидкость 1:5 (г / мл). В результате большая часть Cr 6+ соединения были отделены от хромсодержащего глиноземного шлама. Затем осадок на фильтре растворяли серной кислотой в соответствии с соотношением твердой и жидкой фаз 1:3 (г / мл), а затем H 2 О 2 был использован для преобразования остаточного Cr 6+ кому:Cr 3+ . Наконец, кислотный раствор хромсодержащего глиноземного осадка был успешно получен, и компоненты были проанализированы с помощью химического титрования и спектрофотометра в видимом свете (VIS, 721N, Varian, America), показанного в таблице 2.
Синтез наностержней оксида алюминия
Два моля на литр раствора NaOH и раствора додецилбензолсульфоната медленно добавляли к 0,25 моль / л Al 2 . (SO 4 ) 3 раствор при перемешивании на магнитной мешалке при 85 ° C, и значение pH смешанного раствора доводили до 9,0 с помощью NaOH или H 2 SO 4 решение. После перемешивания в течение 5 ч и выдержки в течение 20 ч осадки отделяли и несколько раз промывали деионизированной водой и этиловым спиртом. Затем образцы сушили в вакууме при 40 ° C в течение 15 ч, а затем готовили прекурсоры. Наконец, образцы прокаливали при 250 ° C в течение 1 часа, 400 ° C в течение 1 часа, 770 ° C в течение 1 часа, 900 ° C в течение 1 часа и 1050 ° C в течение 2 часов непрерывно, а затем образцы были собраны. для использования. Нелегированный оксид алюминия получали из чистого Al 2 . (SO 4 ) 3 раствора, и образцы с ионным легированием были приготовлены тем же способом, что и выше. Между тем, хлораты Cr, Fe и Mg были добавлены в Al 2 (SO 4 ) 3 раствор в соответствии с содержанием легирующего элемента в шламе хромсодержащего оксида алюминия (таблица 2), а также оксид алюминия, легированный хромом, железом и магнием. Используя кислотный раствор хромсодержащего глиноземного шлама в качестве сырья, был назван оксид алюминия, который был приготовлен из хромсодержащего глиноземного шлама.
Характеристики стержней из нанооксида алюминия
Кристаллические фазы образцов охарактеризованы методом порошковой рентгеновской дифракции (XRD) на рентгеновском дифрактометре D / MAX-RB (Rigaku, Япония) с Cu K-излучением в диапазоне 2θ от 10 ° до 70 ° при сканировании. скорость 2 ° / мин. Инфракрасные спектры с преобразованием Фурье (FT-IR) образцов были охарактеризованы с использованием ближнего FT-IR спектрометра Scimitar 2000 (Thermo electronic, США), и спектры регистрировались в диапазоне 4000–400 см -1 . Термическую стабильность прекурсора исследовали на термогравиметрическом анализаторе (TG-DSC, STA449F3, NETZSCH, Германия) при скорости потока 30 мл / мин в воздушной атмосфере и температуре 15–1200 ° C со скоростью нагрева 10 ° C. С / мин. Морфологию, кристаллическую структуру и распределение элементов в образцах исследовали с помощью автоэмиссионной просвечивающей электронной микроскопии (FETEM, Jem-2100F, JEOL, Япония). Спектры рентгеновской фотоэлектронной спектроскопии (XPS) образцов были записаны на XPS (ESCAMABMKLL, VG, UK), оборудованном полусферическим электронным анализатором и Al Kα Источник рентгеновского излучения.
Результаты и обсуждение
XRD-анализ наностержней оксида алюминия
Для подтверждения кристаллической структуры образцов были записаны рентгенограммы, как показано на рис. 1. Для нелегированных наностержней оксида алюминия результаты XRD показывают наличие различных кристаллических структур оксида алюминия, включая корунд ( α -Al 2 О 3 , син.) (JCPDS № 46–1212) и оксид алюминия ( θ -Al 2 О 3 , JCPDS № 35–0121), и дифракционные пики θ -Al 2 О 3 слабее (рис. 1 (а)). Как правило, оксид алюминия переводится из переходного состояния θ -Al 2 О 3 в установившееся состояние α -Al 2 О 3 при 1000 ~ 1200 ° C. По сравнению с нелегированным образцом наностержни оксида алюминия, легированного хромом, имеют относительно более сильные пики θ -Al 2 О 3 и относительно более слабые пики α -Al 2 О 3 (Рис. 1 (б)). Это означает, что кристаллический переход ограничен легированным Cr в процессе прокаливания, поэтому меньше θ -Al 2 О 3 преобразуется в α -Al 2 О 3 после прокаливания при 1050 ° C. Из рис. 1 (c) видно, что пики α -Al 2 О 3 сильнее и острее, чем на рисунках (а) и (б), что предполагает больший размер кристаллов и лучшую кристалличность. Между тем, пики θ -Al 2 О 3 еще слабее, что указывает на то, что переход в кристалл облегчается легированным Fe. Это может быть потому, что больше θ -Al 2 О 3 преобразуется в α -Al 2 О 3 после прокаливания. Рисунок 1 (d) показывает, что наностержни оксида алюминия, легированного магнием, имеют относительно более сильные и острые пики α -Al 2 О 3 и относительно более слабые пики θ -Al 2 О 3 . Предполагается, что образец содержит больше α -Al 2 О 3 и менее θ -Al 2 О 3 , что может быть связано с тем, что легированный Mg способствует кристаллическому переходу оксида алюминия в процессе прокаливания. Для наностержней оксида алюминия, полученных из хромсодержащего шлама оксида алюминия, пики α -Al 2 О 3 почти исчезают, а пики θ -Al 2 О 3 становятся сильнее, но недостаточно острыми (рис. 1 (е)). Указывается, что θ -Al 2 О 3 имеет плохую кристалличность и меньший размер кристаллов. Это может быть связано с тем, что больше примесных элементов хромсодержащего шлама оксида алюминия легировано оксидом алюминия, и кристаллический переход оксида алюминия ограничен в процессе прокаливания. Итак, θ -Al 2 О 3 редко преобразуется в α -Al 2 О 3 .
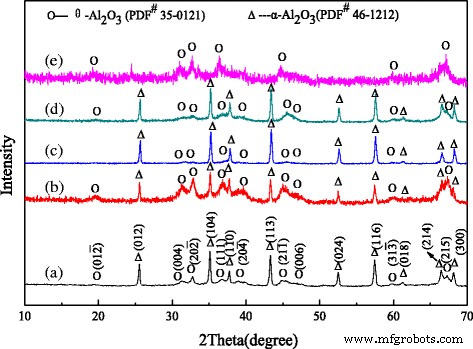
Картины XRD наностержней оксида алюминия, легированных различными ионами: a нелегированный оксид алюминия, b Оксид алюминия, легированный хромом, c Глинозем, легированный Fe, d Оксид алюминия, легированный магнием, и е глинозем, полученный из хромсодержащего глиноземного шлама
FT-IR Спектры наностержней оксида алюминия
ИК-Фурье спектры наностержней оксида алюминия в диапазоне 4000–400 см −1 изображены на рис. 2 [27]. Пики поглощения при 3500–3300 и 1635 см −1 появляющиеся во всех спектрах, приписываются валентным колебаниям ассоциации нехимических связей групп ОН и деформационным колебаниям H – O – H соответственно, указывая на то, что в образцах присутствуют поровая вода и адсорбированная вода [30]. Пики на 2360 см −1 объясняются наличием углекислого газа. На рис. 2 (2) показана область отпечатков пальцев в ИК-Фурье спектрах образцов. Как показано на рис. 2 (2a), для нелегированного образца пики при 829, 589 и 449 см −1 относятся к AlO 6 колебания, указывающие на образование α -Al 2 О 3 [1]. Между тем, пики на 762 см −1 приписываются изгибным колебаниям Al – O – Al, а колебания 663 и 488 см −1 относятся к валентным колебаниям и изгибным колебаниям Al – O соответственно, что указывает на образование θ -Al 2 О 3 . Рисунок 2 (2b) показывает, что пики α -Al 2 О 3 слабее, чем на рис. 2 (2а), что указывает на то, что легирование хромом предотвращает образование α -Al 2 О 3 в процессе прокаливания. Для оксида алюминия, легированного Fe и Mg, пики θ -Al 2 О 3 становятся слабее, а пики α -Al 2 О 3 имеют очень небольшие изменения (рис. 2 (2c, d)). По сравнению с рис. 2 (2a), пики слегка сместились в красную или голубую сторону, что свидетельствует о том, что легированные Fe и Mg улучшают рост α -Al 2 О 3 и слегка преобразуют химическую связь наностержней оксида алюминия. Рис. 2 (2e) представляет собой область отпечатков пальцев FT-IR спектров наностержней оксида алюминия, полученных из хромсодержащего шлама оксида алюминия. Пики ниже 500 см −1 исчезнут, указывая на отсутствие α -Al 2 О 3 в образцах. Более того, пики на 900–500 см −1 являются диспергированными, что может быть результатом колебаний M – O и M – O – M (M представляет собой Al или легированный элемент оксида алюминия из хромсодержащего глиноземного шлама). Приведенные выше результаты соответствуют результатам XRD.
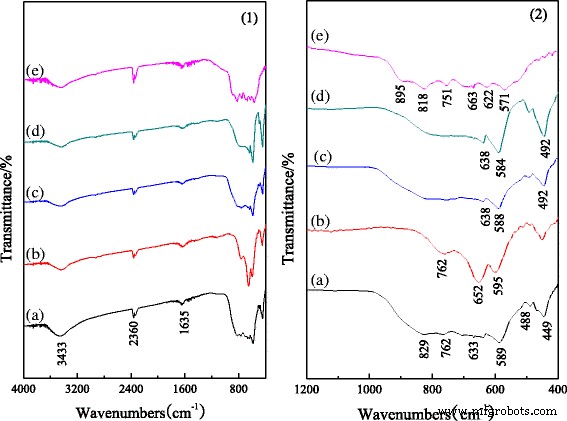
ИК-Фурье спектры стержней из нанооксида алюминия, легированных различными ионами: a нелегированный оксид алюминия, b Оксид алюминия, легированный хромом, c Глинозем, легированный Fe, d Оксид алюминия, легированный магнием, и е глинозем, полученный из хромсодержащего глиноземного шлама
TG-DSC наностержней оксида алюминия
Кривые термогравиметрического анализатора (TG) и дифференциальной сканирующей калориметрии (DSC) прекурсоров наностержней оксида алюминия показаны на рис. 3. Результаты XRD показывают, что прекурсором наностержней оксида алюминия является AlO (OH) (JCPDS № 49–0133). Как показано на рис. 3а, на воздухе в нелегированном образце можно увидеть только три стадии. Ниже 250 ° C потеря массы около 40% на кривой ТГ и соответствующие эндотермические пики при 50 и 150 ° C на кривой ДСК связаны с испарением влаги и десорбцией адсорбированной воды. Вторая стадия находится между 250 и 730 ° C, с общей потерей массы около 35%, и два эндотермических пика находятся при 320 и 694 ° C. При температуре 320 ° C эндотермический пик обусловлен превращением AlO (OH) в аморфный Al 2 . О 3 . Между тем, слабый эндотермический пик при 694 ° C приписывают превращению аморфного Al 2 О 3 на θ -Al 2 О 3 . На третьей стадии при температуре выше 730 ° C наблюдается небольшая потеря массы и сильный эндотермический пик при 980 ° C, который в основном является результатом преобразования θ -Al 2 О 3 до α -Al 2 О 3 . По сравнению с нелегированным образцом легирование ионами металлов приводит к смещению эндотермических пиков. На рис. 3б – д видно, что эндотермические пики смещаются в сторону более высоких температур и становятся расширенными. Это может быть связано с тем, что легированные ионы изменяют ход трансформации фазовой структуры, поэтому степень трансформации θ -Al 2 О 3 до α -Al 2 О 3 отличается для каждого образца. Результаты согласуются с данными XRD и FT-IR.
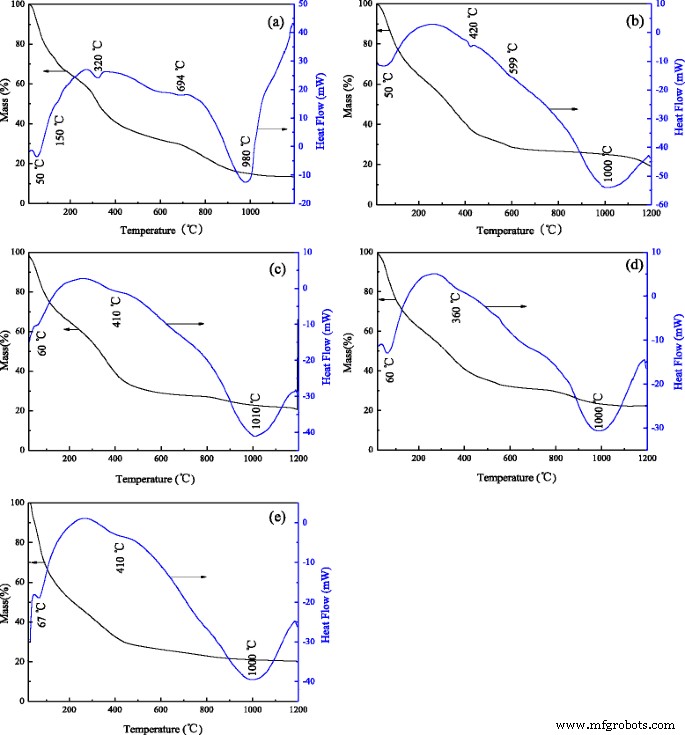
ТГ и ДСК предшественников наноразмерных стержней из оксида алюминия, легированных различными ионами: a нелегированный оксид алюминия, b Оксид алюминия, легированный хромом, c Глинозем, легированный Fe, d Оксид алюминия, легированный магнием, и е Глинозем, полученный из хромсодержащего глиноземного шлама
Изображения наностержней оксида алюминия в TEM, SAED и HRTEM
На рисунке 4 представлены результаты ПЭМ, электронной дифракции (SAED) и просвечивающей электронной микроскопии высокого разрешения (HRTEM). Как показано на рис. 4 (a1 – a3), нелегированный оксид алюминия представляет собой дисперсные наностержни диаметром 4–6 нм и длиной 20–60 нм. Между тем, плоскости (215), (006), (21 \ (\ overline {1} \)) и (20 \ (\ overline {4} \)) соответствуют θ -Al 2 О 3 (JCPDS № 35–0121), а плоскости (300), (214), (113) и (104) связаны с α -Al 2 О 3 (JCPDS № 46–1212). Кроме того, наблюдаемое межплоскостное расстояние 0,273 и 0,284 нм можно отнести к плоскостям (20 \ (\ overline {2} \)) и (004) θ -Al 2 О 3 , а шаг решетки 0,255 и 0,348 нм может соответствовать плоскостям (104) и (012) α -Al 2 О 3 . По сравнению с нелегированным образцом, образец, легированный хромом, представляет собой наностержни диаметром 4–6 нм и длиной 50–120 нм (рис. 4 (b1)). На рисунке 4 (b2) показано, что плоскости (215), (21 \ (\ overline {1} \)), (20 \ (\ overline {2} \)) и (111) соответствуют θ -Al 2 О 3 , а плоскости (300), (214), (113) и (104) соответствуют α -Al 2 О 3 . Как показано на рис. 4 (b3), межплоскостное расстояние 0,202 нм, 0,273 нм, 0,284 нм и 0,454 нм присвоено (21 \ (\ overline {1} \)), (20 \ (\ overline { 2} \)), (004) и (10 \ (\ overline {2} \)) плоскости θ -Al 2 О 3 , а межплоскостное расстояние 0,209 и 0,238 нм отнесено к плоскостям (113) и (110) α -Al 2 О 3 . Рисунок 4 (c1) показывает, что образец, легированный Fe, представляет собой смесь наностержней диаметром 5–10 нм и длиной 30–100 нм и наночастиц около 10 нм. На рисунке 4 (c2) показано, что плоскости (20 \ (\ overline {2} \)) соответствуют θ -Al 2 О 3 , а плоскости (300), (214), (024), (113), (104) и (116) соответствуют α -Al 2 О 3 , это согласуется с результатами XRD. Между тем, наблюдаемые межплоскостные расстояния 0,284 и 0,454 нм соответствуют плоскостям (004) и (10 \ (\ overline {2} \)) θ -Al 2 О 3 , а межплоскостное расстояние 0,238 и 0,255 нм отнесено к плоскостям (110) и (104) α -Al 2 О 3 (Рис. 4 (c3)).
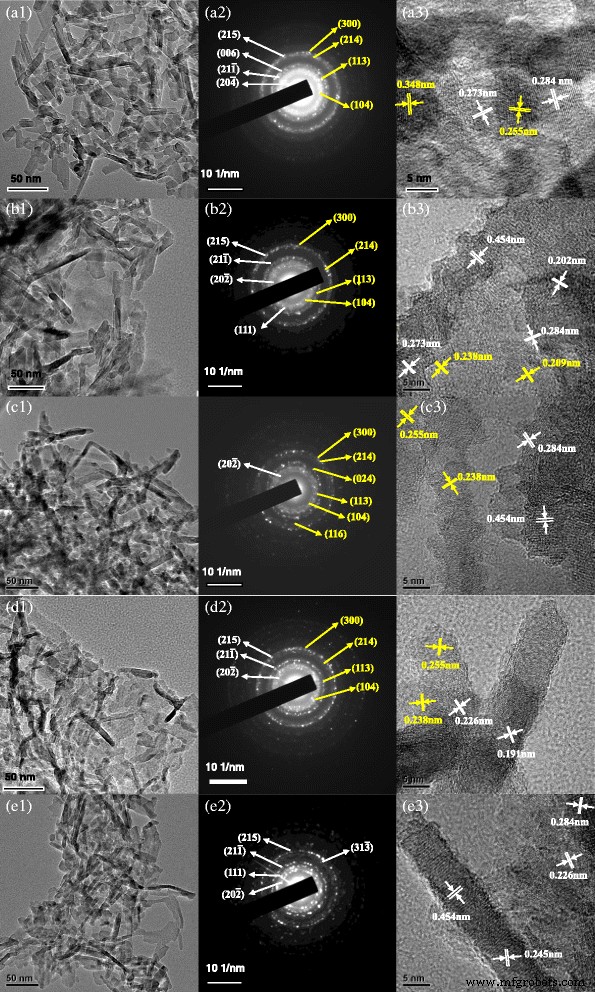
ПЭМ, SAED и HRTEM наностержней оксида алюминия, легированных различными ионами: a нелегированный оксид алюминия, b Оксид алюминия, легированный хромом, c Глинозем, легированный Fe, d Оксид алюминия, легированный магнием, и е оксид алюминия, полученный из хромсодержащего шлама оксида алюминия. (1) ТЕМ; (2) САЭД; (3) HRTEM
Как показано на рис. 4 (d1 – d3), легированный магнием образец представляет собой хорошо диспергированные наностержни диаметром 5–10 нм и длиной 20–50 нм, причем наночастицы размером около 10 нм существуют одновременно. Результаты SAED показывают, что плоскости (215), (21 \ (\ overline {1} \)) и (20 \ (\ overline {2} \)) соответствуют θ -Al 2 О 3 , а плоскости (300), (214), (113) и (104) соответствуют α -Al 2 О 3 . Результаты ПЭМВР показывают, что наблюдаемое межплоскостное расстояние 0,226 и 0,191 нм соответствует плоскостям (20 \ (\ overline {4} \)) и (006) θ -Al 2 О 3 , а межплоскостное расстояние 0,255 и 0,238 нм отнесено к плоскостям (104) и (110) α -Al 2 О 3 . Рис. 4 (e1 – e3) показывает, что образец, приготовленный из хромсодержащего оксида алюминия, представляет собой хорошо диспергированные наностержни диаметром 4–6 нм и длиной 50–100 нм, причем одновременно существуют наночастицы размером около 5–10 нм. Результаты SAED и HRTEM показывают, что (215), (111), (21 \ (\ overline {1} \)), (31 \ (\ overline {3} \)) и (20 \ (\ overline {2 } \)) плоскости соответствуют θ -Al 2 О 3 , а наблюдаемое межплоскостное расстояние 0,226, 0,245, 0,284 и 0,454 нм присвоено (20 \ (\ overline {4} \)), (111), (004) и (10 \ (\ overline {2 } \)) плоскости этого. Однако нет плоскостей в соответствии с α -Al 2 О 3 . В результате наностержни нелегированного оксида алюминия хорошо диспергируются, чем другие, и частицы имеют правильную форму. Возможно, что примесные элементы легированы в кристалл оксида алюминия и сдерживают рост кристаллов наностержней оксида алюминия в соответствии с правилами. Таким образом, на форму и дисперсность наностержней оксида алюминия влияют легированные элементы.
EDS-характеристика прекурсора наностержней оксида алюминия, легированного различными ионами
Результаты EDS показывают, что Cr, Fe и Mg легированы в предшественник наностержней оксида алюминия с молярным количеством 2,06, 0,99 и 0,58% соответственно (таблица 3). Это количество легирования близко к добавляемой дозе примесного элемента (Таблица 2), что указывает на то, что большинство примесных элементов легированы в предшественник наностержня оксида алюминия. Между тем, для образца, приготовленного из хромсодержащего шлама оксида алюминия, легированное молярное количество Cr, Fe и Mg составляет 2,11, 0,14 и 0,96% соответственно. Результаты показывают, что большая часть Cr и Mg легирована в образец, но небольшое количество Fe легировано в него. Возможно, легирование Fe ограничивается конкуренцией Cr и Mg.
XPS-анализ нанометровых волокон из оксида алюминия, легированных различными ионами
На рисунке 5 показаны XPS-спектры O1 s и Al 2 p . Как показано на рис. 5a, пики при 531,90, 531,85, 531,15, 531,20 и 532,00 эВ относятся к нелегированным, легированным хромом, легированным Fe и Mg наностержням оксида алюминия, а также образцу, полученному из хромсодержащего материала. глиноземный шлам соответственно. Пики присвоены O 2− Аль 2 О 3 [31]. На Фигуре 5b показаны пики Al 2 p при 74,00, 74,25, 74,75, 74,38 и 73,90 эВ. относятся к указанным выше образцам соответственно. Пики приписываются Al 3+ Аль 2 О 3 . Между тем, хорошая симметрия кривой подтверждается гауссовой аппроксимацией, что указывает на то, что в образцах образуется меньше другого кислорода и алюминия. O1 s Энергия связи (BE) нелегированных и легированных хромом наностержней оксида алюминия и образца, приготовленного из хромсодержащего шлама оксида алюминия, почти и выше, чем у образцов, легированных Fe и Mg. Порядок наименьших O1s BE следующий:легированные Fe, легированные Mg, легированные Cr, нелегированные наностержни оксида алюминия и образец, приготовленный из хромсодержащего шлама оксида алюминия. Однако Al 2p BE наоборот. Результаты XRD показывают, что более переходное состояние θ -Al 2 О 3 находятся в нелегированных и легированных хромом наностержнях оксида алюминия и образце, приготовленном из хромсодержащего шлама оксида алюминия, и более α -Al 2 О 3 находятся в наностержнях оксида алюминия, легированного Fe и Mg. Благодаря форме согласования [AlO 4 ] для θ -Al 2 О 3 и [AlO 6 ] для α -Al 2 О 3 , возможно, что O1 s BE из [AlO 6 ] больше и Al 2 p BE меньше, чем у [AlO 4 ]. Кроме того, дефекты решетки Al 2 О 3 вызваны тем, что ионы Cr, Fe и Mg входят в Al 2 О 3 решетка. Таким образом, на химические состояния O и Al влияет дефект решетки, и энергия связи изменяется.
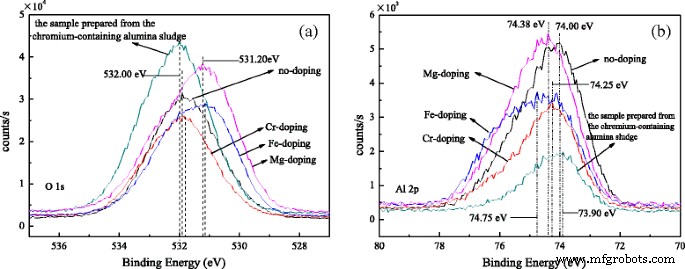
XPS-спектры a O1 s и b Al 2 p для наностержней оксида алюминия, легированных различными ионами
На рис. 6 представлены рентгеновские фотоэлектронные спектры легирующего иона. Как показано на рис. 6а, пики при 589.80 и 578,52 эВ отнесены к Cr 2p 1/2 и Cr 2p 3/2 Cr (VI), а пики при 587,53 и 577,39 эВ отнесены к Cr 2p 1/2 и Cr 2p 3/2 Cr (III). Это показывает, что Cr присутствует в наностержнях оксида алюминия, легированного Cr, в виде Cr (VI) и Cr (III). Однако большая часть Cr присутствует в виде Cr (III) в образце, приготовленном из хромсодержащего шлама оксида алюминия. Это указывает на то, что часть Cr (III) окисляется в процессе прокаливания в образце, легированном Cr, но меньше Cr (III) окисляется в образцах, приготовленных из хромсодержащего шлама оксида алюминия. Для образцов, приготовленных из шлама хромсодержащего оксида алюминия, поскольку образуется комбинация химических связей Cr – O и примесного металлического элемента, электродный потенциал Cr 6+ / Cr 3+ увеличивается при высокой температуре, поэтому в образце мало Cr (VI). Как показано на рис. 6b, пики при 724,45 и 711,30 эВ относятся к Fe 2p 1/2 и Fe 2p 3/2 Fe 2 О 3 , а 722,38 и 710,44 эВ отнесены к Fe 2p 1/2 и Fe 2p 3/2 Fe 3 О 4 . Результаты показывают, что Fe присутствует в образце, легированном Fe, в виде Fe (II) и Fe (III). Предполагается, что элемент Fe вводится в решетку предшественника оксида алюминия и занимает место в решетке алюминия во время синтеза. В процессе последующего прокаливания небольшое количество Fe (III) восстанавливается до Fe (II) за счет восстановления вещества в воздухе. Однако в образце, приготовленном из хромсодержащего оксида алюминия, пиков Fe нет из-за небольшого количества Fe в образце (Таблица 3). Как показано на фиг. 6c, пики при 50,20–50,34 эВ относятся к Mg 2 p MgO, предполагая, что Mg присутствует в легированном Mg образце как MgO. Однако пик Mg 2p очень слаба в образце, приготовленном из хромсодержащего шлама оксида алюминия. Возможно, содержание Mg встречается редко. Результаты согласуются с EDS. По результатам XRD, FT-IR и XPS показано, что дефект решетки одноэлементных легирующих образцов формируется из-за примесей металлического элемента, входящего в решетку оксида алюминия. Однако из-за конкуренции нескольких элементов больше Cr вводится в решетку глинозема, полученного из хромсодержащего глиноземного шлама, и вводится мало элементов Fe и Mg.
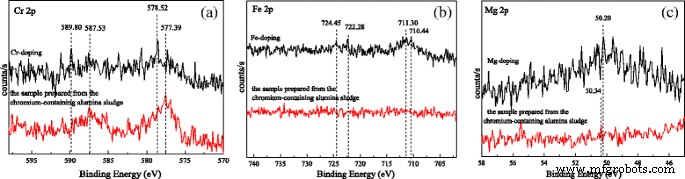
XPS-спектры a Cr 3+ 2 п , b Fe 3+ 2 п , и c Мг 2+ 2 п
Выводы
Таким образом, примесные элементы были легированы в наностержни оксида алюминия, такие как Cr, Fe и Mg. Кристаллическое преобразование оксида алюминия ограничено легированным Cr и облегчается легированными Fe и Mg, которые превращаются из θ -Al 2 О 3 до α -Al 2 О 3 в процессе прокаливания. Кроме того, кристаллическое превращение оксида алюминия сильно сдерживается совместно легированными элементами из хромсодержащего шлама оксида алюминия. На процесс преобразования фазовой структуры, химическую связь, микроструктуру и химическое состояние O и Al наностержней оксида алюминия влияют легированные элементы. В образце, приготовленном из хромсодержащего шлама оксида алюминия, легирование Fe ограничивается конкуренцией Cr и Mg. Это исследование предполагает, что наностержни оксида алюминия могут быть приготовлены из хромсодержащего шлама оксида алюминия для снижения затрат и устранения загрязнения.
Сокращения
- BE:
-
Связующая энергия
- DSC:
-
Анализ методом дифференциальной сканирующей калориметрии
- EDS:
-
Энергодисперсионный спектрометр
- FETEM:
-
Автоэмиссионная просвечивающая электронная микроскопия
- FT-IR:
-
Инфракрасные спектры с преобразованием Фурье
- HRTEM:
-
Просвечивающая электронная микроскопия высокого разрешения
- SAED:
-
Электронная дифракция в выбранной области
- ТЕМ:
-
Просвечивающая электронная микроскопия
- TG:
-
Термогравиметрический анализатор
- XPS:
-
Рентгеновская фотоэлектронная спектроскопия
- XRD:
-
Рентгеновская порошковая дифракция
Наноматериалы
- Приготовление порошка рения
- Способы приготовления танталового порошка
- Преобразование из десятичной нумерации
- От электрического к электронному
- 3 причины для перехода с C на C ++
- Наноцеллюлоза из сине-зеленых водорослей
- Золотые наностержни с покрытием BSA для фототермической терапии NIR-II
- Получение и магнитные свойства легированных кобальтом наночастиц шпинели FeMn2O4
- Наножидкости TiO2 - Часть 1:Приготовление и свойства
- От пользовательского интерфейса к ИИ:путь к автоматизации



