Раскисление стали
Раскисление стали
Процесс производства стали состоит из рафинирования чугуна до стали, которое осуществляется в окислительной атмосфере. В процессе рафинирования кислород растворяется в стали. Ниже приведены основные источники кислорода в стали.
- Продувка кислородом
- Использование окислительных шлаков и железной руды в процессах производства стали
- Поглощение кислорода воздуха жидкой сталью во время разливки
- Окислительные огнеупоры футеровки
- Ржавый и мокрый лом.
Раскисление является последней стадией производства стали. При производстве стали стальная ванна во время выпуска содержит от 400 до 800 частей на миллион активности кислорода. Раскисление проводят при выпуске путем добавления в разливочный ковш соответствующих количеств ферросплавов или других специальных раскислителей. Если в конце продувки содержание углерода в стали ниже нормативного, жидкая сталь также подвергается переуглероживанию в разливочном ковше. Однако большие добавки в разливочном ковше отрицательно сказываются на температуре жидкой стали.
Растворимость кислорода в стали пренебрежимо мала. При затвердевании расплавленной стали избыток кислорода отбрасывается затвердевающей сталью. Растворимость кислорода в жидкой стали составляет 0,23 % при 1700 град. С. Она уменьшается в процессе охлаждения, а затем резко падает при затвердевании жидкой стали, достигая 0,003 % в твердой стали.
Избыток кислорода, высвобождаемый из твердого раствора , окисляет компоненты стали, такие как C, Fe, и легирующие элементы, что приводит к образованию пузырей и неметаллических включений , захваченных структурой литой стали. И пузыри, и включения оказывают значительное влияние на механические свойства и отрицательно сказываются на качестве стали.
Чтобы предотвратить окисление стальных компонентов во время затвердевания, необходимо уменьшить содержание кислорода в жидкой стали. Это осуществляется путем раскисления стали, которая представляет собой сталеплавильную технологическую операцию, при которой концентрация (активность) кислорода, растворенного в жидкой стали, снижается до необходимого уровня. В дополнение к производству качественной стали за счет устранения пузырей и минимизации неметаллических включений раскисление также используется для контроля размера зерна для повышения ударной вязкости стали.
Было разработано несколько стратегий раскисления стали. Это может быть достигнуто путем добавления металлических раскислителей в жидкую сталь либо до, либо после ее выпуска, или путем вакуумной обработки, при которой углерод, растворенный в стали, является раскислителем. Помимо раскисления металлическими раскислителями и раскисления вакуумом, иногда применяют еще один метод раскисления, а именно диффузионное раскисление.
По степени раскисления различают четыре типа раскисления:от полностью раскисленного до слабо раскисленного. Ни один из различных типов не лучше другого, но каждый полезен по-своему. По степени раскисления углеродистые стали можно разделить на четыре группы.
- Римминговые стали – эти стали представляют собой частично раскисленные или нераскисленные низкоуглеродистые стали, выделяющие достаточное количество монооксида углерода во время затвердевания. Слитки кантованных сталей характеризуются хорошим качеством поверхности и большим количеством газовых раковин. Стали с каймой обычно разливают без добавления раскислителей в сталь в печи или только с небольшими добавками в жидкую сталь в разливочном ковше, чтобы иметь достаточное количество кислорода для обеспечения желаемого выделения газа за счет реакции в литейной форме с углеродом. . Точные применяемые процедуры зависят от того, имеет ли сталь содержание углерода в более высоких диапазонах (C =от 0,12 % до 0,15 %) или в более низких диапазонах (C =0,10 % макс.). Когда жидкая сталь в изложнице начинает затвердевать, происходит активное выделение газа монооксида углерода (CO), в результате чего внешняя корка слитка состоит из относительно чистой стали с низким содержанием углерода и других растворенных веществ. Такие слитки лучше всего подходят для изготовления электродных стержней и стальных листов.
- Сталь с защитным кожухом. Применение стали с защитным покрытием – это разновидность стальной кромки. Действие закраивания может начаться нормально, но затем прекращается через минуту или более, закрывая литейную форму чугунной крышкой. Эта практика обычно применяется в сталях с содержанием углерода более 0,15 %. Практика слитков с крышками обычно находит применение в производстве листов, полос, проволоки и прутков.
- Полуспокойные стали. Эти стали представляют собой не полностью раскисленные стали, содержащие некоторое количество избыточного кислорода, который реагирует с углеродом, образуя достаточное количество монооксида углерода во время затвердевания жидкой стали, чтобы компенсировать усадку при затвердевании. Эти стали обычно имеют содержание углерода в диапазоне от 0,15 % до 0,30 % и находят широкое применение в конструкционных формах
- Спокойные стали – эти стали раскислены до такой степени, что при затвердевании не происходит образования и выделения монооксида углерода. Слитки и отливки из спокойной стали имеют однородную структуру и не имеют газовой пористости (пузырей). Алюминий используется для раскисления вместе с ферросплавами марганца и кремния. В некоторых случаях применяют силицид кальция или другие специальные сильные раскислители. Чтобы свести к минимуму количество трубопроводов, почти все спокойные стали отливают в литейные формы с большими торцами с горячей крышкой. При непрерывной разливке жидкая сталь должна быть полностью раскислена для бездефектной разливки. Спокойные стали обычно используются, когда требуется однородная структура готовых сталей. Легированные стали, стали для ковки и стали для науглероживания относятся к этому типу, когда основным качеством является прочность. При производстве некоторых сталей сверхглубокой вытяжки низкоуглеродистая (C =0,12 % макс.) сталь раскисляется, обычно со значительным количеством алюминия, который добавляется в ковше, в литейную форму или и то, и другое. Хотя раскисление стали алюминием подавляет образование монооксида углерода во время затвердевания и, следовательно, подавляет газовые выбросы, существует множество операций обработки стали, при которых раскисление стали алюминием нежелательно.
В основном при раскислении стали используются три элемента. Это марганец (Mn), кремний (Si) и алюминий (Al). Марганец и кремний добавляют в виде высокоуглеродистых или низкоуглеродистых ферросплавов или в виде кремнемарганцевого (Si-Mn) сплава. Алюминий, добавляемый для раскисления, имеет уровень чистоты около 98 %. Иногда для раскисления также используется кальций (Ca).
Кальций является наиболее эффективным раскислителем, а Si менее эффективен по сравнению с Ca. Al также является сильным раскисляющим элементом по сравнению с Si. Хотя Ca и Al являются очень эффективными раскислителями, но они очень быстро окисляются и, кроме того, их плотность намного ниже, чем у стали. Также Ca имеет температуру кипения 1485°C, что означает, что Ca находится в газовой фазе при температуре выплавки стали. Для раскисления с помощью Ca необходимы подходящие методы впрыска или методы добавления.
Раскисление можно проводить либо одним элементом, таким как Si, Al, Mn и т. д., либо смесью элементов, таких как Si + Mn, Ca-Si-Al и т. д. Раскисление одним элементом известно как простое раскисление.
Тогда как раскисление смесью элементов известно как сложное раскисление. Как при простом, так и при сложном раскислении образуется оксид; поэтому его также называют раскислением осаждением. Раскисление также осуществляется углеродом под вакуумом; который называется вакуумным раскислением. Элементы добавляются в виде ферросплавов Fe-Si, Fe-Mn или Fe-Si + Fe-Mn и т. д. При комплексном раскислении, когда используется смесь Si + Mn, Ca + Si, Ca + Si + Al, сообщаются преимущества по сравнению с простым.
- Растворенный кислород ниже.
- Из-за образования жидкого продукта раскисления можно легко получить агломерацию продукта большого размера и легко флотировать.
Раскисление Fe-Mn
Когда сталь частично раскисляется Mn, железо также участвует в реакциях, образуя жидкий или твердый Mn (Fe) O в качестве продукта раскисления.
[Mn] + [O] =MnO
[Fe] + [O] =FeO
Состояние равновесия стали с продуктом раскисления Mn(Fe)O показано на рис. 1.
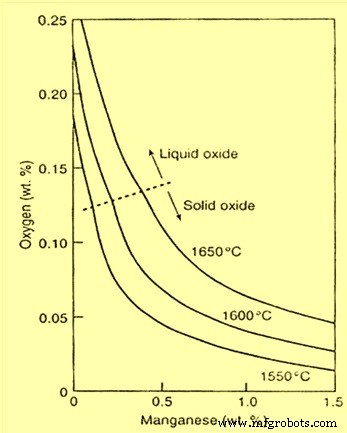
Рис. 1 Содержание марганца и кислорода в железе в равновесии с FeO – жидкий или твердый раствор MnO
Раскисление Si и Mn
Раскисление кремнием намного полнее, чем раскисление марганцем, и одновременное раскисление этими двумя элементами дает гораздо меньше остаточного кислорода в растворе из-за пониженной активности кремния. В зависимости от концентрации Si и Mn, добавляемых в сталь в разливочном ковше, продуктом раскисления будет либо расплавленный силикат марганца (MnO.SiO2), либо твердый кремнезем (SiO2).
[Si] + 2[O] =SiO2 (1)
[Mn] + [O] =MnO (2)
Одно из первых новаторских исследований равновесия реакции шлак-металл было приписано Корберу и Олсену за их измерение равновесного распределения Mn и Si между жидким железом и шлаком MnO-FeO-SiO2, насыщенным SiO2. Результаты их экспериментов при 1600 ± 10°С показаны на рис. 2.
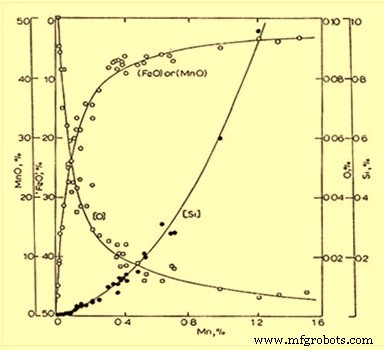
Рис. 2 Концентрация Mn, Si и O в жидком железе, уравновешенном SiO2. Насыщенный силикат марганца плавится при 1600 ± 10 град С
Раскисление кремнием, марганцем и алюминием
Полуспокойные стали с остаточным содержанием растворенного кислорода в пределах от 40 до 23 ppm получают путем раскисления стали в разливочном ковше с добавлением небольшого количества алюминия вместе с силикомарганцем или комбинацией ферросилиция и ферромарганца. В этом случае продуктом раскисления является жидкий марганцево-алюмосиликатный состав, близкий к 3MnO.Al2O3.SiO2. С небольшим добавлением алюминия, т.е. около 15 кг на 100 т тепла вместе с Si/Mn почти весь алюминий расходуется на это комбинированное раскисление с Si и Mn. Остаточный растворенный алюминий в стали будет менее 10 частей на миллион. Равновесия раскисления с Si и Mn по сравнению с Al, Si и Mn для продукта раскисления, насыщенного Al2O3, показаны на рис. 3.
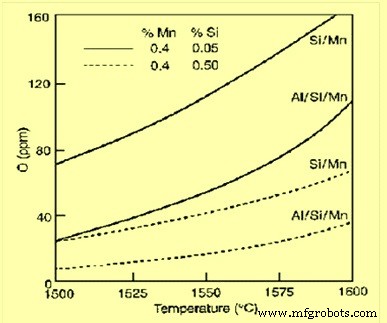
Рис. 3. Равновесия раскисления с Si и Mn по сравнению с Al, Si и Mn для продукта раскисления, насыщенного Al2O3
Раскисление алюминием
Алюминий является очень эффективным раскислителем, который используется в большинстве сталеплавильных операций. Обычно раскисление алюминия проводят в разливочных ковшах. В некоторых случаях добавки Al также делают в литейной форме во время слиткового или непрерывного литья. Видимые соотношения равновесия для продуктов раскисления:чистого Al2O3 и расплавленного алюмината кальция с соотношением CaO/Al2O3, равным 1, показаны на рис. 4.
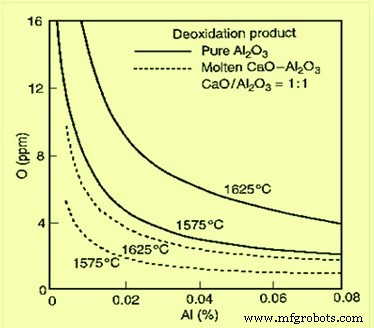
Рис. 4. Раскисление Al в равновесии с Al2O3 или жидким алюминатом кальция с CaO/Al2O3, равным 1
Когда раскисленную алюминием сталь обрабатывают Ca-Si, включения оксида алюминия превращаются в расплавленный алюминат кальция. При соотношении CaO/Al2O3, равном 1, активность Al2O3 составляет 0,064 по отношению к чистому Al2O3 при температурах в диапазоне 1500–1700 °C.
Производственный процесс
- Какие продукты сделаны из углеродистой стали?
- Стальная вата
- Ножницы
- Цинк
- Различия между углеродистой сталью и нержавеющей сталью
- Типы стали — Руководство по покупке Томаса
- Что такое высокоуглеродистая нержавеющая сталь?
- Что такое среднеуглеродистая сталь?
- Углеродистая сталь ASTM A595 класса A
- Углеродистая сталь ASTM A595 класса B



