Коррозия стальной арматуры в бетоне
Коррозия стальной арматуры в бетоне
Железобетон (ЖБ) представляет собой композиционный материал, состоящий из стальных арматурных стержней (арматурных стержней), заделанных в бетонную массу. Арматурные стержни несут основную часть растягивающей нагрузки и придают определенную степень сопротивления растрескиванию бетону, который сам подвергается сжимающей нагрузке. Сталь в бетоне обычно находится в пассивном, не подверженном коррозии состоянии. Однако на практике не всегда достигаются некорродирующие, пассивные условия, из-за которых происходит коррозия арматуры. Коррозия арматуры имеет физические последствия, такие как снижение предела прочности и работоспособности бетонных конструкций. Коррозия стальной арматуры в бетоне является большой универсальной проблемой. Повреждение, вызванное коррозией, может в значительной степени снизить эксплуатационную надежность и структурную целостность ЖБ. Повреждение бетонной конструкции, вызванное коррозией, требует скорейшего ремонта или, в некоторых случаях, полной замены бетонной конструкции.
Всякий раз, когда арматура, встроенная в сталь, подвергается коррозии, продукты коррозии увеличивают ее объем. Все формы оксида и гидрооксида железа имеют удельный объем больше, чем у стали. Силы расширения, создаваемые коррозией стали, приводят к растрескиванию при растяжении и ржавчине бетона. Это, в свою очередь, приводит к снижению эксплуатационных качеств и структурной целостности бетона, помимо ухудшения его эстетики. Как только начнется коррозия, это только вопрос времени, когда бетонной конструкции будет нанесен совокупный ущерб, и она выйдет из строя задолго до расчетного срока службы.
Двумя основными причинами коррозии арматуры в бетоне являются (i) локальное разрушение пассивирующей пленки на стали под действием ионов хлора и (ii) общее нарушение пассивации за счет нейтрализации щелочности бетона из-за реакции с атмосферой. СО2 (углекислый газ). Основными факторами, влияющими на коррозию арматуры в RC, являются (i) потеря щелочности из-за карбонизации, (ii) потеря щелочности из-за хлоридов, (iii) трещины в бетоне из-за механической нагрузки, (iv) блуждающие токи, ( v) атмосферное загрязнение, (vi) пути проникновения влаги, (vii) водоцементное отношение, (viii) низкая прочность бетона на растяжение, (ix) электрический контакт с разнородными металлами и (x) коррозия из-за разницы в окружающей среде.
Электрохимическая природа коррозии стали в бетоне
Коррозию можно определить как износ или разрушение материала в результате реакции с окружающей средой. Это электрохимический процесс (рис. 1), который требует протекания электрического тока и многих химических реакций. Примером электрохимического процесса является гальванический элемент. Для работы электрохимической ячейки необходимы три основных элемента, а именно (i) анод, (ii) катод и (iii) электролит. Анод — это единица, производящая электроны, а катод — единица, потребляющая электроны. Электролит представляет собой среду, через которую может происходить ионный поток. Типичные реакции на аноде и катоде для коррозии железа:(i) анодная реакция Fe =Fe (++) + 2e(-) (окисление), катодная реакция 2H (+) + 2e(-) =H2 (восстановление) , и реакция деполяризации 2H(+) +2e(-) + 0,5 O2 =H2O.
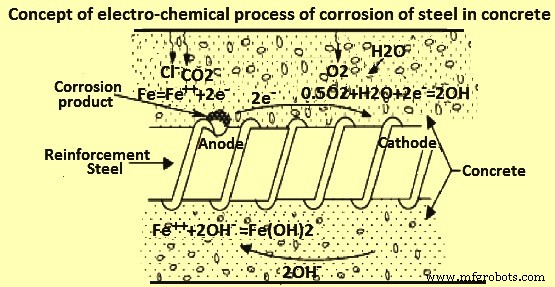
Рис. 1. Концепция электрохимического процесса коррозии арматуры в бетоне
На аноде металлическое железо (Fe) окисляется и генерируются электроны. Поскольку металл должен оставаться в состоянии электронного равновесия, равное количество электронов расходуется на катоде для образования газообразного водорода (H2). Газ H2 имеет тенденцию оставаться вблизи поверхности арматурного стержня, и реакция становится самотормозящейся. В этом случае говорят, что катод поляризован, и дальнейшая реакция невозможна, пока не будет удалена защитная пленка H2 (деполяризована). H2 может выделяться в виде газа, но обычно этот процесс протекает довольно медленно. Более важным является разрушение пленки H2 под действием деполяризующего действия кислорода (O2). В этом случае O2 предотвращает накопление газообразного H2, поглощая свободные электроны. Как только слой H2 разрушен, реакции коррозии продолжаются.
Поскольку ионы натрия и хлора в реакции не участвуют, суммарную реакцию можно выразить как сумму анодной реакции и реакции деполяризации. Использование реакции H2O =H(+) + OH(-) дает основную реакцию коррозии Fe + H2O + 0,5 O2 =Fe(OH)2. Осаждающееся соединение представляет собой гидроксид железа, форму ржавчины беловатого цвета. Однако в насыщенных кислородом растворах гидроксид железа дополнительно окисляется до гидроксида железа. В итоге образуется хорошо знакомая красновато-коричневая ржавчина
Тип коррозии арматуры
В арматуре, залитой в бетон, наблюдаются два типа коррозии. Это (i) щелевая коррозия и (ii) точечная коррозия. Щелевая коррозия представляет собой локальную форму коррозии, обычно связанную с застойным раствором на уровне микросреды. Такая застойная микросреда обычно возникает в щелях (защищенная зона). О2 в жидкости, находящейся глубоко в щели, расходуется на реакцию с металлом. Содержание O2 в жидкости в устье щели, которая подвергается воздействию воздуха, больше. Таким образом, формируется локальная ячейка, в которой анодом (областью атаки) является поверхность, контактирующая с обедненной кислородом жидкостью. В случае точечной коррозии теории пассивности делятся на две основные категории. Первый основан на адсорбции, а второй – на наличии тонкой оксидной пленки. Питтинговая коррозия в первом случае возникает из-за того, что вредные частицы или активаторы, такие как ион хлорида, конкурируют с ионом О2 или ионом гидроксила на определенных участках поверхности. В соответствии с теорией оксидной пленки вредные частицы внедряются в пассивную пленку, что приводит к ее локальному растворению или развитию проводящих путей. После возникновения язвы распространяются автокаталитически, что приводит к закислению активной области и ускоренной коррозии.
Механизм коррозии
В идеально однородной среде коррозия маловероятна. Однако железобетон ни в коем случае не является однородным материалом, и ячейки коррозии возникают при определенных условиях. Существует множество причин неоднородности бетона, усиливающей коррозию. Бетон может быть ячеистым, пористым, неравномерно влажным и сухим. Растрескивание вызывает различия в напряжении стали, дифференциальной аэрации и отложениях солей. В самом арматурном стержне всегда присутствуют неоднородности из-за начальных заблокированных остаточных напряжений и производственных процессов. В результате области с более низким потенциалом становятся анодными, а области с более высоким потенциалом — катодными. Влажный бетон действует как электролит, действие которого еще более усиливается при наличии ионов солей. Коррозия в железобетоне обычно подпадает под две основные группы, а именно (i) бетон с трещинами и (ii) бетон без трещин.
В случае свежего бетона без трещин обычно имеется достаточная стойкость к коррозионному воздействию. Бетонное покрытие арматуры очень эффективно предотвращает проникновение коррозионно-активных веществ на уровень стали. Очевидно, что чем толще и плотнее бетонный слой, тем эффективнее он противостоит коррозии. Кроме того, свежий бетон имеет очень высокое значение pH, что обычно препятствует коррозионным реакциям. Число рН является показателем кислотности или щелочности среды. Цифры от 0 до 7 указывают на кислотность раствора (при которой коррозия усиливается), а цифры от 7 до 14 указывают на щелочность раствора (при которой коррозия замедляется). Свежий бетон имеет высокое содержание Ca(OH)2 (гидроксида кальция), что придает ему pH около 13. Последней защитой от коррозии является синяя оксидная пленка (прокатная окалина) вокруг поверхности арматуры. Эта оксидная пленка предотвращает прямой контакт коррозионных агентов с голым металлом. Таким образом, прокатная окалина обеспечивает локальную защиту от коррозии.
Однако с течением времени вышеуказанные условия имеют тенденцию меняться. Вода, соль, O2, CO2 и промышленные газы (при наличии) начинают медленно проникать в бетон, скорость которого зависит от проницаемости бетонного покрытия. CO2, который проникает в бетон через поры и трещины, вступает в реакцию с Ca(OH)2 с образованием карбоната кальция. Таким образом, снижается как значение рН, так и защитные свойства бетона. Общий механизм возникновения коррозии в бетоне показан на рис. 2.
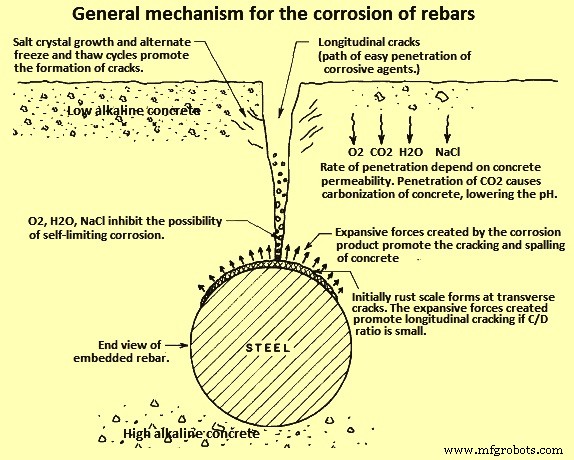
Рис. 2. Общий механизм коррозии арматуры
Вероятность коррозии высока, когда рН бетона падает до 8. Кристаллизация соли и эффекты замораживания-оттаивания создают внутренние силы, которые неблагоприятно влияют на долговечность бетонного покрытия. Когда коррозионная среда достигает стали, она концентрирует свое воздействие на дефектах оксидной пленки. Что еще более важно, если соль присутствует, она разрушает пассивность оксидной пленки на стали, что способствует коррозии.
Очевидно, что при больших трещинах в бетоне фаза проникновения вышеописанной последовательности значительно короче, и коррозия быстро начинается на стали ниже трещин. В участках бетона без трещин происходит та же последовательность, что и описанная, но с гораздо меньшей скоростью. То есть коррозия начинается, как только среда, способствующая коррозии, проникает через бетон до уровня стали.
Следует помнить, что присутствие соли является важным фактором в процессе коррозии. Ионы соли разрушают пассивность стали, создают ячейки коррозии и повышают электропроводность электролита. Без ионов соли коррозию арматуры в бетоне можно остановить на длительный период времени. В этом случае скорость коррозии обычно контролируется процессами карбонизации. Если бетонное покрытие является относительно непроницаемым и толстым, коррозия вообще не может возникнуть в местах без трещин. Однако трещины в этом случае не теряют своего значения, так как под ними может возникнуть локальная коррозия.
Образовавшиеся продукты коррозии, как правило, оказывают ингибирующее действие на продолжающиеся коррозионные реакции. Эти продукты могут изолировать основной металл от диффузии O2 и H2 и, таким образом, остановить реакции коррозии. Этот процесс известен как самоограничивающаяся коррозия. Самоограничивающаяся коррозия может иметь место при высоком соотношении C/D (толщина защитного слоя/диаметр арматуры), которое, по-видимому, определяет возникновение и степень продольного расщепления вдоль арматуры. Продольное расщепление происходит в основном из-за сил растяжения, создаваемых продуктами коррозии, которые занимают примерно в три раза больший объем, чем сталь, из которой они сформированы. Если защитный слой бетона не способен противостоять таким силам, образуются продольные трещины, через которые O2 и другие внешние агенты получают доступ к стали. На данный момент это только вопрос времени, когда конструкция достигнет опасного состояния коррозии и подлежит ремонту или замене. Повторные нагрузки также могут играть роль в нарушении защитного эффекта коррозионной корки, но необходимы дополнительные исследования, чтобы установить их важность.
Сталь термодинамически нестабильна в земной атмосфере и, следовательно, всегда имеет тенденцию возвращаться в более низкое энергетическое состояние, такое как оксид или гидроксид, в результате реакции с O2 и водой. Эти процессы происходят непрерывно. Вопрос, представляющий интерес в использовании стали, заключается в том, чтобы контролировать эти процессы, чтобы они происходили на практике. К счастью, только поверхностные атомы стали подвергаются воздействию атмосферы и, следовательно, доступны для реакции. В случае стержня диаметром 15 мм это составляет всего около 1 на каждые 40 миллионов атомов. Любое покрытие на стали еще больше снижает это число.
Для стали, встроенной в бетон, сам бетон обеспечивает покрытие, ограничивающее доступ воды и O2 к стальной поверхности. Вторым полезным аспектом бетона является то, что раствор в порах цементного теста имеет очень высокую щелочность и, как показано на диаграмме Пурбе на рис. 3, при уровнях pH, типичных для бетона, продукты коррозии, которые образуются, нерастворимы. . Они создают очень тонкое (около нескольких нанометров) защитное покрытие на стали (пассивная пленка), которое ограничивает потерю металла с поверхности стали из-за коррозии примерно от 0,1 до 1,0 микрометра в год. Обычно считается, что при этих скоростях пассивной коррозии сталь, залитая в бетон, обычно не подвергается заметной деградации в течение 75-летнего срока службы, а объем продуктов коррозии недостаточен для того, чтобы вызвать какие-либо повреждающие напряжения в бетоне. Пассивная пленка образуется не сразу, а начинается, как только pH воды затворения повышается в бетоне, когда цемент начинает гидратироваться и стабилизируется в течение первой недели, чтобы защитить сталь от активной коррозии.
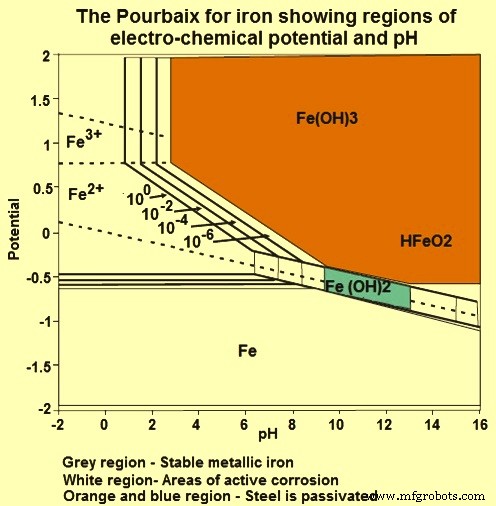
Рис. 3. Диаграмма Пурбе железа
Коррозия, будь то с незначительной пассивной скоростью или с разрушающей активной скоростью, является электрохимическим процессом, включающим установление анодных и катодных полуэлементных реакций на микроскопическом и/или макроскопическом уровнях. В растворах с высоким pH и в отсутствие ионов хлорида реакция анодного растворения железа уравновешивается катодной реакцией, в которой ионы Fe2+ объединяются с ионами OH-, образуя стабильную пассивную пленку.
Для одновременного протекания процесса коррозии необходимы как анодная, так и катодная реакции. Аноды могут быть расположены рядом друг с другом или могут быть разделены. Когда они расположены непосредственно рядом друг с другом, то есть в микроскопическом масштабе, возникающая коррозионная ячейка называется микроячеистой коррозией. Когда они разделены некоторым конечным расстоянием, возникающая коррозионная ячейка называется макроячеистой коррозией. Коррозия арматуры в бетоне может быть вызвана комбинацией микроячеистой и макроячеистой коррозии. На рис. 4 показана микроячеистая и макроячеистая коррозия арматурных стержней в бетоне.
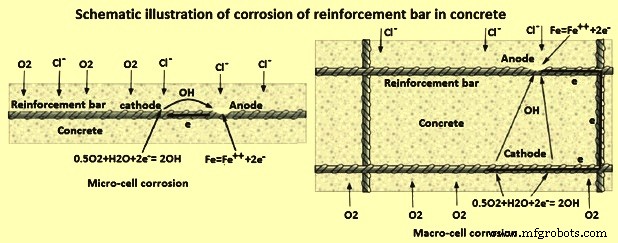
Рис. 4. Микро- и макроячеистая коррозия арматуры в бетоне
Коррозия, вызванная хлоридами
Механизм, с помощью которого ионы хлорида разрушают пассивную пленку, до конца не изучен, в основном потому, что пленка слишком тонкая, чтобы ее можно было исследовать, и потому, что события происходят внутри бетона. Одна из гипотез состоит в том, что ионы хлора внедряются в пассивную пленку и снижают ее сопротивление. Это включение неравномерно и, если оно происходит, способствует более быстрой реакции и образованию анодной зоны, где коррозия продолжается, а оставшаяся часть стали остается пассивной (рис. 5b).
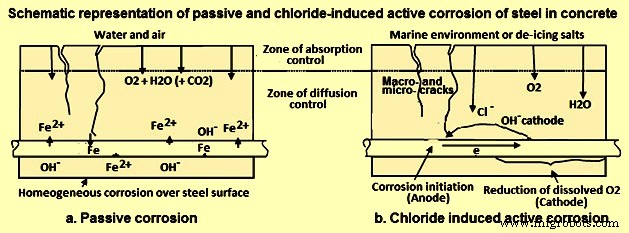
Рис. 5. Схематическое изображение пассивной и активной коррозии, вызванной хлоридами
Вторая гипотеза состоит в том, что ионы Cl- «конкурируют» с анионами OH- за соединение с катионами Fe2+ и, поскольку ионы Cl- образуют растворимые комплексы с ионами Fe2+, пассивная пленка не образуется и процесс стимулирует дальнейшее растворение металла. . Растворимые комплексы железа и хлорида диффундируют из стали и впоследствии разрушаются, что приводит к образованию экспансивных продуктов коррозии и одновременному высвобождению ионов Cl-, которые затем могут мигрировать обратно к аноду и далее реагировать со сталью. В этом общем процессе ионы гидроксила постоянно потребляются, локально снижая pH (т.е. делая раствор кислым в этой локализованной области) и, таким образом, усиливая дальнейшее растворение металла. Ионы Cl-, с другой стороны, не расходуются, и тогда атака становится «автокаталитической». В конечном итоге поперечное сечение арматуры и ее структурная прочность серьезно ухудшаются.
Любой из этих гипотетических механизмов объясняет часто наблюдаемый локальный характер приступа. Локальные активно корродирующие участки ведут себя как аноды, а оставшиеся пассивные участки становятся катодами, где происходит восстановление растворенного O2. Гальванические элементы могут быть макро- или микромасштаба в зависимости от ряда факторов. Таким образом, анод и катод могут быть далеко друг от друга или соседствовать на атомном уровне.
Зависимость коррозии арматуры от времени
Процесс коррозии арматуры имеет три различных этапа (i) инициирование, (ii) депассивация и (iii) распространение. Инициация предшествует депассивации, за которой следует распространение до конечного состояния (рис. 6). После инициации на внешней поверхности бетона появляется трещина, которая распространяется и приводит к дальнейшему повреждению и развитию. Срок службы определяется, когда арматурный стержень достигает конечного состояния, когда начинается отслаивание бетона.
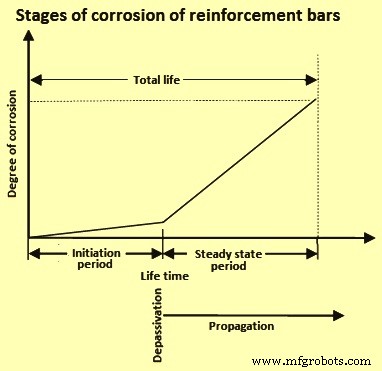
Рис. 6. Стадии коррозии арматуры
Продукты коррозии
Наиболее пагубным последствием хлоридной коррозии арматуры является накопление в бетоне объемистых нерастворимых продуктов коррозии, что приводит к возникновению внутренних напряжений и, в конечном итоге, к растрескиванию и отслаиванию бетонного покрытия. Ясно, что, как только такое повреждение становится очевидным визуально, арматура подвергается очень быстрому дальнейшему коррозионному воздействию, потому что доступ к O2 и влаге больше не ограничивается диффузией через защитный слой бетона. Все формы оксидов и гидроксидов железа имеют высокие удельные объемы, превышающие объем стали арматурного стержня (рис. 7). Таким образом, степень повреждения бетона определенным количеством коррозии зависит от специфики образующихся продуктов коррозии и их распределения в защитном слое бетона, а также от пористости и прочности самого бетона.
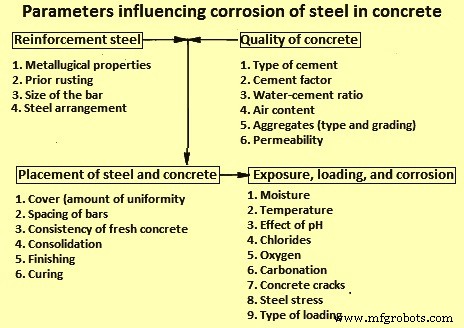
Рис. 7 Удельный объем продуктов коррозии железа
Иногда предполагают, что продукты коррозии представляют собой ржавчину, т.е. Fe2O3.3H2O, и поэтому на поврежденном бетоне наблюдается продукт оранжевого цвета. Следовательно, также предполагается, что продукты коррозии более чем в шесть раз превышают объем стали, из которой они образуются, и на этом выводе основаны прогнозируемые напряжения в бетоне. Фактически, анализ образовавшихся продуктов показывает, что существуют и другие продукты, как показано на рис. 7, которые имеют удельный объем в диапазоне от 2,2 до 3,3 раз больше, чем у стали. И только после растрескивания и сколов и, соответственно, воздействия атмосферы эти изделия превращаются в привычную нам ржавчину.
Параметры, влияющие на коррозию стали в бетоне
Параметры, влияющие на коррозию стали в бетоне, показаны на рис. 8. К параметрам, связанным со сталью, относятся металлургические свойства, предварительное ржавление, размер стержня и расположение стали.

Рис. 8. Параметры, влияющие на коррозию стали в бетоне
Металлургические свойства – Наверное, общеизвестно, что многие элементы, легированные сталью, обладают повышенной коррозионной стойкостью. Основные элементы, замедляющие коррозию, включают медь (Cu), никель (Ni) и хром (Cr), большинство из которых присутствует в стали для арматуры в незначительных количествах. Было обнаружено, что определенные комбинации этих и других элементов улучшают коррозионную стойкость сталей, но с практической точки зрения мало влияют на применение арматурной стали в бетоне.
Локализованные металлургические различия в атомной структуре стали вызывают дифференциальные энергетические поля внутри стали и способствуют образованию анодной и катодной областей, необходимых для электрохимической коррозии. Эти области, по сути, представляют собой разные материалы, соприкасающиеся друг с другом. Энергетические поля обычно связаны с дислокациями, несогласованными границами зерен, включениями, примесями, границами металлургических фаз и т. д. Например, установлено, что ферритная фаза стали легко подвергается коррозии, а цементит устойчив к коррозии. Там, где обе фазы соседствуют друг с другом, цементит становится катодом, а феррит становится анодом, и развивается коррозионная ячейка.
Следует признать, что источники дифференциального энергетического поля для коррозионных ячеек присутствуют во всех коммерческих сталях, и, следовательно, должны быть найдены средства ингибирования коррозии, отличные от попыток гомогенизировать стали, что нецелесообразно и имеет сомнительную эффективность. По этой причине хорошо, что влияние этих различных энергетических полей на коррозию арматурной стали минимально, пока рН окружающего бетона остается относительно высоким (в диапазоне от 10 до 13).
В дополнение к источникам коррозионных ячеек, связанных с базовой атомной структурой стали, поверхность арматурного стержня предлагает дополнительные возможности для образования ячеек. Такие факторы, как шероховатость поверхности, царапины, порезы и особенно прокатная окалина, часто являются причиной возникновения коррозии. Если прокатная окалина, образовавшаяся во время горячей прокатки стали, не приводит к сплошному покрытию окалиной, то участки поверхности, покрытые прокатной окалиной, являются катодными по отношению к непокрытым прилегающим областям.
В некоторых случаях металлические покрытия обеспечивают защиту стальных поверхностей от коррозии. Однако такие катодные покрытия, как Ni и Cu, неэффективны для арматурных сталей, поскольку они относительно дороги и могут быть повреждены во время строительства, что создает серьезные условия локальной коррозии. Кадмий (Cd) и цинк (Zn) являются анодами стали и могут использоваться в качестве расходуемых покрытий. Оцинкованные покрытия на арматуре, возможно, практичны, но чтобы они были эффективными, покрытие должно быть достаточной толщины.
Предварительная ржавчина арматуры – Большое влияние оказывает состояние арматуры перед заделкой. В некоторых стандартах требуется, чтобы рыхлая «чешуйчатая» ржавчина должна быть удалена с арматурной стали перед использованием, а обычное грубое обращение обычно удаляет вредную ржавчину. С другой стороны, некоторые другие стандарты менее строги в отношении предварительной ржавчины арматурных стержней, поскольку разрешено использование предварительно проржавевшей арматуры при условии соблюдения требований по высоте деформации, размерам и весу зачищенного стержня.
Кроме того, сообщалось, что нормальная ржавчина фактически увеличивает сцепление. Также было обнаружено, что для 14-дневного бетона использование ранее проржавевшей сварной сетки приводило к меньшему проскальзыванию связи по сравнению с чистой проволокой. Однако долгосрочные последствия использования ранее проржавевшей арматуры четко не определены. Это особенно важно для открытых конструкций. На самом деле было высказано предположение, что предшествующая ржавчина предварительно напряженных напрягаемых элементов может вызвать серьезную коррозию после заливки в бетонный раствор. Та же проблема может быть выражена в отношении ранее проржавевших арматурных стержней в открытых элементах конструкции.
Размер стержня и расположение стали – Относительно мало исследований коррозии, в которых учитывались переменные, связанные с размером стержня и расположением стали. В одном исследовании было установлено, что сварная сетка из арматурных стержней подвержена коррозии не больше, чем арматурные стержни с индивидуальной изоляцией. В другом исследовании было замечено, что существует взаимосвязь между расстоянием между стержнями и растрескиванием, вызванным коррозией. В этом исследовании арматурные стержни, расположенные на расстоянии 300 мм друг от друга, как правило, образовывали канавки, в то время как арматурные стержни, расположенные на расстоянии 150 мм друг от друга, имели тенденцию к образованию ослабленных плоскостей.
Профилактические меры
Для уменьшения и предотвращения коррозии арматурных стальных стержней в бетоне используется несколько методов. Некоторые из них связаны с производством бетона, в то время как другие связаны с качеством, составом и покрытием стали, используемой для изготовления арматурных стержней. Обычно выбор делается по цене. На арматуру наносят следующие покрытия:(i) горячее цинкование погружением, (ii) эпоксидное покрытие, наплавляемое, и (iii) плакирование из нержавеющей стали. Применяются также арматурные стержни из нержавеющей стали. Покрытия имеют тот недостаток, что покрытия могут быть физически повреждены или подвергнуты электрохимическому проникновению, так что основная сталь снова становится уязвимой для обычного процесса коррозии. Также были опробованы стальные арматурные стержни специального состава для защиты от коррозии. Несколько сталелитейных заводов экспериментировали с различными составами атмосферостойких сталей. Однако после обширных испытаний было обнаружено, что атмосферостойкие стали постоянно плохо работают при захоронении. Следовательно, большинство производителей отказались от производства стальной арматуры.
Производственный процесс
- Почему сталь корродирует (и способы ее предотвращения)
- Стальная вата
- Бетонная плотина
- Защита от коррозии и облегчение транспортных средств
- Почему нержавеющая сталь устойчива к коррозии?
- Коррозионное растрескивание нержавеющей стали 316L под напряжением в процессе эксплуатации в H2S
- Что такое стальная опалубка?
- EN 10216-5 Марка X1NiCrMoCuN25-20-7 отожженный раствор (+AT)
- S32550 / AMAZON 256 Дуплексная нержавеющая сталь
- S31803 / COLDUPLEX Дуплексная нержавеющая сталь



