Измерение pH
Очень важным измерением во многих жидких химических процессах (промышленных, фармацевтических, производственных, пищевых и т. Д.) Является измерение pH:измерение концентрации ионов водорода в жидком растворе. Раствор с низким значением pH называется «кислотой», а раствор с высоким значением pH - «щелочью». Обычная шкала pH простирается от 0 (сильная кислота) до 14 (сильная щелочь), где 7 в середине представляет чистую воду (нейтральную):
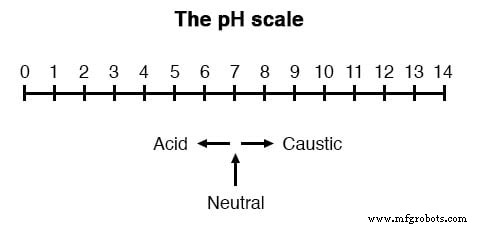
Значение pH определяется следующим образом:строчная буква «p» в значении pH обозначает отрицательный общий логарифм (с основанием десять), а заглавная буква «H» обозначает элемент водород. Таким образом, pH - это логарифмическое измерение количества молей ионов водорода (H +) на литр раствора. Между прочим, префикс «p» также используется с другими типами химических измерений, где желательна логарифмическая шкала, двумя такими примерами являются pCO2 (углекислый газ) и pO2 (кислород).
Логарифмическая шкала pH работает так:раствор с 10 -12 молей ионов H + на литр имеет pH 12; решение с 10 -3 молей ионов H + на литр имеет pH 3. Хотя это очень редко, существуют такие вещи, как кислота с показателем pH ниже 0 и щелочь с pH выше 14. Понятно, что такие растворы довольно концентрированы и чрезвычайно реактивный.
pH-электроды
В то время как pH можно измерить по изменению цвета некоторых химических порошков («лакмусовая бумажка» - знакомый пример из школьных уроков химии), непрерывный мониторинг процесса и контроль pH требует более сложного подхода. Наиболее распространенным подходом является использование специально подготовленного электрода, предназначенного для того, чтобы ионы водорода в растворе могли мигрировать через селективный барьер, создавая измеримую разность потенциалов (напряжений), пропорциональную pH раствора:
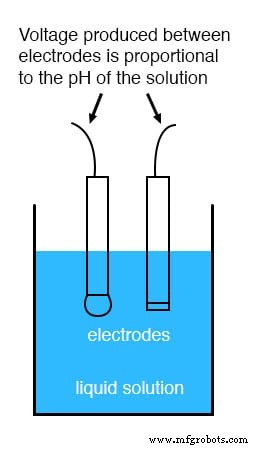
Конструкция и теория работы pH-электродов - очень сложный предмет, который здесь рассматривается лишь кратко. Важно понимать, что эти два электрода генерируют напряжение, прямо пропорциональное pH раствора. При pH 7 (нейтральный) между электродами будет 0 вольт. При низком pH (кислотном) будет развиваться напряжение одной полярности, а при высоком pH (щелочь) будет развиваться напряжение противоположной полярности.
Измерительный электрод
К сожалению, конструктивное ограничение pH-электродов заключается в том, что один из них (называемый измерением электрод) должен быть изготовлен из специального стекла для создания ионоселективного барьера, необходимого для экранирования ионов водорода от всех остальных ионов, плавающих в растворе. Это стекло химически легировано ионами лития, что заставляет его электрохимически реагировать с ионами водорода. Конечно, стекло - не совсем то, что вы бы назвали «проводником»; скорее, это очень хороший изолятор.
Это представляет собой серьезную проблему, если мы намереваемся измерить напряжение между двумя электродами. Путь цепи от контакта одного электрода через стеклянный барьер, через раствор к другому электроду и обратно через контакт другого электрода является одним из чрезвычайно высокое сопротивление.
Электрод сравнения
Другой электрод (называемый эталонным электрод) изготовлен из химического раствора нейтрального (7) буферного раствора pH (обычно хлорида калия), позволяющего обмениваться ионами с технологическим раствором через пористый сепаратор, образуя соединение с испытательной жидкостью с относительно низким сопротивлением. Сначала можно спросить:почему бы просто не окунуть в раствор металлический провод, чтобы обеспечить электрическое соединение с жидкостью? Причина, по которой это не сработает, заключается в том, что металлы, как правило, обладают высокой реакционной способностью в ионных растворах и могут создавать значительное напряжение на границе контакта металла с жидкостью.
Использование влажной химической поверхности раздела с измеряемым раствором необходимо, чтобы избежать создания такого напряжения, которое, конечно, было бы ошибочно интерпретировано любым измерительным устройством как показывающее pH.
Вот иллюстрация конструкции измерительного электрода. Обратите внимание на тонкую стеклянную мембрану с добавлением лития, через которую создается pH-напряжение:
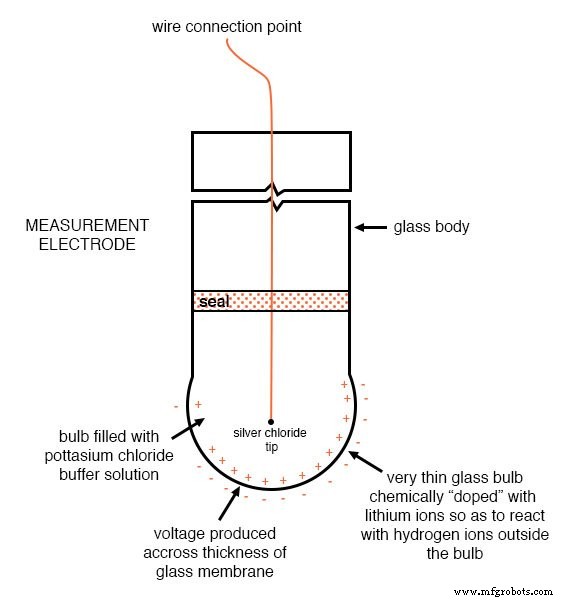
Вот иллюстрация конструкции электрода сравнения. Пористое соединение, показанное в нижней части электрода, - это место, где буфер хлорида калия и технологическая жидкость соприкасаются друг с другом:
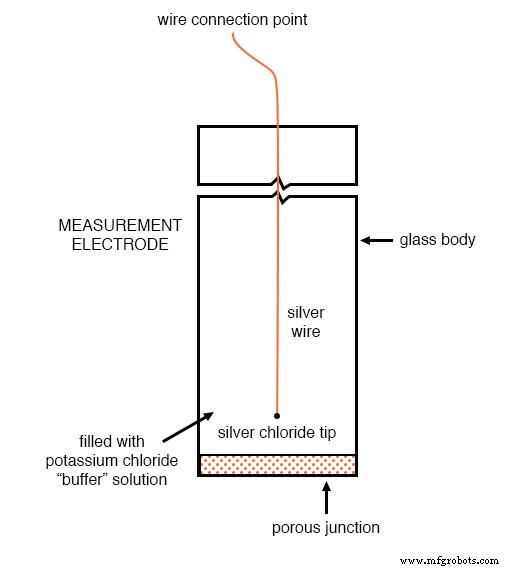
Назначение измерительного электрода - генерировать напряжение, используемое для измерения pH раствора. Это напряжение появляется по всей толщине стекла, помещая серебряный провод с одной стороны напряжения, а жидкий раствор - с другой. Задача электрода сравнения - обеспечить стабильное соединение без напряжения с жидким раствором, чтобы можно было создать полную схему для измерения напряжения стеклянного электрода.
В то время как соединение электрода сравнения с испытательной жидкостью может составлять всего несколько киломов, сопротивление стеклянного электрода может составлять от десяти до девяти сотен мегаом, в зависимости от конструкции электрода! Поскольку любой ток в этой цепи должен проходить через оба сопротивление электродов (и сопротивление, представленное самой испытательной жидкостью), эти сопротивления включены последовательно друг с другом и, следовательно, складываются, чтобы получить еще большую сумму.
Обычный аналоговый или даже цифровой вольтметр имеет слишком низкое внутреннее сопротивление для измерения напряжения в такой цепи с высоким сопротивлением. Эквивалентная принципиальная схема типичной цепи датчика pH иллюстрирует проблему:
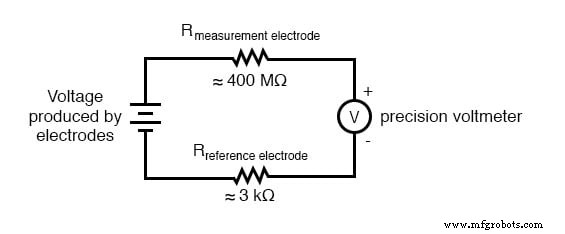
Даже очень небольшой ток в цепи, проходящий через высокое сопротивление каждого компонента в цепи (особенно стеклянную мембрану измерительного электрода), будет вызывать относительно значительные падения напряжения на этих сопротивлениях, серьезно снижая напряжение, видимое измерителем. Положение усугубляется тем, что перепад напряжения, создаваемый измерительным электродом, очень мал, в диапазоне милливольт (в идеале 59,16 милливольт на единицу pH при комнатной температуре). Измеритель, используемый для этой задачи, должен быть очень чувствительным и иметь чрезвычайно высокое входное сопротивление.
Наиболее распространенным решением этой проблемы измерения является использование измерителя с усилением с чрезвычайно высоким внутренним сопротивлением для измерения напряжения электрода, чтобы пропускать через цепь как можно меньший ток. Благодаря современным полупроводниковым компонентам вольтметр с входным сопротивлением до 10 17 Ω можно построить без особых трудностей. Другой подход, редко встречающийся в современном использовании, заключается в использовании потенциометрической схемы измерения напряжения с нулевым балансом для измерения этого напряжения без рисования каких-либо ток от тестируемой цепи. Если техник захочет проверить выходное напряжение между парой pH-электродов, это, вероятно, будет наиболее практичным способом сделать это с использованием только стандартного настольного измерительного оборудования:
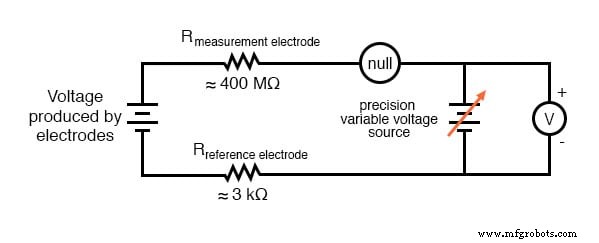
Как обычно, прецизионный источник напряжения будет регулироваться техником до тех пор, пока нуль-детектор не зарегистрирует ноль, затем будет просматриваться вольтметр, подключенный параллельно источнику питания, чтобы получить показания напряжения. Когда детектор «обнулен» (регистрирует точно ноль), в цепи pH-электрода должен быть нулевой ток и, следовательно, не должно падать напряжение на сопротивлениях любого из электродов, что дает реальное напряжение электрода на выводах вольтметра.
Требования к проводке pH-электродов, как правило, даже более жесткие, чем проводка термопар, требуя очень чистых соединений и коротких расстояний между проводами (10 ярдов или меньше, даже с позолоченными контактами и экранированным кабелем) для точных и надежных измерений. Однако, как и в случае с термопарами, недостатки измерения pH с помощью электродов компенсируются преимуществами:хорошей точностью и относительной технической простотой.
Немногие измерительные технологии вызывают трепет и таинственность, присущие измерению pH, потому что его так часто неправильно понимают и его трудно устранить. Не вдаваясь в подробности точной химии измерения pH, можно сказать несколько мудрых слов о системах измерения pH:
- Все pH-электроды имеют ограниченный срок службы, и этот срок в значительной степени зависит от типа и серьезности эксплуатации. В некоторых случаях срок службы pH-электрода составляет один месяц, а в других случаях срок службы одного и того же электрода (-ов) может составлять более года.
- Поскольку стеклянный (измерительный) электрод отвечает за генерирование напряжения, пропорционального pH, его следует рассматривать как подозрительный, если система измерения не может генерировать достаточное изменение напряжения для данного изменения pH (приблизительно 59 милливольт на pH ед.) или не реагирует достаточно быстро на быстрое изменение pH тестовой жидкости.
- Если система измерения pH «дрейфует», создавая ошибки смещения, проблема, скорее всего, связана с электродом сравнения, который должен обеспечивать соединение нулевого напряжения с измеряемым раствором.
- Поскольку измерение pH является логарифмическим представлением концентрации ионов, существует невероятный диапазон условий процесса, представленных на кажущейся простой шкале от 0 до 14 pH. Кроме того, из-за нелинейного характера логарифмической шкалы изменение на 1 pH на верхнем конце (скажем, с 12 до 13 pH) не представляет такое же изменение химической активности, как изменение на 1 pH на нижнем конце. (скажем, от 2 до 3 pH). Инженеры и технические специалисты систем управления должны знать об этой динамике, если есть надежда на контроль . pH процесса при стабильном значении.
- Следующие условия опасны для измерительных (стеклянных) электродов:высокие температуры, экстремальные уровни pH (кислотные или щелочные), высокая концентрация ионов в жидкости, истирание, плавиковая кислота в жидкости (HF кислота растворяет стекло!), и любое материальное покрытие на поверхности стекла.
- Температурные изменения в измеряемой жидкости влияют как на реакцию измерительного электрода на заданный уровень pH (в идеале - 59 мВ на единицу pH), так и на фактический pH жидкости. Устройства для измерения температуры могут быть вставлены в жидкость, и сигналы от этих устройств могут использоваться для компенсации влияния температуры на измерение pH, но это будет компенсировать только реакцию измерительного электрода в мВ / pH, а не фактическое изменение pH в технологическом процессе. жидкость!
В области измерения pH все еще наблюдаются успехи, некоторые из которых открывают большие перспективы для преодоления традиционных ограничений pH-электродов. В одной из таких технологий используется устройство, называемое полевым транзистором . для электростатического измерения напряжения, создаваемого ионопроницаемой мембраной, а не для измерения напряжения реальной схемой вольтметра. Хотя эта технология имеет собственные ограничения, это, по крайней мере, новаторская концепция, которая может оказаться более практичной в будущем.
ОБЗОР:
- pH - это показатель активности ионов водорода в жидкости. Это отрицательный логарифм количества ионов водорода (в молях) на литр жидкости. Таким образом:10 -11 молей ионов водорода в 1 литре жидкости =11 pH. 10 -5,3 молей ионов водорода в 1 литре жидкости =5,3 pH.
- Базовая шкала pH простирается от 0 (сильная кислота) до 7 (нейтральная, чистая вода) до 14 (сильная щелочь). Химические растворы с уровнем pH ниже нуля и выше 14 возможны, но редко.
- pH можно измерить путем измерения напряжения между двумя специальными электродами, погруженными в жидкий раствор.
- Один электрод, сделанный из специального стекла, называется измерительным . электрод. Его задача - создать небольшое напряжение, пропорциональное pH (в идеале 59,16 мВ на единицу pH).
- Другой электрод (так называемый эталон электрод) использует пористое соединение между измеряемой жидкостью и стабильным буферным раствором с нейтральным pH (обычно хлоридом калия) для создания электрического соединения с жидкостью при нулевом напряжении. Это обеспечивает непрерывность всей цепи, так что напряжение, создаваемое по толщине стекла измерительного электрода, может быть измерено внешним вольтметром.
- Чрезвычайно высокое сопротивление стеклянной мембраны измерительного электрода требует использования вольтметра с чрезвычайно высоким внутренним сопротивлением или вольтметра с нулевым балансом для измерения напряжения.
Промышленные технологии
- Дифференциальные уравнения
- Интеграция ЧМИ-ПЛК
- Что такое шероховатость поверхности? - единица, диаграмма, измерение
- Технология вставки монет как тепловое решение для печатных плат
- От начала до конца:основы измерения поверхности
- UGIPURE® 4472 Отожженный раствор
- UGIMA®-X 4305 Отожженный раствор
- UGI® 316Ti Отожженный раствор
- UGIPERM® 12FM Отожженный раствор
- UGIMA® 4598 Отожженный раствор



