Доменный шлак и его роль в работе печи
Доменный шлак и его роль в работе печи
Важность шлака доменной печи (ДП) для обеспечения бесперебойной работы доменной печи иллюстрируется старой поговоркой:«Если вы позаботитесь о шлаке, печь позаботится обо всем остальном». Было проделано огромное количество работ по доменному шлаку с изучением его свойств, механизмов образования и влияния на работу печи. Шлак хорошего качества необходим для получения качественного чугуна в доменной печи.
Практика использования доменного шлака необходима для выполнения определенных требований для эффективной работы доменной печи. Эти требования включают (i) поглощение всех невосстановленных нелетучих компонентов шихты и удаление их из доменной печи, (ii) наличие жидкости с низкой вязкостью, (iii) способность поглощать серу в основном содержится в топливе, (iv) оно должно содержать как можно меньшее количество оксида железа, чтобы увеличить выход чугуна, (v) его объем должен быть как можно меньше, не влияя на десульфурацию, ( vi) диапазон температур, в котором компоненты шихты становятся когезионными, должен быть узким для обеспечения лучшей проницаемости столба шихты, и (vii) ее качество должно быть таким, чтобы из нее можно было получить товарный материал. Эти требования частично дополняют друг друга, а частично исключают друг друга. Следовательно, необходимо указать приоритеты.
К счастью, существуют общие зависимости, дающие более практическое представление о природе шлаков, которые можно использовать ежедневно. Однако важно иметь общее представление о фундаментальной природе доменного шлака, чтобы понять общие взаимосвязи.
Основы доменного шлака
Основы доменного шлака сложны. Приблизительно 40 % кислород является самым большим элементом в шлаке. Следовательно, шлак представляет собой оксидную систему и имеет ионную природу. Из-за особенностей процесса доменной печи образование шлака представляет собой многостадийный процесс, включающий значительные изменения состава и температуры. Четыре основных компонента доменного шлака:SiO2 (кремнезем), CaO (известь), MgO (магнезия) и Al2O3 (глинозем). Эти четыре компонента шлака доменной печи образуют многочисленные соединения, обусловливающие широкий диапазон химических и физических свойств. Меньшие компоненты шлака представляют особый интерес с точки зрения химии чугуна, а управление печью усложняет физико-химические свойства шлака.
К основным шлакам доменной печи относятся вопросы, связанные с процессом доменной печи. Эти вопросы включают образование шлака, течение в горне, молекулярную структуру шлака и то, как структура связана с химическими показателями, известными как основность, затвердевание шлака и влияние изменений теплового состояния печи на состав шлака.
Шлакообразование – ДП представляет собой напорный противоточный теплообменный реактор с обратным холодильником, газ-твердо-жидкостный реактор с уплотненным слоем. Он выполняет три основные функции, а именно (i) восстановление оксидов железа до металлического железа (ii) плавление металлического железа и оксидов, что обеспечивает (iii) отделение примесей шихты и топлива от жидкого железа. Эти характеристики процесса приводят к разделению печи на три вертикальные зоны по отношению к шлакам (i), а именно (i) зернистая зона, (ii) зона образования шлака и (iii) зоны горна. Эти три зоны и некоторые специфические реакции для каждой зоны представлены на рис. 1.
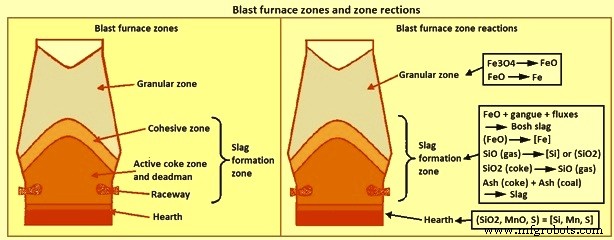
Рис. 1. Зоны доменной печи и реакции в зонах
Зерновая зона расположена в верхней части печи, где все загружаемые компоненты находятся в твердой фазе. Зернистая зона сверху ограничена линией стока, а снизу – началом образования жидких фаз – когезионной зоной. По мере спуска шихты через зернистую зону она нагревается газами из нижней части печи и осуществляется часть восстановления оксидов железа. Степень восстановления, происходящая в зернистой зоне, зависит от природы железосодержащих материалов, распределения шихты, состава газа и характера течения.
Зона шлакообразования начинается в когезионной зоне, где начинается разупрочнение шихты, и продолжается ниже уровня фурмы. Таким образом, зона образования шлака включает когезионную зону, зону активного кокса, мертвую зону и дорожку качения. Шлак, образующийся в верхней части зоны шлакообразования, называется «чашевым» или «первичным» шлаком, а шлак, выходящий из зоны внизу, — «подовым» шлаком. Обычно предполагается, что первичный шлак состоит из всех компонентов шихтового шлака, включая оксиды железа, не восстановленные в гранулированной зоне, но не включает золу от кокса или впрыскиваемого угля. Состав шлака изменяется по мере его опускания в печь за счет поглощения золы кокса и угольной золы, серы и кремния из газа, а также восстановления оксида железа. Температура шлака возрастает порядка 500°С по мере его опускания на фурменное возвышение. Эти изменения в составе и температуре могут значительно повлиять на физические свойства шлака, особенно на температуру ликвидуса и вязкость.
Третья зона – шлаковый слой горна печи. Шлак, образующийся в зоне шлакообразования, собирается в шлаковом слое, заполняя пустоты в горновом коксе и «плавая» по слою чугуна. Горячий металл проходит через слой шлака и достигает слоя горячего металла. Большая площадь поверхности между жидким металлом и шлаком при прохождении жидкого металла через слой шлака улучшает кинетику химических реакций. Эти реакции приводят к значительным изменениям в химическом составе чугуна. В частности, содержание [Si] и [S] перед входом в слой шлака намного выше, чем в слое горячего металла. Образование шлаков в зоне шлакообразования очень специфично для печи из-за влияния свойств шихты и работы печи.
Структура шлака – Представление о структуре шлака (рис. 2) основано на структуре, образованной кремнеземом. На молекулярном уровне атом кремния расположен в центре тетраэдра, окруженного четырьмя атомами кислорода, по одному атому кислорода в каждом углу тетраэдра, как показано на рис. 2а. Каждый атом кислорода связан с двумя атомами кремния, и, следовательно, каждый атом кислорода является углом двух тетраэдров. Совместное использование атомов кислорода приводит к полимеру или сети в трех измерениях в кристаллическом состоянии, где все углы являются общими (рис. 2b). При нагревании кремнезема некоторые угловые связи разрушаются, но полимерная природа структуры сохраняется даже в расплавленном состоянии, как показано на рис. 2c.
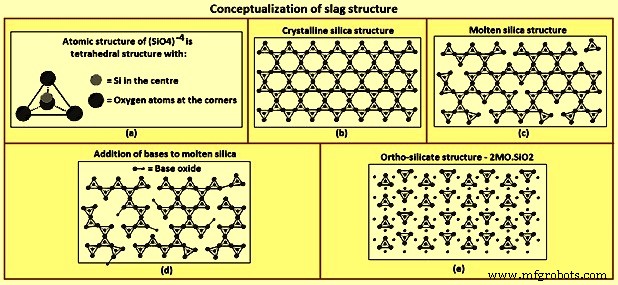
Рис. 2. Концептуализация структуры шлака
Добавление оксидов металлов, таких как CaO и MgO, разрушает структуру полимера. Эти оксиды действуют как доноры кислорода, замещая атом кислорода в одном углу тетраэдра и разрывая угловую связь тетраэдра с тетраэдром (рис. 2d). Разрушение структуры полимера продолжается с добавлением большего количества оксидов металлов до тех пор, пока молярное отношение оксидов металлов к кремнезему не станет равным двум, после чего все связи тетраэдра с тетраэдром разрываются (рис. 2e). Молярное соотношение двух составляет ортосиликатную композицию:2CaO-SiO2, 2MgO-SiO2 и CaO-MgO-SiO2. Al2O3 действует аналогично SiO2 при формировании полимеров и принятии атомов кислорода из основных оксидов. Оксиды, которые принимают кислород, SiO2 и Al2O3, называются кислотными оксидами. Оксиды, отдающие кислород, CaO и MgO, называются основными оксидами.
Основность шлака – Очень полезно при соотнесении свойств многокомпонентной системы с ее составом разработать индекс, основанный на составе. Проблема при разработке индекса заключается в том, как отразить в индексе значимость каждого компонента системы. Различная природа кислотных оксидов (А) и основных оксидов (В) использовалась при разработке показателей состава шлака, обычно называемых основностью. Примерами разработанных показателей основности являются (i) избыточные основания ={(CaO) + (MgO)} – {(SiO2) + (Al2O3)}, (ii) основность (B/A) ={(CaO) + (MgO)} / {(SiO2) + (Al2O3)}, (iii) коэффициент Белла ={(CaO) + 0,7(MgO)} / {0,94(SiO2)+ 0,18(Al2O3)} и (iv) оптическая основность ={(CaO) + 1,11 (MgO) + 0,915 (SiO2) + 1,03 (Al2O3)} / {(CaO) + 1,42 (MgO) + 1,91 (SiO2) + 1,69 (Al2O3)}.
Показатели основности можно сгруппировать в общие категории, а именно (i) различия между количеством оснований и кислот, как показано в уравнении (i) выше, (ii) отношения оснований к кислотам на основе весовых процентов, как показано в уравнении (ii) выше, (iii) отношения оснований к кислотам, основанные на молярных концентрациях, как показано в уравнении (iii) выше, и (iv) сумма основности каждого компонента и его молярной концентрации, как показано в уравнении (iv) выше. Как и следовало ожидать на основании предыдущего описания структуры шлака, те показатели, которые отражают молекулярную природу состава шлака, уравнения (iii) и уравнение (iv), имеют тенденцию быть лучшими предикторами свойств шлака. Однако, поскольку индекс, определяемый уравнением (ii), вероятно, является наиболее часто используемым определением.
Влияние температуры — [Si], основность и объем шлака – Количество [Si] увеличивается с увеличением температуры чугуна в доменной печи, как показано на рис. 3. Количество увеличения [Si] при заданном повышении температуры варьируется от печи к печи, но тенденция является одинаково для всех печей. По мере увеличения [Si] уменьшается (SiO2) и, следовательно, увеличивается основность и уменьшается объем шлака. Величина увеличения основности для конкретного увеличения [Si] зависит от объема шлака. На рис. 3а показано изменение B/A для начальных объемов шлака 200 кг/т ТМ (килограммов на тонну чугуна) и 300 кг/т ТМ, а также для соотношения [Si] и температуры чугуна, приведенного на рисунке. Продемонстрированная здесь нормальная тенденция заключается в том, что чем больше объем шлака, тем меньше изменение B/A при одном и том же изменении [Si] или температуры чугуна.
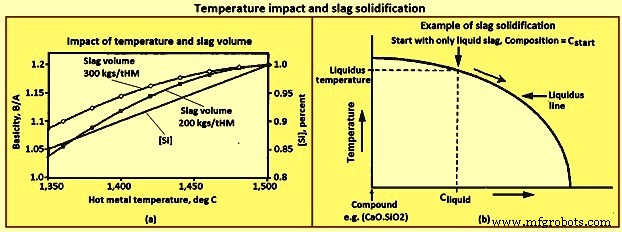
Рис. 3. Влияние температуры и затвердевание шлака
Затвердевание шлака – Общее определение температуры плавления применимо только к однокомпонентной системе, такой как вода, где выше температуры плавления существует только жидкая вода, а ниже температуры плавления – только твердая вода. Шлак представляет собой многокомпонентную систему и, следовательно, не имеет единого определения температуры плавления, за исключением конкретных составов. Большинство составов шлака имеют как твердую, так и жидкую фазы, присутствующие в диапазоне температур. Самая низкая температура, при которой существует только жидкая фаза для определенного состава, называется температурой ликвидуса.
На рис. 3b показан путь затвердевания шлака на упрощенной фазовой диаграмме. Начните со шлака состава Cstart при температурах, при которых существует только жидкий шлак. По мере остывания шлака, перемещаясь по диаграмме вертикально вниз, состав жидкого шлака не меняется до пересечения с «линии ликвидуса». Пересечение с «линии ликвидуса» – температура ликвидуса для состава Cstart. Очень небольшое количество твердого соединения образуется при температуре ликвидуса слева. При дальнейшем снижении температуры ниже температуры ликвидуса продолжаются три изменения, а именно (i) образуется больше твердого соединения, (ii) количество жидкого шлака уменьшается, и (iii) состав жидкого шлака изменяется, приближаясь к прямо по «линии ликвидуса». В примере, где образуется соединение 2CaO.SiO2, основность жидкого шлака уменьшается по мере его охлаждения, поскольку 2CaO.SiO2 содержит примерно в два раза больше CaO, чем SiO2.
Путь затвердевания показывает, как компаунд может образовываться, даже если состав жидкого шлака значительно отличается от состава компаунда. Весовое отношение CaO к SiO2 =1,86 для соединения двухкальциевого силиката, 2CaO.SiO2. Хотя до сих пор ни одна доменная печь не работала успешно с использованием шлаков с отношением CaO к SiO2, приближающимся к 1,86, в шлаках действующих доменных печей могут образовываться значительные количества двухкальциевого силиката. Образование достаточного количества двухкальциевого силиката приводит к образованию твердого шлака, который при охлаждении распадается на пыль, известный как «падающий» или «пылящий» шлак. Разрушение вызвано 10-процентным объемным расширением двухкальциевого силиката, когда он претерпевает фазовый переход при 675 °C. Рекомендуемое значение для предотвращения «падающего» шлака составляет (CaO) менее 0,9(SiO2) + 0,6(CaO). A2O3) + 1,75 (с).
Важно помнить, что фазовые диаграммы основаны на условиях равновесия. Равновесные условия подразумевают, что скорость охлаждения медленнее скорости реакций, таких как образование двухкальциевого силиката. Описанный выше путь отверждения «обойден», если скорость охлаждения очень высока, как при гранулировании шлака и, в меньшей степени, при гранулировании шлака. Быстрое охлаждение блокирует композицию в твердой стеклофазе, где кинетика реакций слишком медленная для образования соединений.
Поток шлака В горне – Контроль уровня шлака в горне важен для поддержания стабильной работы печи, особенно в связи с увеличением производительности чугуна. Высокий уровень шлака приводит к увеличению давления дутья и стенок зазора, а также к нарушению равномерного опускания шихты. Одной из проблем контроля уровня шлака является течение шлака в горне при выпуске. В горне стекание шлака к летке затруднено, чем стекание горячего металла к летке. Течение жидкого металла имеет большую движущую силу из-за более высокой плотности жидкого металла по сравнению со шлаком. Путь потока горячего металла, как полагают, в основном проходит через «свободные от кокса» области ниже и/или вокруг кокса. Путь потока шлака к летке проходит через кокс.
На рис. 4 показана конфигурация пода и возможная последовательность стадий пода при выпуске, которые приводят к ложному состоянию сухого пода в конце выпуска. Считается, что поверхность горячего металла остается относительно плоской по всей площади пода во время выпуска из-за высокой плотности горячего металла и «свободного от кокса» пути к летке. Поверхность шлака в районе летки может быть значительно ниже, чем в других областях горна. Когда скорость выпуска шлака выше, чем скорость потока шлака через горн в область летки, в области летки происходит истощение шлака, и поверхность шлака начинает изгибаться вниз по направлению к летке, как показано на шаге 4 Рис. 4. Истощение шлака продолжается до тех пор, пока в летке не останется шлака, и печь не будет казаться сухой, когда в горне все еще остается значительное количество шлака, как показано на шаге 5 на рис. 4. Сведение к минимуму сопротивления течению шлака в горн сводит к минимуму количество шлака, остающегося в горне в конце выпуска. Resistance to slag flow in the hearth is reduced as the porosity of the hearth coke bed is increased and the slag viscosity is reduced.
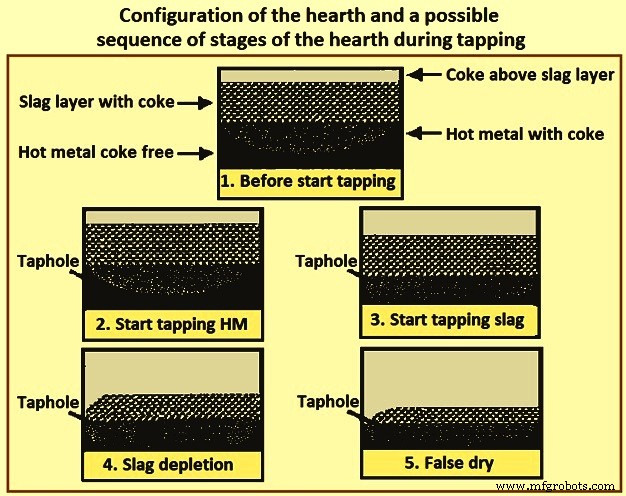
Fig 4 Configuration of the hearth and a possible sequence of stages of the hearth during tapping
Oxide system
Around 95 % of the slag consists of SiO2, CaO, MgO, and Al2O3. The requirement of low viscosity can be met by a variety of components in this quaternary system. Ignoring the presence of MgO, the phase diagram of the ternary oxide system CaO-Al2O3- SiO2 (Fig 5) shows a low melting temperature region which is parallel to the CaO-SiO2 binary with low Al2O3 content. This region extends from high SiO2 content to the saturation isotherm for 2CaO.SiO2 and then for essentially constant CaO content toward high Al2O3 content. The MgO content of the slag does not substantially affect the relative position of the low melting temperature region and only affects the absolute values of the melting temperatures.
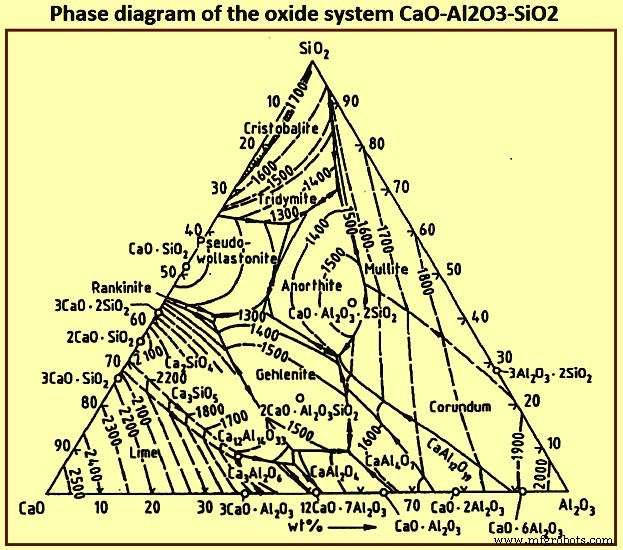
Fig 5 Phase diagram of the oxide system CaO-Al2O3- SiO2
The oxide system which forms the basis for BF slags is the lime-silica-alumina (CaO-SiO2-Al2O3) system modified due to the presence of certain percent of MgO in the slag. Fig 6 shows the phase diagram of CaO-Al2O3-SiO2-10 % MgO system.
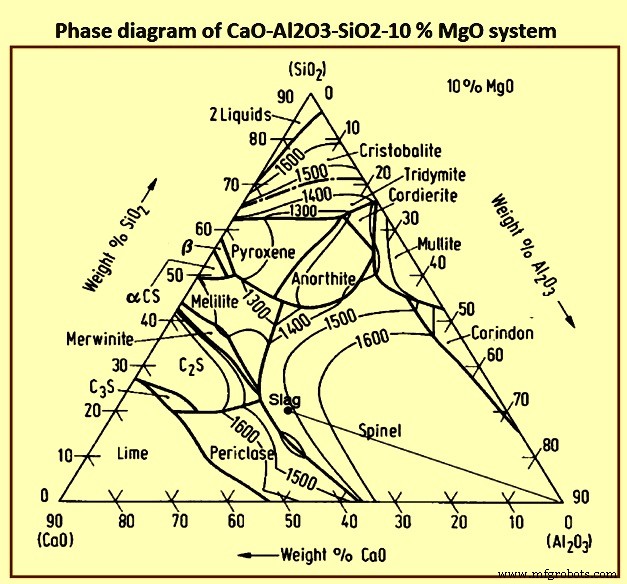
Fig 6 Phase diagram of CaO-Al2O3-SiO2-10 % MgO system
The compositions of BF slags as encountered under various operating conditions are shown in Fig 7. The desulphurization of hot metal increases with slag basicity, i.e. with increasing CaO and / or MgO content, region 1 in Fig 7 can, hence, be used only for processing low sulphur burden. Since the gangue constituents normally form a low basicity slag, region 1 largely represents the slag composition without addition of fluxes. The furnace can be operated at a relatively low temperature because of the low melting points. Region 2 is reached for low iron content burden with acid gangue constituents. This mode of operation prevails, and needs extensive desulphurization of the hot metal outside of the BF. The attainment of a basicity which results in adequate desulphurization within the furnace needs a large lime (CaO) addition which leads to a high slag volume and hence a higher coke rate. Region 3 represents the world wide preferred slag compositions for large blast furnaces. In this case, depending on the alumina content, dolomite is to be added to satisfy the needed MgO contents.
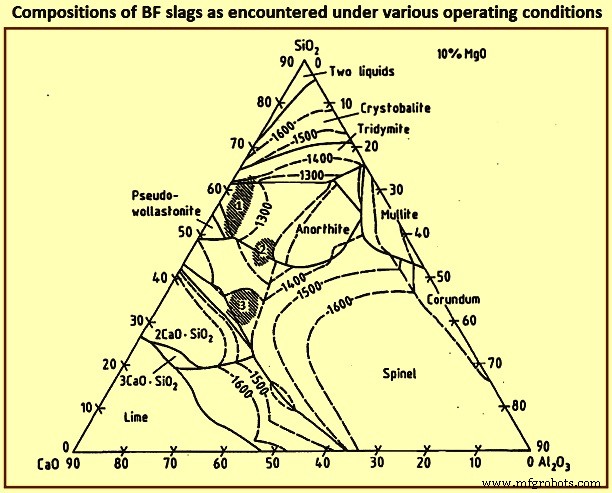
Fig 7 Compositions of BF slags as encountered under various operating conditions
Tab 1 shows the optimum components of the BF slag. Slags with higher basicities (B) as shown in Tab 1 do favour optimum softening conditions. The softening and the melting range of the gangue constituents is around 80 deg C to 130 deg C for B=0.5, and around 20 deg C to 50 deg C for B =2. Because of the higher melting temperature of the highly basic slag and of extra energy needed due to the larger quantity of the flux addition, the slag basicity is hence maintained at around 1.2.
| Tab 1 Optimum composition of BF slag | |||
| Al2O3 | CaO | MgO | SiO2 |
| % | % | % | % |
| 5 | 43 | 16 | 36 |
| 10 | 44 | 14 | 32 |
| 15 | 44 | 12.5 | 28.5 |
| 20 | 45 | 11 | 24 |
| 25 | 48 | 8 | 19 |
| 30 | 56 | 5 | 9 |
| 35 | 54 | 4 | 7 |
Slag properties
The physical and chemical properties of slags are primarily a function of the slag composition and temperature. The following describes these relationships for the purpose of developing general trends.
Liquidus temperatures – The relationships of liquidus temperature and composition for the four primary components of slag are represented on a quaternary phase diagram. Fig 8 has been generated from ternary planes of the quaternary phase diagram. Figures 8a and 8b are not phase diagrams. There are two general trends derived from these figures. The first is that the liquidus temperatures increase with increases in (Al2O3) and B/A, and the second is that the (MgO) in the range of 8 % to 14 % tends to minimize the increase in liquidus temperature caused by the increase in either (Al2O3) or B/A.
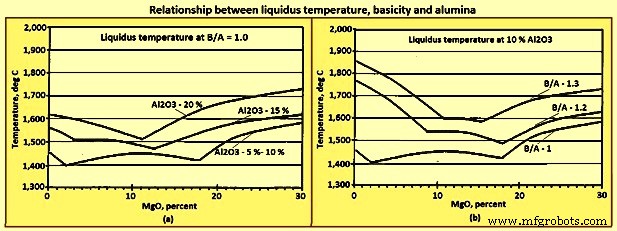
Fig 8 Relationship liquidus temperature, basicity, and alumina
Viscosity – Viscosity is a measure of the quantity of force needed to change the form of a material and is reported in unit called ‘poise’. The higher the viscosity, the more force is needed to cause a liquid to flow. For comparison purposes considering that at 20 deg C the viscosity of water is 0.01002 poise, a typical acceptable slag viscosity is around 2 to 5 poise, and the viscosity of the liquid SiO2 is of the order of 100,000 poise. The high viscosity of liquid SiO2 is caused by the polymer structure. The breakdown of the polymer structure by the basic oxides lowers the viscosity. The decrease in the viscosity of all liquid slags with increasing the B/A is shown Fig 9a. In general, the viscosity of any liquid / solid mixture increases as the quantity of suspended solids increases. The impact of temperature on slag viscosity is considerably higher at temperatures below the liquidus temperature than above the liquidus temperature as shown in Fig 9b.
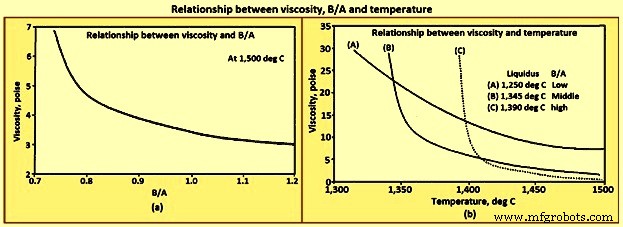
Fig 9 Relationship between viscosity, B/A and temperature
There are two general trends which are seen for the viscosity. Above the liquidus temperature, the viscosity of liquid slags decreases with increasing temperature and B/A. At temperatures below the liquidus temperature, the viscosity decreases with increasing temperature, and decreasing B/A.
Sulphur partition ratio – The BF ironmaking is a very good desulphurizing process compared to the steelmaking process because of the difference in the oxygen potential of the slags of the processes. The effect of the oxygen potential on desulphurization can be shown using equation (CaO) + [S] =(CaS) + (FeO), where the oxygen potential is indicated by the (FeO). The higher the (FeO) the more the reaction is driven to the left and the higher the [S]. Steelmaking slags with (FeO) of 15 % to 25 % are, hence, weaker desulphurizing slags than the BF hearth slags with (FeO) of less than 1 %.
Essentially all the sulphur into the BF leaves the furnace in the hot metal and slag. A relationship for the prediction of [S] can be developed based upon a mass balance of sulphur for one ton of hot metal, as per the equation (i) below, and the defined term sulphur partition as per the equation (ii) below. The prediction of [S], by equation (iii) below, is derived by the substitution of [S] from the equation (i) into equation (ii) and then solving for [S].
Equation(i) is St =[S] /100 x 1,010 + (S) /100 x Svol where 1,010 is the kgs of hot metal in a ton of hot metal including a 1 % yield loss, St is the sulphur loading which is the total weight of sulphur in kgs/tHM. Svol is the slag volume which is the weight of slag in kgs/tHM. Equation (ii) Sp =(S) /[S] where Sp is the sulphur partition ratio. Equation (iii) is [S] =St x 100 / (Sp x Svol + 1,010).
The slag Sp can be predicted based upon equation (iv) Sp =147.7 x BB + 37.7 x [Si] – 190 and equation (v) BB ={(CaO) + 0.7(MgO)} / {0.94(SiO2) + 0.18(Al2O3)}. Here BB is the basicity as defined by the bell’s ratio. It is to be noted that the coefficients in equation (iv) have been developed from regression analysis of a specific furnace. Equation (iv) and equation (v) have been used to construct Fig 10(a), and equation (iii), equation (iv), and equation (v) have been used in the construction of Fig 10 (b).
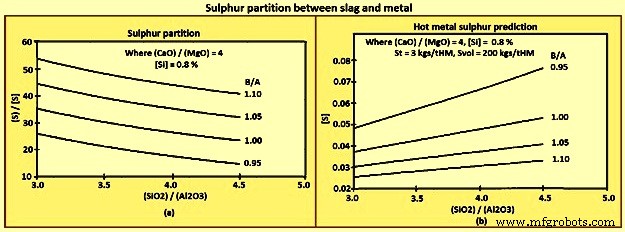
Fig 10 Sulphur partition between slag and metal
The general trends which can be derived from the above equations and figures are (i) [S] decreases with decreasing St and increasing Sp and Svol, (ii) however, Sp normally increases with B/A, (iii) CaO is a better desulphurizer than MgO, and (iv) Al2O3 has a smaller effect on Sp than SiO2.
Alkali capacity – A ‘refluxing’ or ‘recycling’ phenomena occurs in the BF due to the counter-current flow of gases versus solids / liquids, particularly for sulphur, zinc, and alkalis. The recycling of the alkali potassium (K) is shown in Fig 11a. The recycling phenomena is when an element travels down the furnace in a solid or liquid phase, reacts to form gas species in the higher temperature regions of the furnace, then travels back up the furnace as gases, where it reacts and is absorbed by the solid / liquid phases in the lower temperature region of the furnace. The recycling results in much higher internal concentrations of the recycled element than the concentration going in or out of the furnace. For example the internal loading of K can be 10 kgs/tHM, when the materials being charged contain only 2 kgs/tHM.
Alkalis have no beneficial, but many deleterious effects on the BF. Alkalis are absorbed by refractories, coke, and ore causing degradation of the refractories and coke, and ore swelling. Alkalis can also form scabs which can peel off upsetting the thermal condition of the furnace, or build up and constrict burden and gas flow. Alkalis cannot be avoided as they are contained in all coals, cokes, and to a lesser extent ores. The alkali loading is to be minimized wherever possible.
A portion of the alkalis leave the furnace in the top gas, the quantity being a function of the top temperature profile. The remaining alkalis are to be removed in the slag. The ability of slag to remove alkalis from the furnace is referred to as the alkali capacity of the slag. The relationships of alkali capacity to slag composition and temperature are shown in Fig 11b. In general the alkali capacity increases with lower B/A, and with lower temperature.
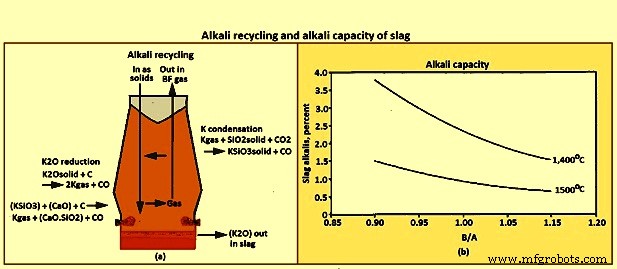
Fig 11 Alkali recycling and alkali capacity of slag
Silica activity – The [Si] produced is dependent upon the burden materials, furnace operation, and slag chemistry. The impact of the slag chemistry is shown in the equation [Si] =(SiO2) x GSiO2 / GSi x Keq / (P to the power 2)co. Here CO is carbon mono-oxide. This equation is developed from the equilibrium constant, equation Keq ={ASi x (P to the power 2)co} / { ASiO2 x Ac}, for the reaction given in equation (SiO2) + 2C =[Si] + 2COgas, the definitions of the activities of (SiO2) and [Si], equation ASiO2 =(SiO2) x GSiO2 and equation ASi =[Si] x GSi, and assuming that the activity of the carbon in the hearth is equal to one. The trend implied by Equation [Si] =(SiO2) x GSiO2 / GSi x Keq / (P to the power 2)co is that the [Si] decreases as the (SiO2) decreases.
Slag design factors
In some of the BFs, a typical slag composition which is formed from the gangue in the ore and ash of the coke is 9 % CaO, 5 % MgO, 75 % SiO2, and 10 % Al2O3. A slag of this composition has a liquidus temperature of the order of 1,600 deg C and does not flow well even above its liquidus temperature. Hence, CaO and MgO are added to the burden to ‘flux’ the gangue and ash resulting in acceptable liquidus temperatures and flow characteristics.
Basic slag design is the selection of the types and quantities of fluxes to be used with a burden and coke to produce a slag of acceptable properties. Burden and coke selections are largely driven by economic issues such as local versus imported sources and degree of beneficiation. These economic driving forces have resulted in a wide range of slag compositions throughout the world.
The general factors to be considered in designing a slag for normal operation are (i) liquidus temperature, that is, the slag is to be completely liquid in the hearth and cast house, (ii) viscosity, that is, the slag is to have a low viscosity, high fluidity, so as to drain from the hearth and down the cast house runners, (iii) sulphur capacity that is the Sp is to be sufficient to produce hot metal with sulphur contents within specifications, (iv) alkali capacity, that is, the slag alkali capacity is to be sufficient to prevent alkali build up in the furnace, (v) hot metal silicon control, that is, the effect of the slag chemistry on the [Si] is to be considered, (vi) slag volume, that is, the slag volume is to be high enough to contribute to the stability of the slag properties and hot metal quality, but not so high as to require excessive fuel or contribute to furnace instability, (vii) robust properties, that is, the slag properties are to be as insensitive to variations in normal variations in furnace operation as possible, specifically hot metal temperature, and (viii) end use, that is, the requirements of the end use of the slag is to be considered.
Slag design is to recognize that the above factors are not independent and that the design always involves a balancing of the above factors to resolve the conflicting trends (Tab 2).
| Tab 2 Normal conflicting trends | ||
| Desired parameter | Basicity | Al2O3 |
| Lower liquidus temperature | Lower | Lower |
| Lower viscosity | Higher | |
| Higher K removal | Lower | Lower |
| Lower [S] | Higher | Higher |
| Lower [Si] | Higher | Higher |
Two examples of the slag design are described below. In the first example (Tab 3) , the issue is to increase the alkali removal without increasing the [S]. The resolution of the issue is to increase the slag volume through the use of additional SiO2 in the burden, while decreasing the slag basicity.
| Tab 3 Example of designing slag for increased K2O removal | |||||
| Basicity | Slag volume | K2O | K2O removed | (S) | S removed |
| B/A | kgs/tHM | % | kgs/tHM | % | kgs/tHM |
| 1.10 | 225 | 0.47 | 1.30 | 1.82 | 5.00 |
| 1.05 | 282 | 0.55 | 1.55 | 1.77 | 5.00 |
| 1.00 | 290 | 0.63 | 1.85 | 1.72 | 5.00 |
| 0.95 | 298 | 0.71 | 2.10 | 1.68 | 5.00 |
The issue in the second example (Tab 4) is to lower the [Si] without negatively impacting the other properties of slag and furnace operation. The resolution of the issue is to decrease the (SiO2) by increasing the (Al2O3) using quartzite, a high (Al2O3) burden material, while holding the (CaO) and (MgO) constant. The change in slag chemistry results into a decrease of both [Si] and [S].
| Tab 4 Example of designing slags with lower [Si] | |||||
| Period | Unit | Base | Number 1 | Number 2 | Number 3 |
| Basicity | 1.12 | 1.13 | 1.13 | 1.12 | |
| (MgO) | % | 11.8 | 11.5 | 11.7 | 11.5 |
| (Al2O3) | % | 7.8 | 10.2 | 10.3 | 11.7 |
| [Si] | % | 0.76 | 0.53 | 0.54 | 0.49 |
| [S] | % | 0.043 | 0.031 | 0.029 | 0.026 |
Slag after the BF
The use of BF slag is driven by the economics of processing and market demand. In the place, where the processing and marketing is performed by the organization producing the slag, the markets tend to be local in nature with minimal processing. As per the present trend, independent organizations take ownership of the liquid slag at the end of the slag runner which has led to wider markets with more extensive processing. The product slag can be classified by the rate of cooling.
Air-cooled slags are those produced with low cooling rates. These are slags which are solidified in pits and frequently cooled with water sprays. The largest uses for air cooled slag are in road construction, railroad ballast, and aggregate. Air-cooled slag has also been used in the production of cement, mineral wool insulation, roofing, and glass.
Pelletized and granulated slags are those produced with high cooling rates. Pelletized slag is produced by pouring liquid slag onto a rotating drum, sometimes with water. Granulated slags are produced by either pouring the liquid slag directly into a large slag pit of water or through the use of high pressure water sprays which breaks the slag up into droplets. Rapidly cooled slags have been used for the same applications as air-cooled slags. The high glass content of rapidly cooled slags makes it particularly suitable for Portland cement production.
Производственный процесс
- Система автоматизации, измерения и управления доменными процессами
- Производство и использование доменного газа
- Грануляция доменного шлака в литейном цехе
- Производительность доменной печи и влияющие параметры
- Высокоглиноземистый шлак и доменная печь
- Неисправности доменной печи во время работы
- Промковш и его роль в непрерывном литье стали
- Сухая грануляция доменного шлака для рекуперации энергии
- Производство чугуна в доменной печи и выбросы оксида углерода
- Точное машиностроение и его роль в производстве



